Материал: Углерод
Углерод
Введение
Современная промышленность электроники находится в
состоянии постоянной погони за уменьшением размеров интегральных схем,
благодаря чему увеличивается скорость, уменьшается потребление энергии и
себестоимость изготовления одного транзистора. В последние десятилетие одним из
лидирующих материалов в электронике является кремний. Но серьезную конкуренцию
могут кремнию может составить углерод, точнее его аллотроп - углеродная
нанотрубка.
1. Общие сведения об углероде
Углерод в периодической системе Менделеева расположен 4-й группе, атомный
номер 6, атомная масса 12.011 /7/. Ядро изотопа ![]() состоит из шести протонов и шести
нейтронов. В1961 году Международным союзом фундаментальной и прикладной химии
изотоп
состоит из шести протонов и шести
нейтронов. В1961 году Международным союзом фундаментальной и прикладной химии
изотоп ![]() выбран основной единицей измерения
атомной массы. Изотоп
выбран основной единицей измерения
атомной массы. Изотоп ![]() радиоактивен и имеет период полураспада 57600 лет, имеется
также нуклеотид
радиоактивен и имеет период полураспада 57600 лет, имеется
также нуклеотид ![]() .
.
Нейтральный атом углерода содержит шесть электронов. Два из них находятся вблизи ядра и образует первый K-слой (1s-состояние). Следующие четыре электрона образуют второй электронный L-слой. Два из четырех электронов находятся в 2s-, а два - в 2p-состоянии.
Нейтральный атом углерода в основном состоянии двухвалентен и имеет
конфигурацию 1![]() 2
2![]() 2
2![]() . Однако в большинстве химических соединений углерод
четырехвалентен. Это состояние получается при переходе одного электрона из
состояния 2sв 2p; данному возбужденному состоянию соответствует конфигурация
1
. Однако в большинстве химических соединений углерод
четырехвалентен. Это состояние получается при переходе одного электрона из
состояния 2sв 2p; данному возбужденному состоянию соответствует конфигурация
1![]() 2s2
2s2![]() 2
2![]() 2
2![]() . Электронные облака, имеющие вид объемных восьмерок,
вытянуты вдоль координатных осей. Переход атома углерода из основного состояния
1
. Электронные облака, имеющие вид объемных восьмерок,
вытянуты вдоль координатных осей. Переход атома углерода из основного состояния
1![]() 2
2![]() 2
2![]() в возбужденноесостояние 1
в возбужденноесостояние 1![]() 2s2
2s2![]() требует энергии порядка 400 кДж/моль, которая затем
компенсируется при образовании химических связей.
требует энергии порядка 400 кДж/моль, которая затем
компенсируется при образовании химических связей.
Существуют три основные валентные состояния атома углерода, от которых зависит характер химических связи между атомами углерода - за счет перекрывания электронных оболочек. От его степени зависит прочность связей. Вытянутые в виде восьмерок 2p-орбитали образуют направленные связи.
Первое валентное s![]() -состояние описывается тетраэдрической моделью. В таком
состоянии находится углерод в молекулах метана
-состояние описывается тетраэдрической моделью. В таком
состоянии находится углерод в молекулах метана ![]() , где атом углерода расположен в
центре тетраэдра, в вершинах которого на одинаковых расстояниях от C- атома расположены атомы водорода.
Углы между направлениями C-H связей одинаковы(109,5°), и эти
четыре эквивалентные связи получаются в результате смещения одного s-электрона и трех p-электронов. В этом случае
отсутствует четкое подразделение на s- и p- электроны, и атом углерода
находится в гибридном состоянии. Данная модель хорошо объясняет конфигурацию
связей углеродных атомов в кристалле алмаза и предельных углеводородах. Рисунок
данной модели изображен на рис. 1.1.
, где атом углерода расположен в
центре тетраэдра, в вершинах которого на одинаковых расстояниях от C- атома расположены атомы водорода.
Углы между направлениями C-H связей одинаковы(109,5°), и эти
четыре эквивалентные связи получаются в результате смещения одного s-электрона и трех p-электронов. В этом случае
отсутствует четкое подразделение на s- и p- электроны, и атом углерода
находится в гибридном состоянии. Данная модель хорошо объясняет конфигурацию
связей углеродных атомов в кристалле алмаза и предельных углеводородах. Рисунок
данной модели изображен на рис. 1.1.
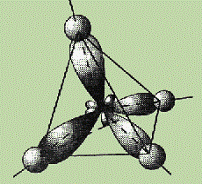
Рисунок 1.1 - Схема тетраэдрической модели
Второе валентное s![]() -состояние описывается тригональной моделью и наблюдается в
предельных органических соединениях с двойной связью. Таково состояние атомов
углерода в ароматических состояниях соединениях и графите. Изэкспериментальных
наблюдений следует, что атом углерода при этом имеет три равномерные
-состояние описывается тригональной моделью и наблюдается в
предельных органических соединениях с двойной связью. Таково состояние атомов
углерода в ароматических состояниях соединениях и графите. Изэкспериментальных
наблюдений следует, что атом углерода при этом имеет три равномерные ![]() - орбитали, расположеннее в плоскости
под углами 120°друг к другу, которые образуются в результате смещения двух p-электронов и одного s-электрона(s
- орбитали, расположеннее в плоскости
под углами 120°друг к другу, которые образуются в результате смещения двух p-электронов и одного s-электрона(s![]() -гибридизация). Четвертый электрон
соответствует
-гибридизация). Четвертый электрон
соответствует ![]() -орбитали, его гантелеобразное симметричное облако вытянуто
вдоль нормали плоскости (рисунок 2). Такая гибридизация наблюдается в этилене,
графите, бензоле и других ароматических соединениях. Связи между атомами в этом
случае осуществляется тремя
-орбитали, его гантелеобразное симметричное облако вытянуто
вдоль нормали плоскости (рисунок 2). Такая гибридизация наблюдается в этилене,
графите, бензоле и других ароматических соединениях. Связи между атомами в этом
случае осуществляется тремя ![]() - связями и одной
- связями и одной ![]() - связью.
- связью.
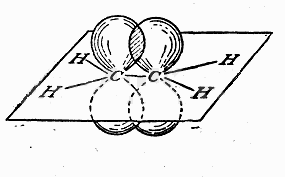
Рисунок 1.2 - Схема тригональной модели
Третье валентное sp-
состояние атомов углерода отмечается в некоторых веществах с тройными связями
между углеродными атомами. Оно описывается диагональной моделью и характерно
для ацетилена (HC![]() CH), синильной кислоты (HC
CH), синильной кислоты (HC![]() N)и др. Тройная углеродная связь соответствует одной тремя
N)и др. Тройная углеродная связь соответствует одной тремя ![]() - связи и двум
- связи и двум ![]() - связям. Это валентное состояние (sp- гибридизации) возникает при
смешивании одного s- электрона с
одним p- электроном, после чего они образуют
две гибридные орбитали, имеющие вид асимметричных гантелей. Эти орбитали
участвуют в образовании
- связям. Это валентное состояние (sp- гибридизации) возникает при
смешивании одного s- электрона с
одним p- электроном, после чего они образуют
две гибридные орбитали, имеющие вид асимметричных гантелей. Эти орбитали
участвуют в образовании ![]() - связей, угол между которыми 180°. Два другие электрона
образует
- связей, угол между которыми 180°. Два другие электрона
образует ![]() - связи.
- связи.
Таким образом, в углеродных материалах могут реализоваться два основных
типа ковалентных связей: ![]() и
и ![]() . Первые образуются за счет перекрытия электронных облаков в
направлении связей (рисунок 1.3).
. Первые образуются за счет перекрытия электронных облаков в
направлении связей (рисунок 1.3).
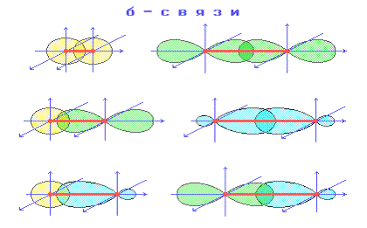
Рисунок 1.3 - Схема ![]() - связи
- связи
Связь, образующаяся за счет бокового перекрытия p-орбиталей перпендикулярно линии связей, называется ![]() - связью (рисунок 1.4). Она менее
прочна, чем
- связью (рисунок 1.4). Она менее
прочна, чем ![]() - связь, поскольку перекрытии электронных орбиталей при
- связь, поскольку перекрытии электронных орбиталей при ![]() - слабее. Таким образом, связи в
соединениях с s
- слабее. Таким образом, связи в
соединениях с s![]() - гибридизацией - это четыре
- гибридизацией - это четыре ![]() - связи, для s
- связи, для s![]() - гибридизации это три
- гибридизации это три ![]() - связи и одна
- связи и одна ![]() - связь, а при sp- гибридизации - две
- связь, а при sp- гибридизации - две ![]() - связи и две
- связи и две ![]() - связи
- связи
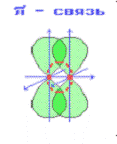
Рисунок 1.4 - Схема ![]() - связи
- связи
Атом углерода имеет довольнобольшое количество аллотропов. Степень
гибридизации этих аллотропов разная - ![]() , где n - дробное число: 1 <n< 3. (показано на рисунках 1.5)
, где n - дробное число: 1 <n< 3. (показано на рисунках 1.5)
углерод нанотрубка хиральность атом
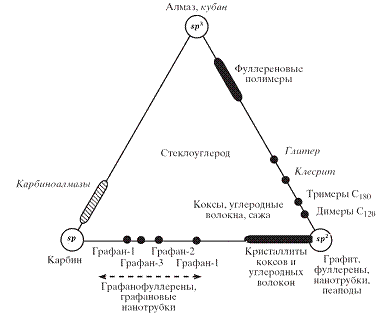
Рисунок 1.5 - Схема классификации углеродных материалов в зависимости от степени гибридизации составляющих их атомов
Согласно схеме 1.5. аллотропы углерода могут иметь
определенную степень гибридизации: ![]() - алмаз;
- алмаз;![]() -графит, фуллерены, нанотрубки,
пеаподы;
-графит, фуллерены, нанотрубки,
пеаподы; ![]() - карбин. Также аллотропы могут
иметь промежуточную степень гибридизации
- карбин. Также аллотропы могут
иметь промежуточную степень гибридизации ![]() , где n - дробное число: 1 <n< 3. Если
, где n - дробное число: 1 <n< 3. Если ![]() то аллотроп является углеродным моноциклом(графаны и его
модификации), при
то аллотроп является углеродным моноциклом(графаны и его
модификации), при ![]() аллотроп будет замкнуто-каркасной структурой (фуллереновые
полимеры, глитер, клесрит, триммеры и димеры). Еще аллотропы углерода могу
иметь смешанную степень гибридизации
аллотроп будет замкнуто-каркасной структурой (фуллереновые
полимеры, глитер, клесрит, триммеры и димеры). Еще аллотропы углерода могу
иметь смешанную степень гибридизации ![]() . Это аллотропы помешенные в центре
треугольника схемы 1.5 стеклоуглерод, кокс, углеродные волокна, сажа. Также
некоторые аллотропы углерода могут находится в
. Это аллотропы помешенные в центре
треугольника схемы 1.5 стеклоуглерод, кокс, углеродные волокна, сажа. Также
некоторые аллотропы углерода могут находится в ![]() гибридизации - это карбиноалмазы.
гибридизации - это карбиноалмазы.
2. Структура нанотрубок
2.1 Хиральность нанотрубки
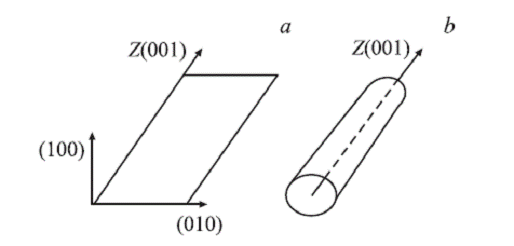
Рисунок 2.1 - Рисунок плоскости (a) и цилиндра (b)
Идеальная однослойная нанотрубка представляет собой свернутую в цилиндр
графитовую плоскость, причем плоскость выложена правильными шестиугольниками, в
вершинах которых расположены атомы углерода /1/. В графитовой плоскости задается
базис согласно рисунку 2.2.
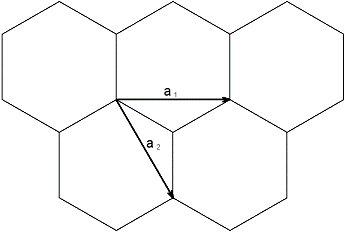
Рисунок 2.2 - Схема графитовой плоскости с заданным базисом векторов
Сворачивание плоскости в цилиндр происходить может под любым углом между
вектором ![]() графитовой плоскости и перпендикуляром
оси нанотрубки, так называемый угол ориентации. Угол ориентации задает
хиральность нанотрубки, которые определяет многие физические характеристики, в
частности, электрические, тепловые и многие другие свойства.
графитовой плоскости и перпендикуляром
оси нанотрубки, так называемый угол ориентации. Угол ориентации задает
хиральность нанотрубки, которые определяет многие физические характеристики, в
частности, электрические, тепловые и многие другие свойства.
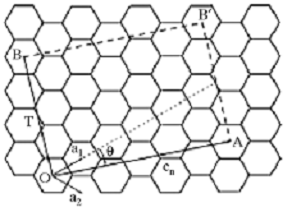
Рисунок 2.3 - Схема иллюстрирующая угол ориентации![]() , где T - направление оси,
, где T - направление оси, ![]() - перпендикуляр оси направления
- перпендикуляр оси направления
Хиральность нанотрубок в базисе (![]() )обозначается набором символов (т,п),
указывающим координаты шестиугольника, который в результате сворачивания
плоскости должен совпасть с шестиугольником, находящимся в начале координат.
Некоторые из таких шестиугольников вместе с соответствующими обозначениями отмечены
на рисунке. Другой способ обозначения хиральности состоит в указании угла
)обозначается набором символов (т,п),
указывающим координаты шестиугольника, который в результате сворачивания
плоскости должен совпасть с шестиугольником, находящимся в начале координат.
Некоторые из таких шестиугольников вместе с соответствующими обозначениями отмечены
на рисунке. Другой способ обозначения хиральности состоит в указании угла ![]() между направлением сворачивания
нанотрубки и направлением, в котором соседние шестиугольники имеют общую
сторону Среди различных возможных направлений сворачивания нанотрубок
выделяются направления для которых совмещение шестиугольника (т,п) с
началом координат не требует искажения в его структуре. Этим направлениям
соответствуют угол
между направлением сворачивания
нанотрубки и направлением, в котором соседние шестиугольники имеют общую
сторону Среди различных возможных направлений сворачивания нанотрубок
выделяются направления для которых совмещение шестиугольника (т,п) с
началом координат не требует искажения в его структуре. Этим направлениям
соответствуют угол ![]() = 0 (armchair-конфигурация) и
= 0 (armchair-конфигурация) и ![]() = 30° (zigzag-конфигурация)
Указанные конфигурации отвечают хиральностям (т, 0) и (2n, п) соответственно.
= 30° (zigzag-конфигурация)
Указанные конфигурации отвечают хиральностям (т, 0) и (2n, п) соответственно.

Рисунок 2.4 - Атомные модели основных конфигураций нанотрубок: a - armchair, b - zigzag,
c -хиральная нанотрубка
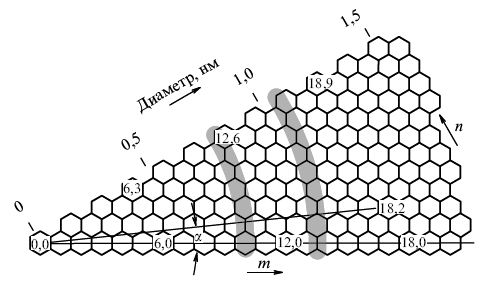
Рисунок 2.5 - Схема иллюстрирующая зависимость
индексов хиральности, угла ориентации и диаметр нанотрубок
Индексы хиральности однослойной нанотрубки (т, п) однозначным
образом определяют ее диаметр D.Эта связь
имеет следующий вид:
![]()
где d0= 0,
142 нм - расстояние между соседними атомами углерода в графитовой плоскости
Связь между индексами хиральности (т, п) и углом ![]() дается соотношением:
дается соотношением:
![]()
Разрешающая способность современных электронных микроскопов недостаточна
для непосредственного различения хиральностинанотрубок, поэтому основной способ
определения данного параметра связан с измерением их диаметра.
2.2 Однослойные нанотрубки
На рисунке 3.1 представлена идеализированная модель
однослойной нанотрубки /1/. Такая трубка не образует швов при сворачивании и
заканчивается полусферическимивершинами, содержащими, наряду с правильными
шестиугольниками, также по шесть правильных пятиугольников. Наличие
пятиугольников на концах трубок позволяет рассматривать их как предельный
случай молекул фуллеренов, длина продольной оси которых значительно превышает
диаметр.
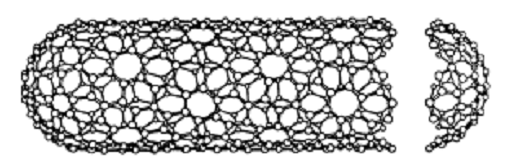
Рисунок 2.6 - Идеализированная модель однослойной нанотрубки
Структура однослойных нанотрубок, наблюдаемых экспериментально, во многих отношениях отличается от представленной выше идеализированной картины. Прежде всего, это касается вершин нанотрубки, форма которых, как следует из наблюдений, далека от идеальной полусферы.
.3 Многослойные нанотрубки
Многослойные нанотрубки отличаются от однослойных
значительно более широким разнообразием форм и конфигураций /1/. Разнообразие
структур проявляется как в продольном, так и в поперечном направлении.
Возможные разновидности поперечной структуры многослойных нанотрубок
представлены на рисунке2.3.1. Структура типа "русской матрешки" (russiandolls) (рисунок2.3.1а) представляет собой совокупность коаксиально вложенных друг
в друга однослойных цилиндрических нанотрубок. Другая разновидность этой
структуры, показанная на рисунке 2.3.1б, представляет собой совокупность
вложенных друг в друга коаксиальных призм. Наконец, последняяиз приведенных структур
(рисунок2.3.1в) напоминает свиток (scroll). Для всех приведенных структур характерно значение расстояния между
соседними графитовыми слоями, близкое к величине 0,34 им, присущей расстоянию
между соседними плоскостями кристаллического графита. Реализация той или иной
структуры в конкретной экспериментальной ситуации зависит от условий синтеза
нанотрубок.
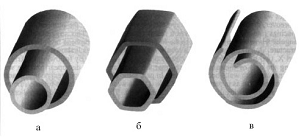
Рисунок 2.7 - Модели поперечных структур многослойных
нанотрубок: (а) "русская матрешка"; (б) шестигранная призма; (в)
свиток
Следует отметить, что несмотря на многочисленные
усилия, предпринимаемые исследователями, до настоящего времени не было получено
прямых экспериментальных данных, указывающих на преобладание той или иной
структуры многослойных наиотрубок, синтезируемых в конкретных условиях. Это
связано с недостаточно высокой разрешающей способностью существующей
экспериментальной аппаратуры (в частности, электронных микроскопов и
рентгеновских дифрактометров). Использование указанных приборов позволяет с достаточно
высокой точностью определить расстояние между соседними плоскостями в
многослойной нанотрубке, однако не позволяет отличить структуру свитка от
структуры "русской матрешки".