Материал: Учебное пособие ЭТМ
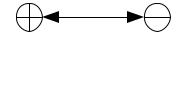
Полярные молекулы резко различаются по виду и размерам атомов, и по их электроотрицательности. Такие молекулы образуют несимметричную молекулу (электронная пара смещена в сторону более электроотрицательного атома). В результате у полярных молекул
R
образуется электрический дипольный момент p=q l , где q — электрический заряд; l — расстояние (рис. 3.2):
Рис. 3.2. Схема, поясняющая возникновение дипольного момента
Дипольный момент (p) измеряется в Кл·м или в Дебаях (Д), 1 Д = 3,3·10- 30 Кл·м.
Примеры неполярных и полярных молекул: Н2, Cl2 — неполярные молекулы (р = 0);
HCl (соляная кислота), С-О (оксид углерода), Н2О — полярные молекулы (р больше 0).
Полярные диэлектрики по сравнению с неполярными обладают значительно более низкими диэлектрическими характеристиками. Неполярные вещества применяются как лучшие диэлектрики. Особенно они важны для устройств, работающих в диапазоне сверхвысоких частот (СВЧ). Полярные вещества применяются там, где допустима изоляция среднего уровня.
Ковалентная связь является очень прочной связью. Это подтверждается, например, тем, что у карбида кремния (SiC) температура разложения порядка 2600 ° С; у углерода в модификации алмаза твердость 10 баллов. Приведенные в качестве примера вещества обладают ковалентной связью.
Данный тип связи наблюдается у веществ в газообразном, жидком и твердом состояниях, имеет место, как в диэлектриках, так и в полупроводниках.
33
3.1.2. Ионная связь
Ионная связь (гетерополярная связь) образуется за счет взаимного кулоновского притяжения разноименно заряженных ионов. При этом притяжение разноименно заряженных ионов превышает отталкивание одноименно заряженных. Эта связь наблюдается в, так называемых, ионных кристаллах, которые являются гигантской ассоциацией ионов.
Прочность или энергия (W) ионной связи определяется следую-
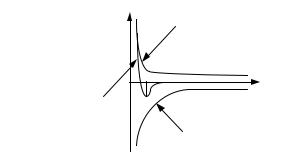
щим (рис. 3.3):
взаимным кулоновским притяжением положительных и отрицательных ионов;
отталкиванием внешних электронных оболочек этих же ионов, возникающим при очень малых расстояниях между ионами.
Рис. 3.3. Энергия ионной связи: δ — расстояние между положительными и отрицательными ионами; r0 — равновесное расстояние между положительными и отрицательными ионами
В итоге образуется кристаллическая структура, которая определяется величиной r0, размерами ионов и имеет минимум свободной энергии. Существует семь типов кристаллических решеток:
кубическая; гексагональная; тетрагональная; ромбическая; триклинная; моноклинная;
ромбоэдрическая (тригональная).
34
Ионные кристаллы образуются, в частности, из следующих эле-
ментов: |
|
|
|
|
|
|
|
|
с |
одной |
стороны |
элементы |
I, II |
и |
III |
групп |
таблицы |
Д. М. Менделеева, такие как: Li, Na, K, Be, Mg, Al, Y и др. ; |
|
|||||||
с |
другой |
стороны |
элементы |
VI |
и |
VII |
групп |
таблицы |
Д. И. Менделеева, такие как: О, F, Cl и др. |
|
|
|
|
||||
Таким образом, ионная связь чаще всего образуется между элементами I, II, III и VI, VII групп таблицы Д. И. Менделеева, т. е. соединяются атомы с резко различной электроотрицательностью.
Пример молекул с ионной связью: Li2O, MgO, NaCl и др. Ионная связь так же, как и ковалентная, очень прочная, напри-
мер, температура плавления оксида алюминия (Al2O3) 2040 °C, оксида магния (MgO) 2800 °C, диоксида тория ThO2 3050 °C. Перечисленные в качестве примера материалы имеют ионный тип связи.
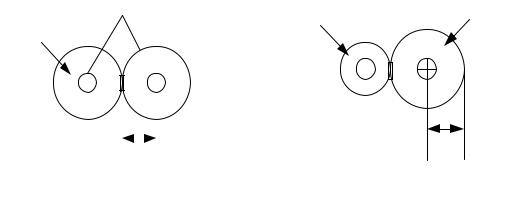
На рис. 3.4 приведены для сравнения молекулы фторсодержащих веществ, различающихся видами химической связи (ионной и ковалентной). Из рисунка видно, что радиус атома фтора в молекуле фтора, обладающей ковалентной связью, не равен радиусу иона фтора в молекуле фторида лития, обладающей ионной связью.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
а) |
|
|
|
|
|
|
|
|
|
б) |
||
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
||||
Рис. 3.4. Фторсодержащие молекулы с ковалентной и ионной связями: а) — молекула фтора (F2), ковалентная связь;
б) — молекула фторида лития (LiF), ионная связь
35
Ионная и ковалентная связи — два крайних вида связи, на практике, как правило, в веществах имеется ковалентная и ионная связи одновременно (смешанная связь) (табл. 3.1). Ионная связь наблюдается в диэлектриках и полупроводниках.
|
|
Таблица 3.1 |
|
Ионность связи |
|
|
|
|
Вещество |
Ионность связи, в долях единицы |
Вид связи |
|
|
|
SiC |
приблизительно 0 |
Ковалентная |
|
|
|
NaCl |
приблизительно 0,94 |
Ионная |
|
|
|
ZnO |
приблизительно 0,62 |
Смешанная |
|
|
|
3.1.3. Металлическая связь
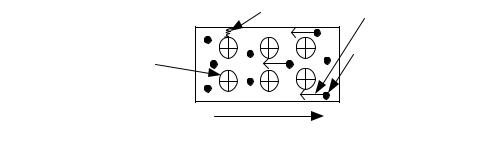
Металлическая связь имеет место в веществах, состоящих из положительно заряженных ионов, находящихся в узлах кристаллической решетки, и квазисвободных (обобществленных, коллективизированных, легко перемещаемых под действием электрического поля) электронов (рис. 3.5).
Рис. 3.5. Схема металлической связи:
Е — напряженность электрического поля; v — скорость
Вещества с металлической связью имеют: высокую электропроводность; высокую теплопроводность;
высокую отражательную способность (блеск);
высокую плотность упаковки (плотность d не менее 22,6 г/см3); пластичность.
36
Вещества, обладающие таким набором свойств, являются ме-
таллами — проводниками (Ag, Cu, Au, Al, Li, Na, Fe и др.).
Металлическая связь, такая же прочная, как ионная и ковалентная, например, температура плавления вольфрама 3380 ° С. Вместе с тем имеются металлы, у которых наблюдается низкая температура плавления Тпл. Например, температура плавления ртути — 39 ° С, це-
зия + 28,5 ° С, галлия + 30,0 ° С.
3.1.4. Молекулярная связь
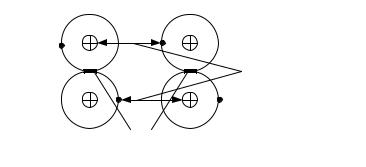
Молекулярная связь (связь Ван– дер– Ваальса) возникает между молекулами, внутри которых уже имеется ковалентная связь. Эта связь обусловлена синхронным движением внешних валентных электронов, которые в каждый момент времени максимально удалены друг от друга (рис. 3.6). При этом силы притяжения валентных электронов положительно заряженными остовами соседних молекул оказываются сильнее сил взаимного отталкивания электронов внешних орбит.
Рис. 3.6. Схема молекулярной связи
Эта связь слабая, у нее низкая энергия связи. Энергия молекулярной связи приблизительно 0,05 – 0,2 эВ, в то время как, энергия связи молекулы с ионной связью, например, NaCl равна 8 эВ. Молекулярная связь легко разрушается тепловым движением. Так, парафин (СnH2n+2 , где n = 40 – 50), обладающий молекулярной связью, имеет температуру плавления 50 – 52 ° С. Наличие в веществе двух видов связи (ковалентной и молекулярной) приводит к тому, что у вещества наблюдается анизотропия свойств. Молекулярная связь имеет место в диэлектриках: полимеры, твердые Н2, N2, O2, Cl2 и др.
37