Материал: Теоретические основы теплотехники 1

81
нента
си |
pm |
p |
i |
|
G |
i |
ri . |
(212) |
|
|
|||||
p |
|
G |
||||
m |
|
|
|
|||
|
|
|
|
|
|
|
Из соотношения (212) следует, что парциальное давление i-го компо-
p |
i |
в смеси идеальных газов определяется через полное давление сме- |
|
|
и молярную концентрацию компонента ri
p i
r |
|
i |
|
pm
.
(213)
После преобразования соотношения (213) получаем, что сумма парци-
альных давлений всех компонентов смеси идеальных газов равна полному давлению смеси
n
p i i 1
n
= ri pm i 1
=
|
|
n |
p |
m |
i |
|
r |
|
|
|
i 1 |
=
pm
.
(214)
Поскольку внутренняя энергия и энтальпия идеального газа - функции только температуры, исходными соотношениями для определения средней температуры смеси идеальных газов Tm служат следующие соотношения:
в схеме смешения при V idem
U |
2 |
U |
1 |
G c |
vm |
T |
|
|
|
|
|
m |
|||
в схеме смешения при |
p |
||||||
|
n |
|
|
|
|
|
|
n |
|
|
|
|
|
G |
c |
T G c |
vm |
T |
|
|
G |
c |
T |
|
i |
vm,i |
i |
m |
|
i |
vm,i |
i |
|||
|
i 1 |
|
|
|
|
|
|
i 1 |
|
|
|
idem |
|
|
|
|
|
|
|
|
|
||
0
;
(215)
|
|
|
|
|
|
|
|
n |
|
|
|
|
|
|
|
n |
|
|
|
|
H |
2 |
H |
1 |
G c |
pm |
T |
|
|
G |
c |
pm ,i |
T G c |
pm |
T |
|
|
G |
c |
pm ,i |
T |
|
|
|
m |
|
i |
|
i |
m |
|
i |
|
i |
||||||||
|
|
|
|
|
|
|
|
i 1 |
|
|
|
|
|
|
|
i 1 |
|
|
|
|
0
.
(216)
С учетом этих соотношений (215), (216) получаем обобщенное выра-
жение по определению средней температуры смеси идеальных газов Tm для различных схем смешения

82
|
|
1 |
n |
|
|
|
1 |
n |
|
|
|
|
||
T |
|
r |
c |
|
T |
|
m |
c |
|
T |
||||
|
|
zm,i |
|
|
zm,i |
|||||||||
m |
|
с |
|
i |
|
i |
c |
|
i |
|
i |
|||
|
|
zm i 1 |
|
|
|
zm i 1 |
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
||||
,
(217)
где mi , ri |
– массовая и молярная концентрации |
сzm,i , czm,i |
– средние удельные массовая и молярная |
нента смеси в процессах z idem ( z p, v ); сzm , czm
совая и молярная теплоемкости смеси,
n |
|
czm mi czm,i |
, |
i 1 |
|
n |
|
czm ri czm,i . |
|
i 1 |
|
i-го компонента смеси;
теплоемкости i-го компо-
– средние удельные мас-
(218)
(219)
Объемная концентрация каждого компонента в смеси |
vi |
определяется |
как отношение приведенного объема Vi,пр компонента при давлении и темпе-
ратуре смеси к объему всей смеси V при тех же условиях
v |
Vi ,пр |
. |
(220) |
|
|||
i |
V |
|
|
|
|
||
Для идеального газа, исходя из уравнения состояния
|
|
|
|
|
|
|
|
|
|
|
|
|
Vi,пр = |
Gi R Tm |
, V = |
G RTm |
. |
(221) |
|||||||
|
|
|||||||||||
|
|
pm |
|
|
pm |
|
||||||
После подстановки Vi,пр и V в соотношение (220) получаем
v |
|
Gi |
|
||
i |
|
G |
|
|
ri
.
(222)
Отсюда следует, что для смесей идеальных газов объемная и молярная

83
концентрации компонентов численно равны.
Смеси реальных газов
Для расчетов характеристик смесей реальных газов обычно использу-
ется следующее уравнение состояния
pmV
z G R |
T |
m |
m |
z G
R
Tm
.
(223)
Определение значений коэффициента сжимаемости z для реальных га-
зовых смесей проводится с использованием закона соответственных состоя-
ний. Однако, в отличие от чистых газов, характеристики соответственных состояний определяются не по фактическим критическим параметрам, а по значениям приведенных критических (псевдокритиеских) давления pпк и
температуры Tпк газовых смесей:
n |
n |
|
|
pпк ri pк , i ; |
Tпк ri Tк , i , |
(224) |
|
i 1 |
i |
1 |
|
где pк,i и Тк,i критические давление и температура компонентов газовой смеси.
Псевдокритические параметры используются для вычисления значений приведенного давлений и температур смеси:
|
p |
|
p |
||
|
||
|
пк |
;
|
T |
|
T |
||
|
||
|
пк |
.
(225)
Значения критических параметров чистых газов приведены в табл. 2
84
Таблица 2
Критические характеристики газов
Газ |
, |
Тк, К |
pк, |
к, кг/м3 |
zк |
|
кг/кмоль |
МПа |
|||||
|
|
|
|
|||
Метан, СН4 |
16,04 |
190,55 |
4,600 |
162 |
0,288 |
|
Этан, С2Н6 |
30,07 |
305,43 |
4,876 |
212 |
0,285 |
|
Пропан, С3Н8 |
44,09 |
369,82 |
4,246 |
225 |
0,281 |
|
Изобутан, и-С4Н10 |
58,12 |
408,13 |
3,645 |
221 |
0,283 |
|
Н-бутан, н-С4Н10 |
58,12 |
425,16 |
3,794 |
228 |
0,274 |
|
Изопентан, и-С5Н12 |
72,15 |
460,40 |
3,381 |
234 |
0,268 |
|
Н-пентан, н-С5Н12 |
72,15 |
469,65 |
3,366 |
232 |
0,262 |
|
Азот, N2 |
28,01 |
126,26 |
3,400 |
304 |
0,292 |
|
Двуокись углерода, СO2 |
44,01 |
304,20 |
7,370 |
468 |
0,274 |
|
Сероводород, Н2S |
34,08 |
373,60 |
9,000 |
346 |
0,283 |
9. Пары и парообразование
Процесс парообразования. Основные определения
При анализе режимов работы теплосиловых установок практически всегда приходиться иметь дело с разного рода жидкостями и их парами.
Процесс парообразования и методика определения основных характе-
ристик процесса парообразования для всех жидкостей практически анало-
гичны, что дает возможность рассматривать процесс парообразования на примере воды, как одного из наиболее распространенных веществ в природе.
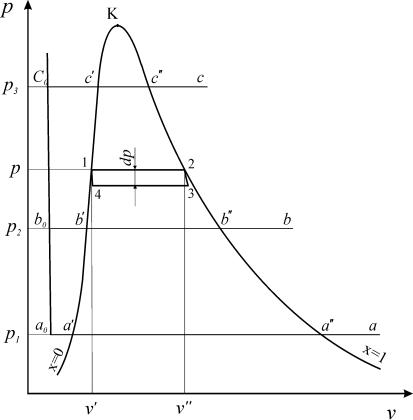
Рассмотрим изобарный процесс парообразования 1 кг воды в координатах р – v (рис. 19).
В исходном состоянии ( а0 ) вода представляет из себя недогретую жид-
кость, имеет температуру ( t0 ), значение которой ниже температуры насы-
щения (ts1 ), а давление воды в этой точке равно р1. В результате изобарного подвода теплоты в процессе ( а0 - а ) вода нагревается до температуры насы-
щения ts1 и в токе ( а ) начинается процесс кипения.
85
Рис. 19. Диаграмма состояний водяного пара в координатах p-v
Процесс кипения протекает на участке а'- а" при постоянном давлении
р1 и постоянной температуре ts1. В точке (а") вода полностью испаряется. Пар в этом состоянии называется сухим насыщенным. На участке (а'-а") вода находится в двух фазах и состоит из смеси кипящей воды и сухого насыщен-
ного пара. Эта двухфазная равновесная система называется влажным насы-
щенным паром. При дальнейшем изобарном подводе теплоты сухой насы-
щенный пар превращается в перегретый (а). Перегретый пар имеет темпера-
туру выше температуры кипения (насыщения) при данном давлении. В со-
стоянии (а) параметры перегретого пара имеют следующие значения: р1, tа > ts1 , va.
Аналогичные процессы изобарного подвода теплоты к воде можно провести при других давлениях р2, р3, и т. д. Соответствующие процессы изображаются линиями b0 -b'-b"-b и с0- с'-с"-с. Точки, характеризующие со-