Материал: Теоретические основы теплотехники 1

76
n G Gi , i 1
(196)
а число киломолей смеси G равно сумме числа киломолей всех компонентов
смеси Gi
n |
|
G G i , |
(197) |
i 1 |
|
где n – число компонентов в смеси.
Одной из важнейших характеристик смеси является ее состав. Он зада-
ется массовыми или молярными концентрациями (долями) компонентов.
Массовой концентрацией или массовой долей mi называется отноше-
ние массы компонента к массе всей смеси
m |
G |
|
G |
|
i |
|
i |
||
|
|
|
||
|
G |
|
n |
|
|
|
|
i |
|
|
|
|
|
G |
|
|
|
i 1 |
|
.
(198)
Молярной концентрацией или молярной долей i-го компонента
ri
называется отношение количества киломолей этого компонента |
G |
i |
||||||
|
|
|
|
|
|
|
|
|
числу киломолей смеси |
|
|
|
|
|
|
|
|
ri |
G |
i |
|
G |
i |
. |
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
||
|
G |
|
n |
|
|
|
|
|
|
|
G i |
|
|
|
|||
|
|
|
|
|
|
|
||
|
|
|
|
i 1 |
|
|
|
|
к общему
(199)
Очевидно, что для термодинамических смесей справедливы следующие соотношения:
n |
n |
|
mi 1 , |
ri 1 . |
(200) |
i 1 |
i 1 |
|

77 |
|
Средняя (кажущаяся) молярная масса смеси m |
равна отношению мас- |
сы смеси к количеству киломолей смеси и может быть определена из следу-
ющих соотношений:
|
|
|
|
|
n |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
G |
|
Gi |
|
|
n |
|
|
G |
i |
|
n |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
m |
|
i |
= |
i 1 |
|
= |
|
|
i |
|
= ri i ; |
|
|
|
||||||||
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
Gi |
|
G |
|
|
i 1 |
|
|
G |
|
|
i 1 |
|
|
|
|
|
|||
|
G |
|
|
G |
|
|
G |
|
|
|
|
|
1 |
|
|
|
1 |
|
|
|||
m |
i |
= |
|
|
= |
|
|
|
|
|
= n |
|
|
|
|
= |
|
|
|
. |
||
G |
i |
n |
|
n |
|
G |
|
|
G |
|
n |
m |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
Gi |
|
|
|
i |
|
|
|
i |
|
|
|
|
i |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
G |
|
|
|
|
|
|
|
|
|
|
|
|
i 1 |
|
|
i 1 |
i |
|
|
i 1 |
i |
|
i 1 |
i |
|
||||||
|
|
|
|
|
|
|
|
|
i |
|
|
|
|
|||||||||
(201)
(202)
Зависимость между массовой и молярной концентрациями устанавли-
вается соотношением
m |
G |
|
i |
||
|
||
i |
G |
|
|
или
= |
|
i |
Gi |
||||
|
|
|
|
|
|
||
|
|
|
G |
||||
|
m |
||||||
|
|
|
|
|
|
||
m |
|
|
|
. |
|||
i |
|
|
|
i |
|||
|
|
|
|
|
|
||
r |
|
|
|
m |
|
||
i |
|
|
|
|
|
||
= ri im
(203)
(204)
Газовая постоянная смеси |
R |
выражению:
|
|
R |
|
n |
|
|
m |
|
= |
|
i |
||
|
||||||
R |
|
|
m |
|||
|
|
|
i 1 |
|
||
|
|
|
|
|
m может быть вычислена по следующему |
|||||||||
|
|
|
|
|
|
|
|
|
|
R |
R |
= |
1 |
|
, |
(205) |
|||
|
|
|
|
|
|
||||
i |
n |
|
n r |
|
|
|
|||
|
|
|
|
|
|||||
|
ri i |
|
|
i |
|
|
|
||
|
|
|
|
|
|
||||
|
i 1 |
|
i 1 Ri |
|
|
|
|||
где R =8314 Дж/(кмоль К) – универсальная газовая постоянная, Ri – характе-
ристическая газовая постоянная компонента смеси.
Для жидких, твердых и газообразных смесей часто используется и по-
нятие объемной концентрации компонентов. Объемной концентрацией i-го компонента vi называется отношение объема данного компонента Vi к объе-
78
му всей смеси V
v |
Vi |
. |
(206) |
|
|||
i |
V |
|
|
|
|
||
Схемы смешения
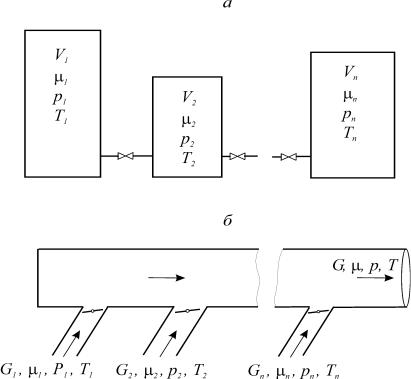
При образовании смесей на практике встречаются две основные схемы смешения: при постоянном объеме (V = idem, рис. 18а) и постоянном давле-
нии (p = idem, рис. 18б).
Рис. 18. Схемы смешения при постоянном объеме (а) и при постоянном давлении (б)
При расчете и анализе схемы смешения при постоянном объеме рас-
сматривается система, включающая ряд резервуаров, соединенных трубопро-
водами с установленными на них кранами (рис. 18а). В каждом резервуаре объемом Vi находится один компонент с известными исходными параметрами (Gi , i , pi , Ti ). После открытия кранов во всех резервуарах происходит выравнивание давления pm, а затем температуры Tm и концентра-
79
ции компонентов (mi, ri) – система переходит в состояние термодинамическо-
го равновесия. Во всех стадиях процесса смешения полный объем системы
сохраняет неизменную величину V =
n Vi i 1
.
В процессе смешения по схеме с постоянным объемом теплота извне не
подводится ( Q |
|
0 ) и внешняя работа не совершается ( |
|
0 |
) и, следова- |
|
L |
||||
|
|
|
тельно, исходя из первого начала термодинамики по внешнему балансу (35),
получаем, что этот процесс смешения идет без изменения внутренней энер-
гии
U1,2 U2 U1 0
(
U
idem
).
(207)
Смесеобразование при постоянном давлении происходит в трубопро-
водах (рис. 18б). К общему трубопроводу отдельными потоками подводятся компоненты. Для каждого компонента известны: массовый расход Gi , мо-
лярная масса i , давление pi и температура Ti . Смесеобразование в трубо-
проводе возможно лишь в случае, когда давление каждого компонента pi
больше среднего давления смеси в трубопроводе pm . При прохождении за-
порного устройства давление компонента уменьшается до среднего давления
смеси |
pm – отсюда наименование схемы ( p idem ). |
|
|
|
Заключительные стадии процесса смешения при |
p idem |
– выравни- |
вание температур, концентраций компонентов в смеси (диффузионные про-
цессы) и переход системы в состояние термодинамического равновесия.
В процессе смешения при |
p idem |
теплота извне не подводится |
( Q 0 ) и внешняя работа не совершается ( W 0 ) и, следовательно, ис-
ходя из первого начала термодинамики по внешнему балансу для потока (81),
получаем, что этот процесс смешения идет без изменения энтальпии
H1,2 H2 H1 0 ( H idem). (208)

80
Смеси идеальных газов
Смеси идеальных газов являются также идеальными газами и подчи-
няются уравнению состояния идеальных газов (уравнению Клапейрона)
pmV G Rm Tm G R Tm , |
(209) |
где pm , Tm – давление и температура смеси.
Средняя температура и среднее давление смеси характеризуют конеч-
ное состояние диффузионного равновесия смеси.
Состояние компонентов смеси в процессе перемешивания непрерывно изменяется, начиная с момента первичного выравнивания давлений компо-
нентов и кончая состоянием диффузионного равновесия, когда давление каждого из компонентов снижается до уровня стабильного парциального давления p i .
Закон диффузионного равновесия смеси идеальных газов (закон Даль-
тона) характеризует установившееся состояние газовой смеси и формулиру-
ется следующим образом: каждый компонент смеси ведет себя в газовой смеси так, как будто он один при температуре смеси Tm равномерно распро-
странен во всем объеме смеси V и развивает при этом давление, которое называется парциальным p i .
Уравнения состояния для i-го компонента и всей смеси идеальных га-
зов могут быть представлены в следующем виде:
p iV
pmV
= |
G |
|
|
G |
|
i RT RTm
;
.
(210)
(211)
При делении уравнения (210) на уравнение (211) получаем