Материал: Структура и методы синтеза полимеров
+Fe2+→RO*+НО-+Fe3+;
2Fe3++2НO-+НО-СН2-SO2Na→2Fe2++HO-CH2-SO3Na+H2O.
Неорганическая система персульфат-тиосульфат действует по схеме:
O8-2-+ S2O3-2-→ SO4-2-+ S*O4-+
S*2O3-; S*O4-+Н2О
→ НSO4-+О*Н.
Образующиеся свободные радикалы инициируют полимеризацию мономеров.
На стадии обрыва цепи образуются нейтральные макромолекулы при рекомбинации (столкновении) макрорадикалов или в результате их диспропорционирования до двух нейтральных макромолекул:
(-CH2-CHX-)n-CH2-XHC*+R-(-CH2-CHX-)m-CH2XHC*→
→R-(-CH2-СНХ-)n-CH2-CHX-CHX-CH2-(-CHX-CH2-)m-R (рекомбинация),(-CH2-CHX-)n-CH2-XHC* + XHC*-CH2-(-CHX-CH2-)m-R→
→R-(-CH2-CHX-)n-CH2-CH2X+XHC=CH-(-CHX-CH2-)m-R
(диспропорционирование).
Вид реакции обрыва цепи зависит от строения
молекул мономера. Если мономер содержит электроноотрицательный или громоздкий
заместитель (метилметакрилат), то цепь обрывается путем диспропорционирования:
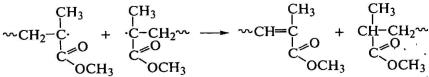 .
.
При полимеризации стирола преобладает
рекомбинация макрорадикалов:
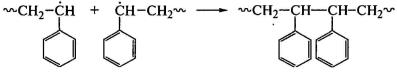
По мере роста цепи увеличивается вязкость
системы, уменьшаются подвижность макрорадикалов и скорость их рекомбинации,
растут время их жизни и концентрация, что приводит к ускорению полимеризации на
поздних стадиях (гель-эффект) и ухудшению механических свойств полимера. Для
регулирования ММ полимера используют реакцию передачи цепи путем введения в
систему регулятора, например меркаптана (RSH),
или растворителя, особенно галогенсодержащего, например тетрахлорида углерода:
~CH2-HXC*+RSH→~CH2-CH2X+RS* (обрыв материальной цепи),
RS*+CH2=СHX→RSCH2-HXC* (начало новой материальной цепи); или
~CH2-HXC*+CCl4→~CH2-HXCCl+C*Cl3 (обрыв материальной цепи),
CH2=СHX+C*Cl3→Cl3C-СН2-HXC*
(начало новой материальной цепи),
или повышения концентрации инициатора до его
индуцированного распада:
~CH2-HXC*+ROOR →
~CH2-CHX-OR+RO*;*+CH2=СHX
→ RО-CH2-HXC* и
т.д.
В отличие от реакции обрыва цепи, они обрывают только материальную цепь - перестает расти число звеньев в макромолекуле. При этом они сами становятся свободным радикалом и продолжают кинетическую цепь, которая измеряется числом элементарных актов присоединения молекул мономера к активному центру в расчете на один свободный радикал, образовавшийся при инициировании реакции полимеризации. С повышением температуры и количества регулятора вследствие ускорения реакций передачи цепи и подавления реакций роста цепи образуются низкомолекулярные вещества (реакция теломеризации), которые можно выделить и использовать для получения новых полимеров.
Кинетика цепной полимеризации по конверсии (степени превращения) мономера характеризуется S-образной кривой с пятью участками (рис.7):
· участок ингибирования, когда концентрация свободных радикалов мала, и они не могут начать цепной процесс полимеризации (1);
· участок ускорения полимеризации, где начинается основная реакция превращения мономера в полимер, при этом скорость реакции растет (2);
· участок стационарного состояния (прямолинейный участок), где расходуется основное количество мономера с постоянной скоростью (3);
· участок замедления полимеризации в связи с резким уменьшением концентрации мономера (4);
· прекращение основной реакции в связи
исчерпанием всего мономера (5).
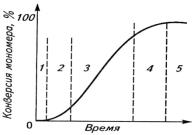
Рис.7. Типичная кинетическая кривая цепной
радикальной реакции
Скорость реакции инициирования пропорциональна концентрации введенного инициатора [I]: vи=kи[I], где kи - константа скорости реакции инициирования. Скорость реакции роста цепи пропорциональна произведению концентраций растущих макрорадикалов [М*] и молекул свободного мономера [М]: vр=kр[М*][М], где kр-константа скорости реакции роста цепи. Скорость реакции обрыва цепи пропорциональна квадрату концентрации соударяющихся макрорадикалов: vобр=kобр[М*]2. Скорость полимеризации является алгебраической суммой скоростей трех ее стадий: vобщ=vи+vр-vобр.
Для кинетического анализа интересен стационарный
период реакции, когда полимеризация идет с постоянной скоростью, и число вновь
образующихся свободных радикалов равно количеству исчезающих макрорадикалов при
обрыве цепей (vи=vобр):
kи[I]=kобр[М*]2.
Отсюда следует, что скорость конверсии мономера пропорциональна квадратному
корню из концентрации инициатора. Степень полимеризации пропорциональна
скорости роста цепи и обратно пропорциональна скорости обрыва цепи, так как
макромолекула образуется при столкновении двух макрорадикалов. Иными словами,
степень полимеризации и средняя молекулярная масса полимера обратно
пропорциональны квадратному корню из концентрации инициатора:
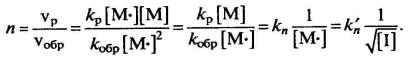
Таким образом, параметры процесса и размер макромолекул для стационарного периода можно выразить через концентрацию химического инициатора.
При повышении температуры на 10оС возрастает в 2-3 раза скорость полимеризации, а со снижением температуры растут регулярность чередования звеньев и величина ММ, уменьшаются доля низкомолекулярных фракций, разветвленность макромолекул и побочные реакции. Для повышения скорости полимеризации при низких температурах вводят промоторы, активирующие распад молекул инициатора. Кинетические закономерности процесса полимеризации поддаются регулированию за счет изменения:
· времени до начала полимеризации (длины индукционного периода) путем введения ингибиторов, реагирующих с начальными радикалами;
· наклона прямолинейного участка
кинетической кривой к оси абсцисс путем введения замедлителей полимеризации
(бензохинон, нитробензол), которые снижают концентрацию радикалов и уменьшают
время их жизни, что приводит к уменьшению длины полимерной цепи. Ингибитор не
влияет на скорость полимеризации, но удлиняет индукционный период. В
зависимости от природы мономера одно и то же вещество может быть и ингибитором,
и замедлителем, и регулятором полимеризации. Бензохинон действует по схеме:
![]() ,
,
![]() .
.
В радикальной полимеризации способно участвовать
большинство выпускаемых промышленностью мономеров этиленового и диенового ряда.
Активность мономеров этиленового ряда зависит от химической природы
заместителей при двойной связи и определяется активностью свободного радикала,
образующегося при разрыве π-связи.
Активность радикала зависит от электроноакцепторных свойств замещающей группы и
растет с увеличением ее способности к делокализации электронного облака.
Наилучшим акцептором электронов является бензольное кольцо стирола, а больше
донорами электронов - алкоксигруппы винилалкиловых эфиров. Радикалы же этих
мономеров дают обратную (антибатную) последовательность активностей: время
жизни радикала тем меньше, чем он активнее и чем меньше эффект сопряжения его
неспаренного электрона с электронной структурой заместителя в молекуле
мономера. Поэтому в порядке убывания активности виниловые мономеры располагаются
в следующий ряд:
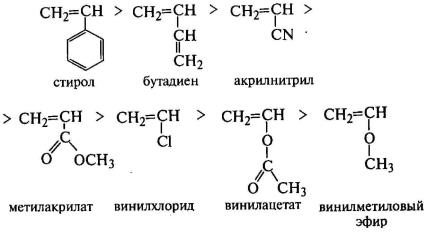
Активность радикалов может быть количественно определена и растет с увеличением соотношения констант kобр/kр. Например, активности радикалов винилацетата, метилметакрилата и стирола в реакции роста цепи соотносятся количественно как 20:2:1. На активность радикалов влияют также условия полимеризации, а на активность мономеров - количество заместителей. Наличие двух бензольных колец при одном атоме углерода в молекуле мономера полностью подавляет его способность к полимеризации из-за сильной стабилизации неспаренного электрона.
Одна из особенностей свободнорадикальной полимеризации состоит в том, что по длине одной макромолекулы могут существовать различные типы соединения звеньев мономеров - «голова к хвосту» (а), «голова к голове» (б), так как радикал может атаковать молекулу мономера с любого ее конца:
а) ~CH2-НC-CH2-HC~ б) ~НC-CH2-CH2-HC-НC-CH2~.
ï ï ï ï ï
R
R R
R R
Нет и порядка в пространственном расположении заместителей у мономерных звеньев из-за отсутствия координирующего действия при присоединении каждой следующей молекулы мономера. Для полимеров винилового ряда характерно чередование звеньев в положении «голова к хвосту», что обеспечивает высокий уровень свойств полимеров, несмотря на отсутствие пространственной регулярности их макромолекул. Поэтому методом свободнорадикальной полимеризации производят основную массу промышленных полимеров этого типа - полистирол, полиакрилонитрил, полиметилметакрилат, поливинилхлорид, поливинилацетат.
По сравнению с мономерами винилового ряда
диеновые мономеры дают наибольшее разнообразие структур макромолекул, так как
каждая молекула содержит две двойные связи. Существуют пять основных типов
соединения звеньев в макромолекуле - в положениях 1,4; 1,1; 4,4; 1,2 и 3,4. В
двух последних случаях их можно рассматривать как полимеры винилового ряда:
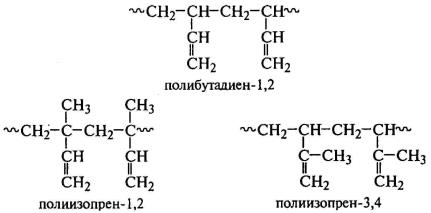
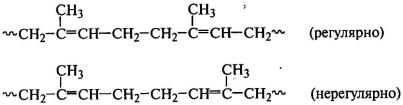
Для несимметричных диенов (изопрен, хлоропрен)
при соединении их звеньев в положениях 1,1 и 4,4 может нарушаться регулярность
их чередования:
 .
.
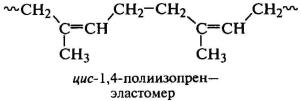
Как отмечалось выше, 1,4-полидиены могут
различаться пространственным расположением СН2-групп в цепях относительно
плоскости двойной связи:
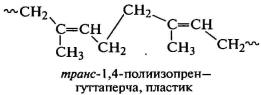 .
.
По длине цепи могут существовать все виды
структур полидиенов, что приводит к нестабильности и невоспроизводимости их
свойств. Структуры-1,4 формируются преимущественно в транс-положении, особенно
при полимеризации активного и поляризованного хлоропрена, поэтому полихлоропрен
производится в промышленном масштабе методом свободнорадикальной полимеризации.
Полибутадиен и полиизопрен наиболее ценны в основном как цис-1,4-изомеры,
поэтому в промышленности все чаще их получают методами ионно-координационной
полимеризации.
4. Ионная полимеризация
Ионная полимеризация сопровождается координацией мономера на поверхности катализатора и отличается от радикальной реакции тем, что:
· растущие частицы (ионы) более активны, чем свободные радикалы;
· инициаторы каталитические (восстанавливают структуру, а не расходуются необратимо) и позволяют получать стереорегулярные полимеры;
· суммарная энергия активации меньше по сравнению с радикальной, и это позволяет снизить температуру реакции вплоть до отрицательных температур;
· среда - не вода, а растворитель с сольватирующим действием на ионы;
· большие значения ММ и узкое ММР полимера, высокая степень химической регулярности макромолекул при полном отсутствии разветвлений.
Она уступает радикальной полимеризации по сложности технологического оформления процесса и по масштабам применения при производстве большинства промышленных полимеров.
Катализаторами катионной полимеризации являются
доноры протона - сильные протонные кислоты (H2SO4)
и кислоты Льюиса (AlCl3,
BF3, TiCl4).
Последние образуют с сокатализатором (Н2О, HCl)
комплексные соединения, которые на стадии инициирования создают с мономером
ионную пару:
СН2=С(СН3)2+Н+[ВF3.ОН]-→
(СН3)3С+[ВF3.ОН]-.
Низкая энергия активации (до 65 кДж/моль) обеспечивает высокую скорость процесса, увеличивающуюся со снижением температуры (температурный коэффициент отрицателен). Например, под действием BF3 изобутилен полимеризуется за несколько секунд при -100оС до полимера большой ММ. В процессе роста цепи ионная пара реагирует со следующей молекулой мономера, а на конце цепи сохраняется карбкатион с противоанионом:
(СН3)3С+[ВF3.ОН]-+СН2=С(СН3)2→(СН3)3СН2(СН3)2С+[ВF3.ОН]-
и т. д.
Поляризация молекулы мономера обеспечивает
регулярное присоединение звеньев («голова к хвосту»), а обрыв цепи невозможен
рекомбинацией одноименно заряженных ионов. Поэтому ионная пара при уменьшении
кинетической подвижности макроиона (с ростом его размеров) перестраивается в
макромолекулу с двойной связью или образует гидроксильную группу и регенерирует
комплекс катализатор-сокатализатор или катализатор:
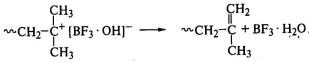 ;
;
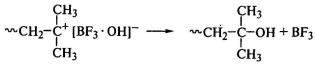 .
.
Катализатор многократно инициирует рост цепи, поэтому при синтезе эффективны даже малые его количества. Энергия активации реакции обрыва цепи через разрыв σ-связи больше, а энергия активации реакции роста цепи, которая определяет весь процесс синтеза и связана с атакой двойной связи мономера ионом карбония, - меньше, чем при свободнорадикальной полимеризации. Поэтому повышение температуры и ведет к снижению скорости реакции синтеза и средней молекулярной массы полимера.
Катализаторами анионной полимеризации являются
щелочные металлы, их амиды, алкилы или комплексы с ароматическими
углеводородами. Полимеризацию с амидом щелочного металла проводят в среде
жидкого аммиака, выполняющего роль растворителя и передатчика реакционной цепи:
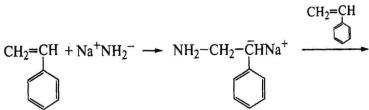
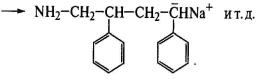
Обрыв цепи происходит путем ее передачи на
растворитель:
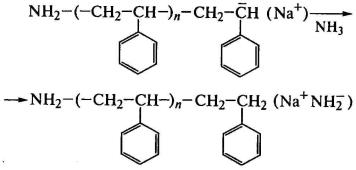
Регенерированный катализатор начинает новую
цепь, и реакция идет до конца при регулярном присоединении мономера «голова к
хвосту». Полимеризация мономеров щелочным металлом проходит через образование
ион-радикала и затем бианиона, по обоим концам которого и присоединяются
последующие молекулы до образования макромолекулы:
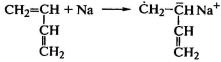 ;
;
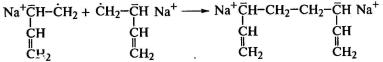 ;
;
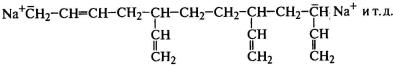 .
.
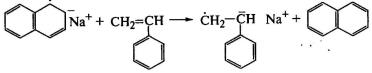
Регулирование молекулярной массы полимера
улучшается каталитическим комплексом щелочного металла с нафталином в среде
полярного растворителя тетрагидрофурана (полимеризация с переносом электрона).
Образующийся комплекс передает свой электрон мономеру, а нафталин
регенерируется:
![]() ;
;
 .
.
В присутствии металлического натрия вновь образуется комплекс, повторяются акты инициирования и роста цепи. При отсутствии примесей обеспечивается рост цепи без обрыва до полного исчерпания мономера с образованием «живых» полимеров, состоящих из заряженных отрицательно макроионов. При добавлении того же мономера продолжается рост цепи, а порции другого мономера - образуется блок-сополимер.
Алкилы щелочного металла отличаются от других
систем высокой способностью координировать молекулу мономера, поэтому
полимеризацию изопрена с н-бутиллитием называют анионно-координационной:
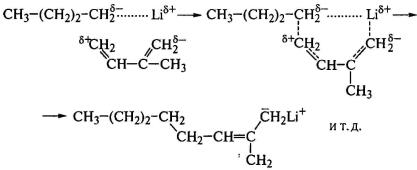
Молекула изопрена внедряется в поле двух центров катализатора - между отрицательно заряженным алкильным остатком и положительно заряженным ионом лития (двухцентровый механизм), принимая цис-конфигурацию, которая и сохраняется при последующих актах роста цепи. Так получают синтетический аналог НК, а процесс такого синтеза в среде неполярных или малополярных растворителей, когда полярность растворителя меньше полярности мономера, является оптимальным. Так же получают полимеры с концевыми функциональными группами - карбоксильными (+СО2) или гидроксильными (+оксид этилена) и звездообразной структуры (в CCl4).