Материал: Сравнительная оценка методов качественного и количественного анализа субстанции сульфацил-натрия
Сравнительная оценка методов качественного и количественного анализа субстанции сульфацил-натрия
Курсовая работа
Тема
курсовой работы «Сравнительная оценка методов качественного и количественного
анализа субстанции сульфацил-натрия»
Содержание
Введение
I.Теоретическая часть
.Фармакопейная статья
. Описание и синтез
. Испытания на подлинность
. Количественное определение
. Хранение и применение
II.Экспериментальная часть
.Испытания на подлинность
. Количественное определение
Заключение
Список литературы
Введение
Сульфацетамид натрия - один из представителей группы сульфаниламидов, группа антимикробных лекарственных средств - производных сульфаниловой кислоты. Их антибактериальные свойства обнаружены немецким учёным Г. Домагком в 1934. В 1935 году ученые Пастеровского института (Франция) установили, что антибактериальным действием обладает именно сульфаниламидная часть молекулы пронтозила(красный стрептоцид), а не структура, придающая ему окраску.
Сульфаниламидные препараты близки по химической структуре парааминобензойной кислоте (ПАБК) - необходимому фактору роста микроорганизмов, при отсутствии которого они не могут размножаться. Основной механизм действия сульфаниламидных препаратов - конкуренция с ПАБК за связывание с определёнными ферментами в микробной клетке. В результате соединения сульфаниламидных препаратов с ферментами бактерии теряют способность синтезировать необходимый им витамин - фолиевую кислоту и осуществлять другие превращения веществ, которые в норме протекают с участием ПАБК. Поскольку эти ферменты обладают более высоким сродством с ПАБК, чем с сульфаниламидными препаратами терапевтический эффект достигается при достаточно больших дозах препаратов. Приём сульфаниламидных препаратов в недостаточных дозах или досрочное прекращение лечения могут привести к появлению устойчивых штаммов возбудителей, не поддающихся в дальнейшем действию сульфаниламидных препаратов.
Цель: провести сравнительную оценку реакций идентификации и методов количественного определения субстанции сульфацил-натрия.
Задачи:
провести обзор литературы, содержащей методики качественного и количественного анализа субстанции;
провести качественное определение субстанции сульфацил - натрия;
провести количественное определение субстанции сульфацил - натрия;
провести статистическую обработку методов количественного определения субстанции сульфацил - натрия;
сделать заключение о возможности использования методов качественного и количественного анализа сульфацил-натрия в фармацевтическом анализе;
. Теоретическая часть
. Фармакопейная статья
ГФ X ФС № 641natrium
Сульфацил-натрий
Сульфацил растворимый (Sulfacylum solubile)
п-Аминобензолсульфонилацетамид-натрий (Albucid-natrium
Sulfacetamidum
Natricum *)
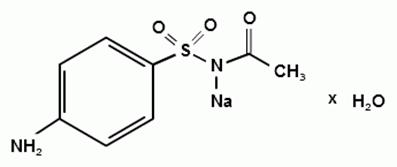
H9N2Na2O3S • H2O. в. 254,24
Описание. Белый кристаллический порошок без запаха.
Растворимость. Легко растворим в воде, практически нерастворим в спирте, эфире, хлороформе и ацетоне.
Подлинность. Препарат дает характерную реакцию на ароматические первичные амины и реакцию Б на натрий.
,1 г препарата растворяют в 3 мл воды и прибавляют 1 мл раствора сульфата меди; образуется осадок голубовато-зеленоватого цвета, который не изменяется при стоянии (отличие от других сульфамидных препаратов).
Прозрачность и цветность раствора. Раствор 1,5 г препарата в 5 мл воды должен быть прозрачным; окраска раствора не должна быть интенсивнее эталона № 5а.
Щелочность. рН 8,5-9,5 (5% водный раствор).
Хлориды. Раствор 0,2 г препарата в 10 мл воды должен выдерживать испытание на хлориды (не более 0,01% в препарате).
Сульфаты. Раствор 0,5 г препарата в 10 мл воды должен выдерживать испытание на сульфаты (не более 0,02% в препарате).
Тяжелые металлы. 1 г препарата растворяют в 17,5 мл воды, добавляют 2,5 мл разведенной уксусной кислоты, взбалтывают в течение 5 минут и выпавший осадок отфильтровывают. 10 мл фильтрата должны выдерживать испытание на тяжелые металлы (не более 0,001% в препарате).
Количественное определение. Около 0,3 г препарата (точная навеска) растворяют в 10 мл воды и 10 мл разведенной соляной кислоты и далее поступают, как указано в статье «Нитритометрия» (стр. 799). В случае применения внутренних индикаторов используют нейтральный красный.
мл 0,1 мол раствора нитрита натрия соответствует 0,02542 г C8H9N2Na2O3S • H2O, которого в препарате должно быть не менее 99,0%.
Хранение. Список Б. В таре, предохраняющей от действия влаги и света.
Высшая разовая доза внутрь 2,0 г.
Высшая суточная доза внутрь 7,0 г.(При лечении
инфекционных глазных заболеваний применяют 10- 20-30% растворы и
мази).Антибактериальное средство.
.Описание и синтез
Сульфацил-натрий - это амфотерное соединение. Наличие амидной группы в структуре сульфацила натрия будет обусловливает его кислотные свойства, которые выражены сильнее основных. Этим объясняется относительная устойчивость и возможность применения как самостоятельного лекарственного средства. Основные свойства обусловлены наличием ароматической аминогруппы. Сульфацил натрия хорошо растворим в воде, водные растворы имеют щелочную реакцию среды вследствие гидролиза ( соль сильного основания и слабой органической кислоты ).
В натриевых солях сульфаниламидов щелочность регламентируется как примесь, остающаяся после их синтеза, а также образующаяся при хранении растворов вследствии гидролиза. Как правило, щелочность в этих лекарственных средствах допускается в определенных пределах. В сульфациле натрия она устанавливается по pH раствора. Наличие амидной группы в структуре будет обусловливать его кислотные свойства.
Синтез сульфацетамида натрия осуществляют из
ацилированного сульфаниламида по следующей схеме:
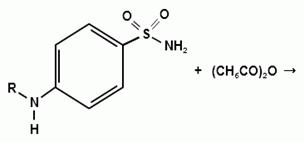
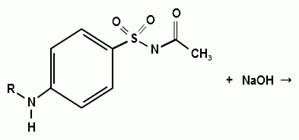
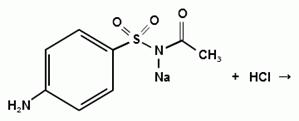
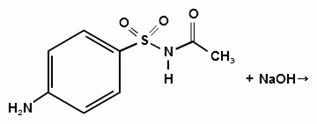
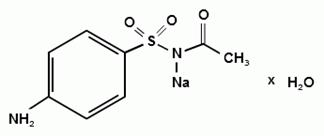
. Испытания на подлинность
Для испытаний подлинности сульфацила - натрия используют общие и частные реакции, обусловленные наличием тех или иных функциональных групп в молекуле.
На первичную ароматическую аминогруппу, проводят реакцию образования азокрасителя, лигниновую пробу, реакцию конденсации:
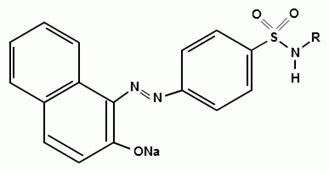
) Реакция образования азокрасителя
Общим свойством первичных ароматических аминов является способность к образованию соли диазония и азокрасителей. Ионы диазония, обладающие электрофильными свойствами, вступают в реакцию электрофильного замещения.
Реакция основана на образовании хлорида диазония
в результате действия раствором нитрита натрия и разведенной хлороводородной
кислотой. Последующее сочетание хлорида диазония в щелочной среде с фенолами
приводит к образованию азокрасителя. Известно очень большое число
азосоставляющих. ГФ рекомендует для выполнения этой реакции щелочной раствор
в-нафтола. В результате реакции появляется вишнево-красное окрашивание или
образуется осадок оранжево-красного цвета.
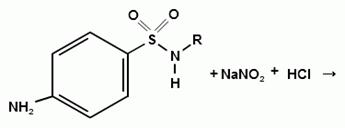
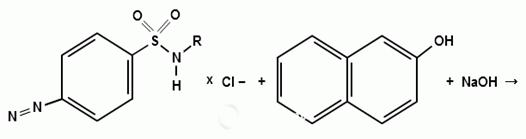
) Лигниновая проба
Эта своеобразная разновидность реакции
образования шиффовых оснований. Она выполняется на древесине или газетной
бумаге, при нанесении на которую сульфацил-натрия и капли разведенной соляной
кислоты появляется оранжево - желтое окрашивание. Сущность происходящего
химического процесса в том, что образуется ароматический альдегид. Альдегиды
взаимодействуют с первичными ароматическими аминами, образуя шиффовые
основания:
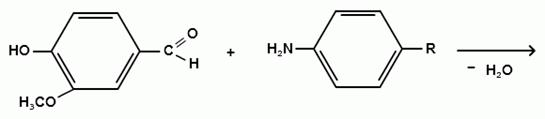
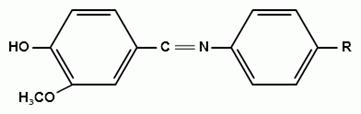
) Реакция конденсации
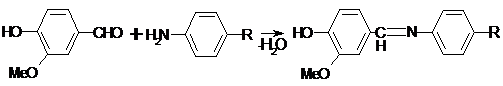
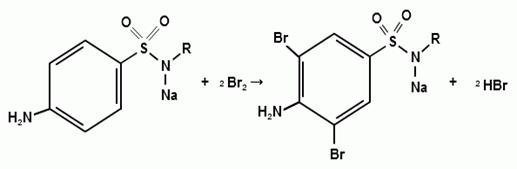
4) Реакция галогенирования ( на ароматический цикл)
Эта реакция основаны на наличии донорной группы
в ароматическом ядре молекулы сульфаниламида (заместитель первого рода).
Реакции галогенирования могут быть использованы как для качественного анализа
(образование осадков дибром- или дийодпроизводных), так и для количественного
(броматометрического, йодометрического, йодхлорометрического) определения
сульфаниламидов.
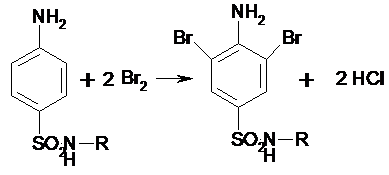
Сульфацил натрий обладает кислотными свойствами, соответственно взаимодействует с металлами:
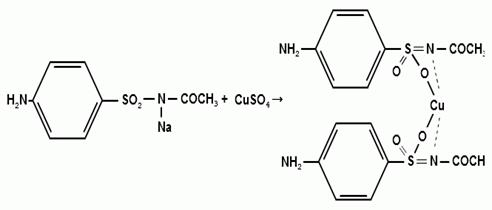
) Реакция образования комплексных солей
Образование окрашенных, нерастворимых в воде
комплексных солей сульфаниламидов является общей реакций, характеризующей их
кислотные свойства, и в то же время позволяющей различить судьфаниламиды внутри
группы, поскольку осадки отличаются характером и устойчивостью окраски. Окраска
и устойчивость комплексных соединений зависят от химической структуры вещества,
в частности от силы кислотности. В ГФ XI
рекомендуется проводить реакцию образования комплексных солей с меди сульфатом.
Реакция среды должна быть нейтральной во избежание образования осадка меди (II)
гидроксида. Сульфацил-натрия образует комплекс голубовато - зеленого цвета.
) Реакция окисления
При окислении сульфаниламидов как ароматических аминов образуются окрашенные соединения. Окисление может происходить под действием кислорода воздуха, особенно в растворах. Так быстрое пожелтение раствора сульфацила-натрия свидетельствует о появлении окрашенных продуктов окисления. Степень окисления сульфаниламидов регламентируется ГФ XI путем определения цветности раствора. Так, при анализе сульфацил - натрия проводится определение степени окраски его раствора определенной концентрации, которая не должна превышать окраску эталона цветности № 6б.
) Реакция обнаружения серы (в сульфамидной группе)
Наличие серы в молекуле сульфаниламидов, как и в других содержащих серу соединениях, можно установить после окисления органической части молекулы концентрированной азотной кислотой или сплавления: с 10-кратным количеством нитрата калия до сульфат-иона. Последний затем обнаруживают с помощью раствора хлорида бария - белый осадок
+ + SO42- → BaSO4↓
) Реакция и нитропруссидом натрия.
Растворы сульфаниламидов в присутствии едких щелочей при добавлении 1% раствора нитропруссида натрия (Na2[Fe(CN)5NO]) и последующем подкислении минеральной кислотой образуют окрашенные в красный или красно-коричневый цвет раствор или осадок.
) УФ-, ИК- спектрофотоместрия
В ФС включены способы идентификации сульфаниламидов по УФ-спектрам поглощения. Выбор этих методик основан на проведении предварительных исследований. В.Е. Чичиро, А.П. Арзамасцевым с сотрудниками унифицированы условия получения УФ-спектров 14 сульфаниламидов для их идентификации. Растворителями служили 0,1 М растворы гидроксида натрия и хлороводородной кислоты. УФ-спектры были сняты в области 210-360 нм. Установлено, что идентифицировать тот или иной сульфаниламид можно по форме УФ-спектра, удельному показателю поглощения или на основании вторых производных УФ-спектров.
УФ-спектр 0,001%-ного раствора сульфацетамида натрия имеет максимум поглощения при 256 нм и минимум - при 227 нм.
Частная реакция определения сульфацил - натрия.
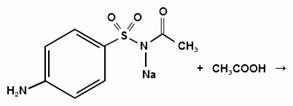
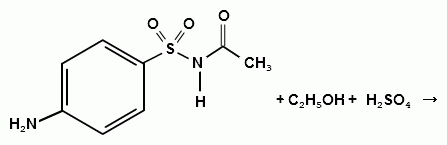
При действии на сульфацил-натрий уксусной
кислотой выделяется бурый осадок сульфацетамида, который после высушивания
должен иметь температуру плавления около 183° С:
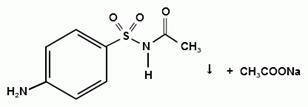
При растворении осадка в этаноле и добавлении
конц. серной кислоты образуется этилацетат, имеющий характерный запах:
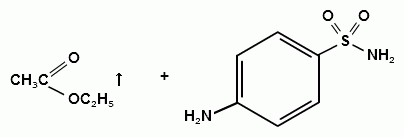
Для отличия натриевых солей от соответствующих сульфаниламидов выполняют реакцию на ион натрия (окраска пламени горелки в желтый цфет), а также реакцию с цинкуранилацетатом - желтое окрашивание.
Na+ + Zn(UO2)3(CH3COO)8 + CH3COO- +
9H2O → NaZn(UO2)3(CH3COO)9 9H2O↓
4.Количественное определение
сульфацил натрий соль реакция
1)Нитритометрия.
Этот метод рекомендован НД для количественного определения сульфаниламидов, являющихся первичными ароматическими аминами. Определение основано на способности первичных ароматических аминов образовывать в кислой среде диазосоединения:
В качестве титранта используют нитрит натрия
(0,1 М раствор). Титруют в присутствии бромида-калия при 18-200С или при
0-100С. Бромид калия катализирует процесс диазотирования, а охлаждение
реакционной смеси позволяет избежать потерь азотистой кислоты и предотвратить
разложение соли диазония. Точку эквивалентности можно установить одним из трех
способов: с помощью внутренних индикаторов (тропеолин 00, нейтральный красный,
смесь тропеолина 00 с метиленовым синим); внешних индикаторов (йодкрахмальная
бумага) или потенциометрически.
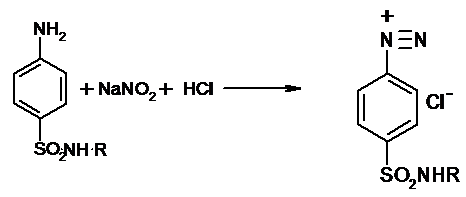
)Нейтрализация.
Поскольку образующаяся натриевая соль легко подвергается гидролизу, то результаты определения получаются заниженные. Поэтому чрезвычайно важен выбор оптимального растворителя, который следует осуществлять с учетом констант диссоциации сульфаниламидов. Сульфаниламиды с константой диссоциации 10-7-10-8 можно титровать в водно-ацетоновом растворе или в этаноле (индикатор тимолфталеин), а с константой диссоциации 10-9 титруют только в неводных растворителях.
Натриевые соли сульфаниламидов можно титровать
кислотой в спирто-ацетоновой среде (индикатор метиловый оранжевый):
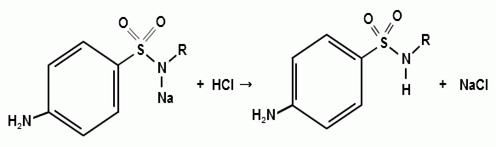
)Броматометрия
Метод основан на реакции галогенирования сульфаниламидов. Титруют раствором бромата калия в кислой среде в присутствии бромида калия. Конечную точку устанавливают при прямом титровании по обесцвечиванию (бромом) индикатора метилового оранжевого, а при обратном титровании -йодометрически:
![]()
![]()
![]()
) Метод Кьельдаля
Используют для количественного определения азота в органических веществах. Определение проводят с помощью прибора, состоящего из колбы Кьельдаля, парообразователя, холодильника, приемника.