Материал: Современное состояние и перспективы использования двойных лекарств в качестве лекарственных средств
Современное состояние и перспективы использования двойных лекарств в качестве лекарственных средств
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РЕСПУБЛИКИ БЕЛАРУСЬ
Учреждение образования
БЕЛОРУССКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ
Фармацевтический факультет
Кафедра фармацевтической технологии и
химии
Современное состояние и перспективы
использования двойных лекарств в качестве лекарственных средств
Липская Маргарита Анатольевна
Минск, 2014
Оглавление
Перечень условных обозначений и сокращений
Введение
. Идентичные и неидентичные двойные лекарства
. Гомодимеры и симметричные лиганды
.1 Симметрия в природе
.2 Гомодимеры как лиганды рецепторов
.3 Гомодимеры как ингибиторы ферментов
.4 Гомодимеры как лиганды ДНК
.5 Гомодимеры фармакологического интереса
. Гетеродимеры и лиганды двойного действия
.1 Гибридные молекулы как лиганды двух различных рецепторов
.2 Гибридные молекулы как ингибиторы ферментов
.3 Гибридные молекулы, действующие на один рецептор и фермент
.4 Другие примеры лекарств двойного действия
. Способ закрепления идентичных и неидентичных двойных лекарств к ассиметричному центру связывания
.1 Идентичные и неидентичные двойные лекарства, взаимодействующие с двумя смежными центрами связывания, расположенными на одной макромолекуле
.1.1 Ингибиторы ацетилхолинэстеразы
.1.2 Бисубстратные ингибиторы
.2 Идентичные двойные лекарства, взаимодействующие с двумя подобными сайтами связывания, расположенными на различных мономерах одной макромолекулы
.2.1 Ингибиторы сиртуина
.2.2 Ингибиторы глутатион S-трансферазы
.2.3 Лиганды рецепторов, связанных с G-белком
.3 Идентичные и неидентичные двойные лекарства, взаимодействующие с двумя различными сайтами связывания, расположенными на различных макромолекулах
.3.1 Лиганды GPCR (гетеродимер)
Заключение
Список использованных источников
Перечень условных обозначений и сокращений
CОХ - циклооксигеназа- рецепторы, сопряженные с G-белком
GST - глутатион-S-трансфераза
LO - липоксигеназа
PAF - фактор активации тромбоцитов- рецепторы, активируемые пероксисомными пролифератами
PR - обратная транскриптаза
SAR - анализ зависимости структура - активность
АПФ - ангиотензин превращающий фермент
АХЭ - ацетилхолинэстераза
ЛС - лекарственное средство
НЭП - нейтральная эндопептидаза
Введение
В стратегии дизайна препаратов прошлых 20 лет ведущим было традиционное понятие: одна болезнь - одна мишень - один подход. Благодаря достижениям биоорганической и бионеорганической химии, молекулярной биологии (особенно благодаря установлению структур некоторых рецепторов и ферментов методом рентгеноструктурного анализа), была идентифицирована структура биологических мишеней, ответственных за болезнь, что привело к дизайну мощных и селективных лигандов или ингибиторов. Но в большинстве случаев, в основе болезни лежат многократные и сложные системы, где больше чем одна биологическая мишень, которые должны быть смодулированы. Некоторые исследования показали, что одновременное и умеренное блокирование или активация нескольких мишеней - более действенное, чем использование селективных и мощных препаратов. Поэтому, создание молекул, действующих на многочисленные биологические мишени, и способных их модулировать, стало инновационным подходом в дизайне ЛС.
Совсем недавно в литературе появилось множество терминов таких как “двойной, димерный, дуальный, гибрид, смешанный или многократный” соединенных с терминами “лиганды, ингибиторы, активаторы, модуляторы или антагонисты”. Лекарства, содержащие две фармакофорные группы, объединенные ковалентно в одну молекулу, названы двойными лекарствами.
Двойные лекарства могут быть идентичными (представляют собой комбинацию двух одинаковых составляющих) и неидентичными (имеющими в качестве составляющих различные структуры). В частности, возможно конструирование сложных «бинарных» структур, содержащих в своем составе несколько функционально значимых частей молекулы. При конструировании двойных лекарств возможны самые различные комбинации, значительно улучшающие активность и фармакокинетические свойства ЛС. Например, если известен фермент, разрушающий ЛС в организме, то возможно конструирование бинарной молекулы, содержащей в своей структуре как фрагмент этого ЛС, так и фрагмент ингибитора данного фермента. При расщеплении данной молекулы в организме ингибирование фермента приведет к пролонгированию действия данного ЛС.
Целью данной курсовой работы является изучение подхода создания двойных
лекарств, преимуществ данного типа модификации в улучшении активности и
фармакокинетических свойств ЛС, оценка современного состояния, а также
перспектив дальнейшего использования двойных лекарств в качестве ЛС.
1. Идентичные и неидентичные двойные лекарства
Соединение двух одинаковых фармакологических объектов приведет к
образованию “идентичного двойного лекарства”, которое является эквивалентом
производного гомодимера. Соединение, где объединены в одну молекулу два
различных фармакологических объекта, называют “неидентичным двойным лекарством”
или гетеродимером. Первая стратегия конструирования - процесс
дублирования/димеризации активного или главного компонента. Цель этого подхода
- производство более мощного и/или более селективного препарата по сравнению с
единичным объектом. Вторая стратегия состоит из соединения двух различных
фармакофоров. В этом случае новое соединение будет обладать всеми
фармокологическими действиями (схема 1.1). Этот подход обладает большим
преимуществом, когда два целевых фермента или рецептора включены в одну болезнь
или расстройство. Лекарство гетеродимер окажет влияние, действуя одновременно
на две биологические мишени [1].
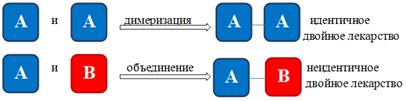
Схема 1.1 - идентичные и неидентичные двойные лекарства
Соединение идентичных или неидентичных фармакофоров можно
классифицировать по способам связи, используемым между двумя объектами.
Объединение может быть достигнуто посредством соединения или другим способом
(простая связь) или способом наложения. Группа связей может быть полимерной
цепью (обычно метиленовая цепь), ароматическим или гетероароматическим кольцом,
а в некоторых случаях неароматическим циклом. Фармакофоры могут быть перекрыты,
когда имеется общая структурная цепь (кольцо или химическая группа),
идентифицированная в двух различных лекарствах. Дублирование аспирина привело к
идентичному двойному лекарству диаспирину, соединенного без связей. Такрин,
ингибитор ацетилхолинэстеразы, был соединен с помощью связей (полиметиленовая
цепь), в результате чего был образован дитакрина. Салициловая кислота и
структура парацетамола перекрываются (способ наложения), образуя неидентичное
двойное лекарство ацетаминосалол (рисунок 1.1) [2].
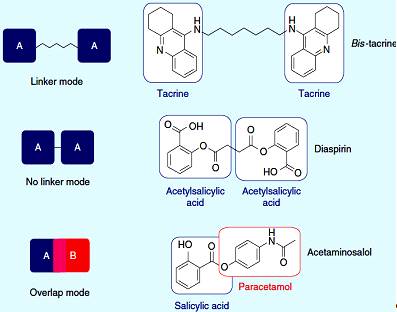
Рисунок 1.1 - Способы соединения двойных лекарств
Неидентичные двойные лекарства также называют лекарствами двойного
действия или гибридами из-за различного фармакологического результата, который
дают две представленные фармакофорные связи. Конструкцию лекарств двойного
действия, названную симбиотическим подходом, можно понять соответственно по
двум стратегиям (схема 1.2). Первая стратегия объединение двух отобранных
неидентичных фармакофоров в гибридную молекулу как иллюстрирование
сульфаниламидной производной. Ассоциативный синтез хлоробензасульфонамида с
производной индола через метиленовые связи приводит к образованию двойного β
- блокатора и
мочегонного агента. Вторая стратегия начинается с соединения-лидера, который,
как уже известно, оказывает оба действия. Рациональная оптимизация приведет к
лекарству двойного действия [1].
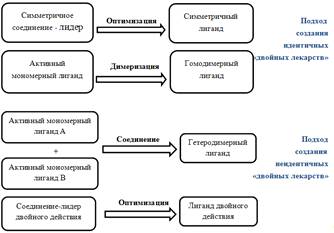
Схема 1.2 - Конструкция двойных лекарств
2. Гомодимеры и симметричные лиганды
Димеризация биологически активной молекулы является альтернативным
подходом в процессе оптимизации соединения-лидера. Обычно дублирование
фармакофора приводит к эквивалентной или более активной производной, которая
показывает различную селективность и фармакокинетические свойства.
Ингибирование фермента будет улучшено, используя гомодимеры ингибиторы.
.1 Симметрия в природе
Природа древний производитель структур с высокой степенью симметрии,
которая позволяет уменьшать информацию и сложность уровней. Естественная
симметрия наблюдается в макромолекулах (олигомеры) таких как ВИЧ, гемоглобин и
инсулин. Соединение мономеров и гексамеров инсулина в присутствии цинка,
приводит к образованию макромолекулярного комплекса с высокой степенью
симметрии (симметрия C3). ДНК, посредством симметричной двухцепочечной
структуры, определяет морфологию и функции клетки. Эти хорошо организованные
высокомолекулярные системы, представляют собой сайты связывания для небольших
молекул, включая воду и ионы. Естественные симметрические структуры обычно
представляют ось симметрии C2, например алкалоид лобеланин (для лечение
наркотической зависимости), спартеин (лечение болезни Грейвса) или
изохондодендрин, и антикоагулянты дикумарол и госсупол. Известны некоторые
примеры симметрических структур C3. Валиномицин, циклический пептидо-лактонный
антибиотик, селективный K - транспортер. Он состоит из циклического тримера,
содержащего l-валин, d - α-гидроксисовалериановую кислоту, d-валин и l - лактат
[3].
2.2 Гомодимеры как лиганды рецепторов
Идентичные двойные лекарства показали большую способность к
потенцированию и / или селективность к рецептору, как лиганды рецептора, по
сравнению с их составляющим единичным звеном. Несколько биогенных аминов
(катехоламины), четвертичные аммониевые соли (ацетилхолин), и пептиды
(ангиотензин, эндотелин) принадлежат к известному классу - двойных рецепторов
G-белка. Они представлены одной субъединицей с семью трансмембранных
сегментами, три внеклеточных и три внутриклеточных петли, которые соединены с
G-белками. Дублирование лекарств в пределах этой серии лигандов было эффективно
в нескольких случаях. Пиперидин - основы димерного лиганды были подготовлены, и
была оценена их способность блокировать транспорт дофамина (DA) и серотонина
(5-HT). Два единичных транс - пиперидина были связаны пентаметиленовой цепью в
гомодимерный лиганд. Процесс димеризации показал увеличение влияния на
деятельность транспортера DA (DAT) и по 5-HT транспортеру (SERT) [4]. Некоторые
селективные антагонисты β1 адренорецепторов были разработаны дублированием
известного окспренолола. Фармакофор фенолоксипропаноламин был димеризован с
помощью метиленовой цепи, для образования симметричного окспренолола. В
зависимости от длины связывающей цепи, могут быть получены селективные β2 или β1 антагонисты. Метоктрамин, селективный антагонист M2,
является полезным для характеристики рецепторов АХ мускаринового типа.
Селективность к М2 - рецепторам была улучшена, путем модификации
фрагмента метоктрамина. Замена 2-месоксибензильной группы, гидрофобным
фрагментом в пирензепине, приводит к образованию очень мощного антагониста M2,
тогда как пирензепин известен как селективный антагонист M1 -
рецепторов. Димеризация фармакофора пирензепина приводит к новому антагонисту с
различной селективностью. Недавно, исследования показали, что длина
полиметиленовой цепи производного метоктрамина полиамина является очень важной,
при преобразовании антагониста мускариновых рецепторов в селективный антагонист
никотиновых рецепторов. Таким образом, по общему образцу, были разработаны
симметрические двойные лекарства, действующие как антагонисты различных
рецепторов [5].
2.3 Гомодимеры как ингибиторы ферментов
Симметрическое расположение в ферментах гомодимеров или тетрамеров
определяет активный центр фермента симметричного вида. Таким образом,
симметричные ингибиторы будут соответствовать связывающему участку фермента.
Обратная транскриптаза ВИЧ (ВИЧ RT) и протеаза (PR ВИЧ) важны для созревания и
производства инфекционных вирусных частиц. Комбинированное ингибирование ВИЧ
транскриптазы и протеазы способно снизить вирусную нагрузку в крови пациентов
[6]. Ферменты, которые являются соответственно гетеро - и гомодимерами для ВИЧ
транскриптазы и протеазы, хорошо охарактеризованы: больше чем 170 структур
протеазы ВИЧ и ее комплексов с различными ингибиторами были решены методами
кристаллографии белка. Симметричная природа протеазы ВИЧ использовалась в
поиске новых лекарств против ВИЧ, которые воплотят предсказанную особенность
активного сайта. Разработка ингибиторов протеаз ВИЧ привела к симметричным
структурам, которые можно разделить на две группы: (a) псевдосимметричные
структуры, такие как производные А74,704 и L700,417, которые содержат
асимметричные атомы в непосредственной близости к ингибитору двойной оси; (b)
полностью C2-симметричные, как ингибиторы циклической мочевины и производные
диола (рисунок 2.1) [7].
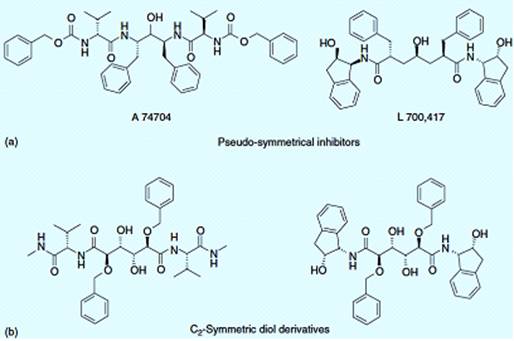
Рисунок 2.1 - Ингибиторы обратной транскриптазы и протеазы ВИЧ
2.4 Гомодимеры как лиганды ДНК
Молекула ДНК является основным объектом многих противоопухолевых агентов. Маленькие молекулы, которые связываются с ДНК интеркалированием, требуют для эффективного связывания полициклических систем в своей структуре. Из-за симметрического расположения двухцепочечной спирали, симметрия найдена в структуре лигандов ДНК. Пентамидин и диамидинобензимидазол (рисунок 2.2) связываются в малой бороздке ДНК и показывают более высокое сродство к областям, богатым основаниями. Соединения с четным числом метиленовых связок бензольного кольца имидазола, имеют более высокое сродство к ДНК, чем те же с нечетным числом метиленов. Моно-интеркалятором DACA, был димеризован с помощью аминополиметиленовой цепи смешанный ингибитор топоизомеразы I/II с цитостатической активностью на линии опухолевых клеток [8].
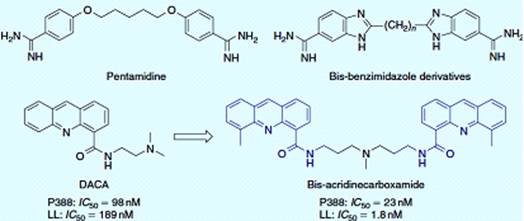
Рисунок 2.2 - ДНК лиганды
Поиск катионных холинергических агентов привел к многочисленным двойным лекарствам. Димеры четвертичных аммониевых солей гексаметония и декаметония являются мощными блокаторами в ганглиях и в нейромышечном синапсе соответственно (рисунок 2.4). Другие нейромышечные блокаторы, такие как сукцинил и себацил дихолин можно рассматривать как двойные лекарства ацетилхолина.
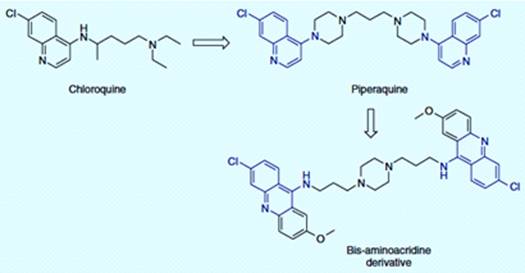
Рисунок 2.3 - Двойные лекарства аминоакридина
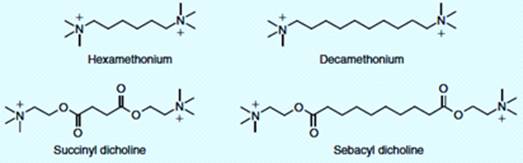
Рисунок 2.4 - Холинергические двойные лекарства
3. Гетеродимеры и лиганды двойного действия
Гетеродимеры и лекарства двойного действия оказывают свое двойное
действие на две различные биологические цели. Это могут быть рецепторы,
ферменты или их комбинация. Объединение двух физиологических эффектов
предназначено для получения синергический эффекта (возрастания эффективности) в
лечении болезни или расстройства. Гибридные молекулы можно получить в
результате объединения двух компонентов различной активности (ассоциативных
синтез) или из соединения с двойным действием. В первом случае, два фармакофора
связаны и идентифицированы, тогда как во втором случае часто возникает
трудность в определении химической части молекулы, которая обладает
биологической активностью. В последнем случае, конструкция лекарства двойного
действия часто основана на структурных модификациях одного из двух
фармакофоров, путем включения важных элементов другого фармакофора.
3.1 Гибридные молекулы как лиганды двух различных рецепторов
обладают физическими, биохимическими и структурными сходствами. Таким образом, селективность к биогенным аминам, таким как норадреналин (NA), (5-HT) серотонин, дофамин (DA) и гистамин (H) зависит от типичного взаимодействия и дополнительных обязательных взаимодействий. Поскольку фармакофоры всех этих лигандов подобны, контроль за их селективностью является важной проблемой химии лекарств. Таким образом, представляет интерес синтез гибридных лекарств, которые связывают различные участки GPCRs как агонисты, антагонисты или агонист-антагонист.
В результате поиска антипсихотических средств без побочных эффектов (например, экстрапирамидные побочные эффекты), антагонисты 5-HT2 рецепторов, такие как ританзерин показали уменьшение побочных симптомов шизофрении. Таким образом, было предложено, что комбинированное введение антагониста 5-HT2 и антагониста D2 рецепторов может быть эффективным в лечении шизофрении. Исследование соединенного γ-карболина, показало что мощное сродство к 5-HT2 и умеренное сродство к D2 рецепторам, было достигнуто и привело к созданию соединения с равносильным и наномолярным сродством к обоим рецепторам [10]. Эффективное антипсихотическое средство Зипрасидон было также разработано из производного нафтилпиперазина с умеренным антагонизмом к 5-HT2А и D2 рецепторам. Положительные инотропные препараты, такие как армродипин были разработаны путем объединения в одной молекуле антагониста гистамина H1 и агониста H2. Объединение слабого частичного агониста H2 со слабым антагонистом H1 привело к образованию гетеродимера, который является очень мощным агонистом H2 (100-кратное увеличение) и антагонистом H1, в 10 раз более активного, чем мономерный фармакофор.
Антигистаминный препарат Лоратадин является слабым антагонистом PAF. Учитывая физиологическое значение PAF при астме, это представляет потенциальный терапевтический интерес, чтобы противодействовать одной молекулой действию обоих медиаторов. Была достигнута оптимизация этого лекарства двойного действия, что привело к повышению антагонизма к PAF и подобному антагонизму к H1. Тромбоксан А2 (TXA2) также является условием развития астмы. Поэтому, были приложены усилия, к разработке антагонистов рецептора TXA2. Концепция симбиотического подхода привела к недавнему открытию производных дибензоксепина. Противоаллергическое средство и антагонист H1 KW-4994, также обладает слабым антагонизмом к TXA2. Успешные модификации привели к созданию двойного антагониста TXA2 и H1, такого как KF 15766 (рисунок 3.1) [11].