Материал: Резников В.А., Штейнгарц В.Д. Аминокислоты PDF
HO2C |
CO2H |
|
RCH2NH2 |
HO2C |
CO2H |
|
O |
|
|
N |
|
|
|
|
|
||
|
|
- H2O |
|
||
α-кетоглутаровая |
|
|
CH R |
||
|
|
|
2 |
||
|
|
|
|
||
кислота |
|
|
|
|
|
HO2C |
CO H |
|
H2O |
HO2C |
CO H |
|
2 |
|
|
|
2 |
|
N |
- RCHO |
|
NH2 |
|
|
|
|
|
||
CHR |
глутаминовая кислота |
|
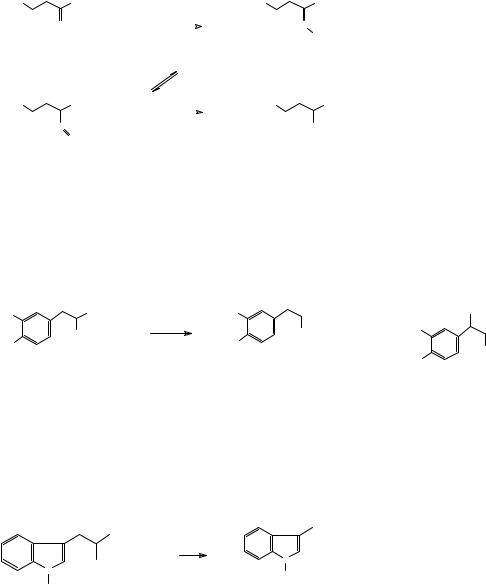
Реакции переаминирования, протекающие в организме, позволяют регулировать аминокислотный баланс – синтезировать аминокислоты, поступающие с пищей в недостатке (кроме незаменимых аминокислот!).
Декарбоксилирование аминокислот в организме происходит при действии ферментов, называемых декарбоксилазами. Некоторые из образующихся в результате реакции аминов, обладают биологической активностью. Особенно существенным является образование дофамина при декарбоксилировании диоксифенилаланина, поскольку дофамин является предшественником адреналина.
HO |
CO H |
|
HO |
OH |
|
2 |
|
|
|
|
NH2 |
|
|
HO |
HO |
- CO2 |
HO |
NH2 |
|
|
NHCH3 |
|||
|
|
|
|
|
диоксифенилаланин |
|
дофамин |
HO |
|
|
|
|||
адреналин
Подобные превращения могут протекать также при действии ферментов, функционирующих в бактериях, участвующих в процессе пищеварения человека. Под действием таких ферментов протекает, например, превращение триптофана в скатол (3-метилиндол) – вещество с сильным специфическим запахом, во многом определяющим запах экскрементов, применяемое, впрочем, в парфюмерии в качестве сенсибилизатора обонятельных рецепторов.
|
CO2H |
|
|
N |
NH2 |
N |
|
H |
|||
H |
|
||
|
|
триптофан скатол
АРОМАТИЧЕСКИЕ АМИНОКИСЛОТЫ
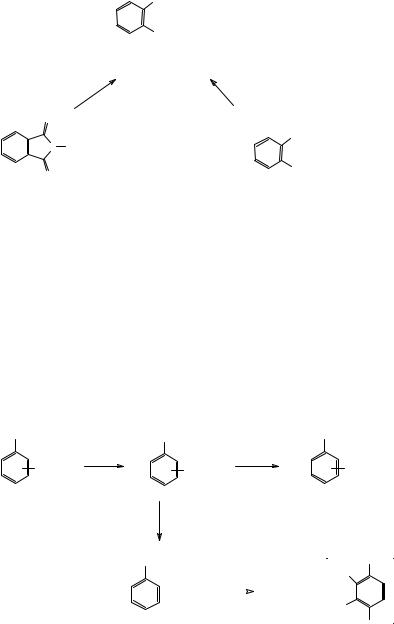
Ароматические аминокислоты можно синтезировать из нитробензойных кислот восстановлением нитрогруппы, либо в условиях каталитического гидрирования, либо взаимодействием с гидразином в присутствие никеля Ренея (восстановление диимидом). По этой схеме в промышленности получают мета- и пара-аминобензойные кислоты. орто-Аминобензойную (антраниловую) кислоту получают при действии гипохлоритом натрия на фталимид либо на фталиминовую кислоту – моноамид фталевой кислоты, являющуюся, по-видимому, промежуточным соединением к орто-аминобензойной кислоте от фталимида (перегруппировка Гофмана).
16
NH2
COOH
антраниловая кислота
NaOCl |
NaOCl |
OH-, H2O
O
CONH2
N H
O |
COOH |
|
фталиминовая |
||
|
||
|
кислота |
Напишите механизм превращения фталимида в орто-аминобензойную кислоту.
Аминобензойные кислоты имеют меньшую температуру плавления, чем алифатические аминокислоты, и значительно лучше растворяются в органических растворителях. Это связано с тем, что они в значительной мере не являются цвиттер-ионными соединениями. Причина этого – меньшая основность аминогруппы, связанной с ароматическим кольцом (сравните основность анилина и циклогексиламина). Все три изомерные аминобензойные кислоты имеют сходные химические свойства, сочетающие реакционную способность как ароматических аминов, так и ароматических кислот. Так, при взаимодействии этих соединений с азотистой кислотой образуются соли диазония, которые в нейтральной среде могут существовать в виде внутренних солей (цвиттер-ионов). Соли диазония, полученные из аминобензойных кислот, могут быть использованы в превращениях, характерных для всех солей диазония, в частности, вступать в реакцию Зандмейера.
NH2 |
N + |
X |
|
2 |
|
CO H |
NaNO2 |
CO2H |
HX |
CO - |
|
H+ |
Cu2X2 |
||||
2 |
2 |
OH-
N2+ |
|
H |
|
|
||||
|
|
|||||||
|
|
|
|
|
|
H |
|
|
|
|
CO - |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|||
2 |
|
|
|
H |
|
|
||
|
|
(циттер-ион из |
|
|
|
|||
|
|
|
H |
|
|
|||
цвиттер-ион антраниловой |
|
|
|
|||||
|
|
|||||||
|
|
|
|
|||||
|
|
кислоты) |
дигидробензол |
|||||
Перечислите заместители X, которые могут быть введены в состав молекулы вместо диазониевой группировки. В каких условиях происходят эти реакции?
Отличительной особенностью соли диазония, полученной из антраниловой кислоты в среде органического растворителя при действии алкилнитритов, является легкость ее разложения при фотолизе или термолизе с образованием дегидробензола. Дегидробензол является исключительно реакционноспособным соединением, и может вступать в различные превращения, например в реакцию Дильса-Альдера в качестве диенофила.
В каких еще реакциях возможно образование дегидро-бензола?
Изобразите структуру продукта взаимодействия де-гидробензола с антраценом.
В случае фотохимического генерирования дегидробензола возможна его димеризация. Изобразите структуру димера дегидробензола. Возможна ли эта реакция в условиях термического генерирования дегидробензола?
17
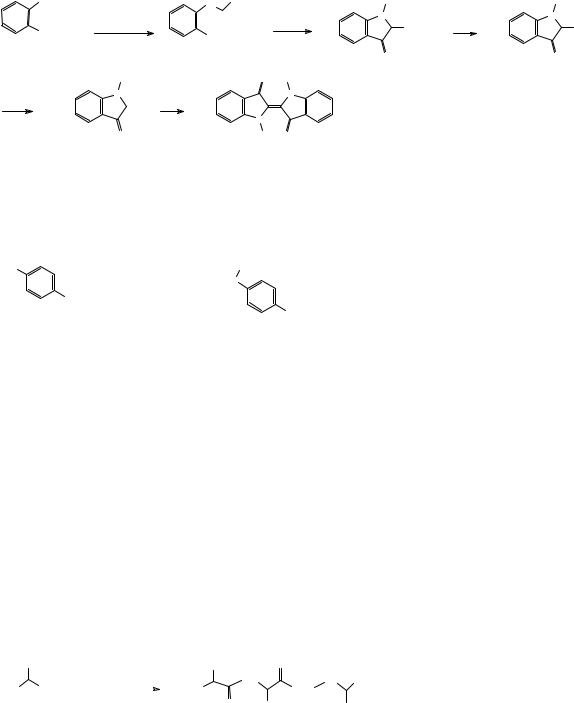
Антраниловая кислота используется в качестве промежуточного соединения в синтезе азокрасителей в качестве диазосоставляющей, а также как исходное соединение в синтезе индиго – синего красителя, используемого с незапамятных времен. Ранее предшественник индиго выделяли из сока тропических растений вида Indigofera, теперь его получают из антраниловой кислоты по схеме, представленной ниже.
NH2 |
NH |
CO2Na |
|
H |
|
H |
ClCH2CO2Na |
|
|
NaOH |
N |
H+ |
N |
|
|
CO2Na |
CO2H |
|||
COOH |
CO2Na |
|
|
|||
NaOH |
t °C |
|
|
|
||
|
|
|
O |
|
O |
|
H |
|
O |
H |
|
|
|
N |
O2 |
|
N |
|
|
|
t |
|
|
|
|
|
|
- CO2 |
- H2O |
N |
|
|
|
|
O |
|
H |
O |
|
|
|
индоксил индиго
Предложите механизм реакции циклизации в схеме синтеза индиго, представленной выше.
пара-Аминобензойная кислота используется в синтезе некоторых анестезирующих средств – анестезина (этиловый эфир пара-аминобензойной кислоты), новокаина и дикаина.
H2N |
CH2CH2CH2CH3 |
HN
CO CH CH N(C H ) |
. HCl |
|
|
|
|
|
||||
2 |
2 |
2 |
2 |
5 2 |
CO |
CH CH N(C H ) |
. HCl |
|||
|
|
|
|
|
||||||
|
|
|
|
|
2 |
2 |
2 |
2 |
5 2 |
|
новокаин |
|
дикаин |
|
|
|
|||||
пара-Аминобензойная кислота является фактором роста многих микроорганизмов (витамин Н). Антимикробное действие сульфамидных препаратов основано на том, что они “подменяют” необходимую для жизни бактерий пара-аминобензойную кислоту в ее биохимических превращениях, образуя чужеродные для микроорганизмов продукты. По тому же принципу действует пара- аминосалициловая кислота, являющаяся важным противотуберку-лезным препаратом.
Предложите метод синтеза пара-аминосалициловой кислоты.
ПЕПТИДЫ И БЕЛКИ
Наличие двух функциональных групп в составе молекулы аминокислоты – аминогруппы и карбоксильной группы – обуславливает возможность их межмолекулярного взаимодействия с образованием амида (сравни 26). Образующаяся при этом амидная связь называется пептидной, а образующиеся по этому принципу амиды называют пептидами или полипептидами. Соответственно, пептид, образованный из двух молекул аминокислоты, называется дипептидом, из трех молекул – трипептидом и так далее. Разумеется, цепь полипептида может быть образована как какой-нибудь одной, так и различными аминокислотами.
NH2 |
NH2 |
|
O |
|
|
- (n - 1) H2O |
|
(NH |
NH CO2H |
n R CO2H |
|
R |
|
)(n-2) |
|
|
|||
|
|
O |
R |
R |
пептид
Природные биологически активные полипептиды - это сложные гетерополимеры, различающиеся последовательностью аминокислотных фрагментов, и даже небольшие изменения этой последовательности приводят к изменению их биологической активности. Мы не будем останавливаться здесь на функциях пептидов в живом организме, поскольку они рассматриваются в курсе “Биохимия”. Отметим только, что практически все ферменты являются полипептидами. Белки – тоже полипептиды,
18
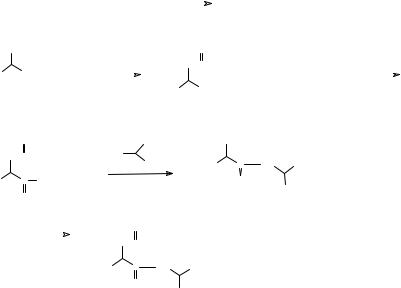
молекулярная масса которых не ниже определенной величины, например 5000. Возможно, различия между белками и иными полипептидами заключены не в химическом, а в пространственном строении молекулы. Для каждого белка гибкая цепь полипептида имеет характерную трехмерную пространственную структуру (супрамолекулярную структуру), например в виде клубка с определенным образом устроенной поверхностью, на которой имеются выступы или впадины. Причем функции белков в организме обуславливаются в значительной степени именно этой трехмерной структурой.
СИНТЕЗ ПЕПТИДОВ
Проблемы, возникающие при синтезе низкомолекулярных пептидов определенного строения, являются следствием бифункциональности исходных соединений и, следовательно, возможности неконтролируемого образования разнообразных пептидных связей как между различными, так и между одинаковыми молекулами аминокислот. Для того чтобы избежать этих осложнений, приходится защищать аминогруппу и активировать карбоксильную. Защищать карбоксильную группу нет необходимости, поскольку она сама по себе обладает достаточно низкой реакционной способностью и способна реагировать с аминогруппой только в весьма жестких условиях. Защитная группа должна устанавливаться селективно именно по защищаемой группе и удаляться в таких условиях, в которых не будут затрагиваться остальные функциональные группы в составе молекулы. Кроме того, когда речь идет об использовании защитных групп в синтезе таких сложных молекул как полипептиды, необходимо, чтобы защита ставилась и снималась с высоким выходом. Например, один из способов защиты (блокировки) аминогруппы заключается во взаимодействии аминокислоты с бензилхлорформиатом. Это соединение получают по реакции эквимолярных количеств бензилового спирта и фосгена. Следует отметить, что бензилхлорформиат быстрее реагирует с аминогруппой, нежели с карбоксильной группой аминокислоты. Впрочем, если даже реакция произойдет и по карбоксильной группе, то в результате образуется смешанный ангидрид, который является активным ацилирующим реагентом по незащищенной аминогруппе другой молекулы аминокислоты (см. ниже).
PhCH2OH + |
COCl2 |
|
PhCH2OCOCl |
|||||||||
|
||||||||||||
|
|
NH2 |
|
|
PhCH2OCOCl |
O |
|
|
EtOCOCl |
|||
R |
CO2H |
NHCOCH2Ph |
|
|
||||||||
|
|
R |
CO2H |
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
аминокислота |
с |
защи- |
|||
|
|
|
|
|
|
|
щенной аминогруппой |
|||||
|
|
O |
|
|
|
|
CO2H |
|
NH2 |
|
|
|
|
|
NHCOCH Ph |
H2N |
|
|
|
|
|
||||
|
|
|
2 |
|
|
|
R' |
R C |
NH |
CO2H |
||
|
|
|
|
|
|
|
||||||
R |
C |
OCOOEt |
|
|
|
O |
R' |
|
|
|||
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
дипептид |
|
|
||
|
|
|
|
|
|
|
|
|
|
|
||
|
HBr/CH |
CO H |
O |
|
|
|
|
|
||||
|
|
3 |
2 |
|
|
|
|
|
|
|
|
|
|
|
или H2/Pd |
NHCOCH2Ph |
|
|
|
|
|
||||
|
|
|
|
|
|
R C NH |
CO2H |
|
|
|
||
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
R' |
|
|
|
|
|
Далее необходимо активировать кислоту с защищенной аминогруппой превращением карбоксильной группы в более активную ацилирующую функцию. Для этого ранее использовали этилхлорформиат, который превращает карбоксильную группу в смешанный ангидрид. Полученная в результате таких превращений молекула способна реагировать только с аминогруппой другой молекулы аминокислоты с образованием дипептида с защищенной концевой аминогруппой. В полученной молекуле содержатся две амидные группы, и для того чтобы получить дипептид необходимо селективно гидролизовать одну из них, то есть снять защитную группу с концевой аминогруппы так, чтобы сформированная пептидная связь осталась незатронутой. Для этого используют либо взаимодействие с раствором бромистого водорода в уксусной кислоте при охлаждении, либо каталитический
19
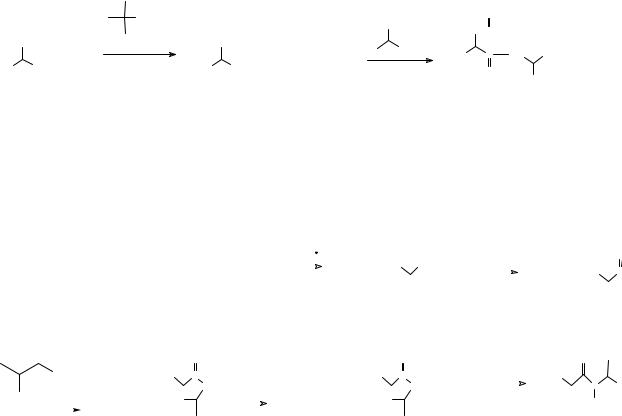
гидрогенолиз. При этом если в синтезе использовались оптически активные аминокислоты, их рацемизация не происходит. Очевидно, что вовлекая в приведенную выше последовательность реакций дипептид с защищенной аминогруппой, можно синтезировать трипептид, тетрапептид, и так далее, варьируя структуру вводимых в реакцию аминокислот, и получить полипептид необходимой длины и структуры. Более совершенный метод синтеза основан на защите аминогруппы третбутоксикарбонильной группой, а для активации карбоксильной группы используется дициклогексилкарбодиимид (ДЦК). Для модификации аминогруппы в составе молекулы аминокислоты с образованием третбутоксикарбониль-ного производного (БОК-производного), ее обрабатывают третбутоксикарбоксазидом. Возникающая при этом защитная группа снимается в более мягких условиях, чем бензилокси-карбонильная – при действии раствора хлористого водорода в уксусной кислоте. ДЦК, как отмечалось выше (26), превращает карбоксильную группу в активное производное, которое образует пептидную связь при взаимодействии с аминами в исключительно мягких условиях.
|
OCON3 |
|
|
NH2 |
|
O |
|
|
|
|
NHCOC(CH ) |
||
|
|
|
|
|
||
NH2 |
(БОКN ) |
NHCOOC(CH3)3 |
|
|
|
3 3 |
R' |
CO2H |
|
|
|||
|
3 |
|
R |
C NH CO2H |
||
R CO2H |
|
R CO2H |
|
ДЦК |
||
|
|
|
O |
|||
|
|
БОК-производное |
|
|
|
R' |
|
|
|
|
|
|
Предложите механизм реакции гидролиза БОК-производного в кислой среде. С чем связана большая легкость протекания реакции по сравнению с бензоилоксикарбонильным производным?
В заключение отметим, что в синтезе пептидов по любому из описанных выше методов для ацилирования обычно используют не саму аминокислоту, а ее эфир, что сводит к минимуму образование побочных продуктов. Ниже приведена классическая схема синтеза дипептида, являющегося аланином, ацилированным по аминогруппе остатком глицина – глицилаланина (gly-ala).
H2NСH2CO2H |
+ PhCH2OCOCl |
a. H2O, OH-(разб.), 5 |
|
PhCH2OCONH CO2H |
|
EtOCOCl |
|
|
O |
|||||
b. H3O+(разб.) |
|
|
|
|
PhCH2OCONH |
COCOEt |
||||||||
Глицин |
бензилхлор- |
|
N-защищенный |
|
|
|
||||||||
|
|
|
|
формиат |
|
|
|
|
глицин |
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
O |
|
|
|
|
O |
|
|
|
O |
|
|
|
OEt |
PhCH2OCONH C |
|
|
|
PhCH2OCONH C |
H2 / Pd |
|
H2N |
|
|||
|
|
|
|
NH |
|
OH- |
|
NH |
|
|
N |
CO2H |
||
|
NH2 |
|
|
|
- PhCH3, -CO2 |
|
||||||||
|
EtO2C |
|
|
|
|
HO2C |
|
|
|
H |
|
|||
|
|
H3O+ |
|
|
|
|
||||||||
этиловый эфир |
|
|
|
|
|
|
|
глицилаланин |
||||||
|
|
|
|
|
|
|
|
|
||||||
аланина |
|
|
|
|
|
|
|
|
|
(gly-ala) |
|
|||
Аналогичным образом глицилаланин может быть синтезирован с применением третбутилкарбоксазида для защиты аминогруппы и ДЦК для активации карбоксильной группы. Выходы продуктов на каждой стадии реакции достаточно высоки и нет принципиального запрета на синтез сколь угодно длинной пептидной цепи с применением этой последовательности реакций. Однако совершенно ясно, что даже если выход на каждой стадии составит более 90%, то при синтезе пептида, включающего, например, 100 аминокислотных фрагментов, в итоге выход конечного продукта составит миллионные доли процента! Поэтому синтез достаточно сложного пептида с использованием этой методологии практически нереален – очень велики затраты времени и очень низок выход целевого продукта. Несколько упрощает дело то обстоятельство, что в природных пептидах встречаются повторяющиеся звенья из нескольких аминокислотных остатков. Это означает, что в синтезе вместо двух аминокислот могут быть использованы два пептида, в одном из которых защищена концевая аминогруппа и активирована карбоксильная группа, а в другом - аминогруппа не защищена, а карбоксильная группа превращена в сложный эфир. Иными словами, синтез более рационально вести не по схеме 1 + 1 2 + 1
20