Материал: Резников В.А., Штейнгарц В.Д. Аминокислоты PDF

Как уже отмечалось ранее, практически все природные α-аминокислоты оптически активны (за исключением глицина) и относятся к L-ряду. Это означает, что в проекции Фишера, если внизу расположить заместитель, а вверху карбоксильную группу, то аминогруппа будет находиться слева.
|
CO2H |
|
CO2H |
H |
CO2H |
||
H2N |
|
H |
H |
|
NH2 |
|
C |
|
|
H3C |
NH2 |
||||
|
|
||||||
|
|
|
|
|
|
|
|
|
R |
|
R |
|
|
||
L-аминокислота |
D-аминокислота |
(S)-аланин |
|||||
Это, разумеется, не означает, что все природные аминокислоты вращают плоскость поляризованного света в одну и ту же сторону, поскольку направление вращения определяется свойствами всей молекулы, а не конфигурацией его асимметрического атома углерода. Большая часть природных аминокислот имеет S-конфигурацию (в том случае, когда в ее состав входит один асимметрический атом углерода). Некоторые микроорганизмы синтезируют аминокислоты D-ряда. Такие аминокислоты называют “неприродными”.
КИСЛОТНО-ОСНОВНЫЕ СВОЙСТВА
Аминокислоты – амфотерные соединение, поскольку в состав их молекулы входит как кислотная – карбоксильная группа, так и основная – аминогруппа. В сильнокислой среде карбоксильная группа полностью недиссоциирована, а аминогруппа протонирована. Наоборот, в сильнощелочной среде аминогруппа находится в виде свободного основания, а карбоксильная группа – в виде карбоксилатаниона. В кристаллическом же состоянии аминокислоты существуют в виде цвиттер-иона (или бетаина), где протон с карбоксильной группы перенесен на аминогруппу.
H CO2- |
H+ |
H CO2H |
H+ |
H CO2H |
R |
OH- |
R |
OH- |
R + |
NH |
|
NH |
|
NH |
2 |
|
2 |
|
3 |
щелочная |
|
|
|
кислая среда |
|
|
|||
среда |
|
|
|
|
H |
- |
|||
R |
|
|
|
CO2 |
+ |
||||
|
NH3 |
|||
цвиттер-ион
Если через водный раствор аминокислоты пропускать электрический ток, то в зависимости от рН среды молекулы аминокислоты будут двигаться либо к аноду, либо к катоду в соответствии с их степенью протонирования-депротонирования. Если величина рН такова, что аминокислота существует преимущественно в виде цвиттер-иона, а концентрации протонированной и депротонированной форм равны, то она не будет перемещаться ни к аноду, ни к катоду. Это, разумеется, не обязательно должно происходить при рН = 7, поскольку константа диссоциации карбоксильной группы чаще всего не совпадает с константой протонирования аминогруппы (или константой диссоциации аммониевой группы). Такое значение рН среды является характеристичным для каждой аминокислоты и называется ее изоэлектрической точкой (pI).
При пропускании постоянного тока через раствор смеси аминокислот последние будут перемещаться к аноду или к катоду с различными скоростями, зависящими от величины рН среды. Разделение и анализ смесей аминокислот, основанный на этом явлении, называется электрофорезом.
Используя кислотно-основные равновесия аминокислот, можно проводить их разделение на ионообменных колонках. Для этого колонку, наполненную адсорбентом (полимером, содержащим в составе макромолекулы, привитые кислотные группы, обычно сульфогруппы), промывают раствором щелочи. При этом кислотные группы переходят в анионную форму. После этого в колонку вносят смесь
11
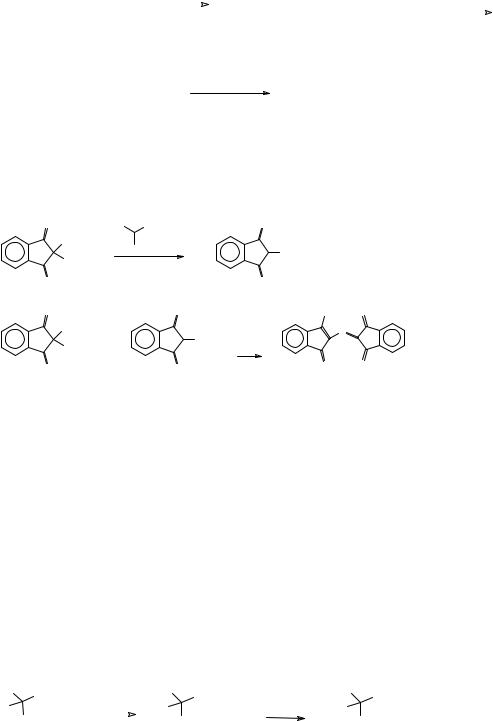
аминокислот в протонированной форме (кислый раствор). Вследствие солеобразования аминокислоты связываются с сульфогруппами адсорбента. Далее колонку начинают промывать (элюировать) буферным раствором, постепенно увеличивая величину рН. При этом различные аминокислоты начинают переходить в анионную форму и смываться с колонки при различных значениях рН. Пропуская выходящий из колонки раствор через детектор, количественно определяют содержание индивидуальных аминокислот в исследуемой смеси.
|
|
|
|
|
|
|
|
|
|
|
|
|
- |
Na+ |
+ |
|
|
|
|
|
|
|
|
|
|
|
|
полимер |
|
SO |
|
|
|
||||||
полимер |
|
SO3H |
+ NaOH |
|
|
|
|
|
|
|
|
|
|
3 |
+ |
H3NCHRCO2H |
|
|
|
|
- H2O |
|
|
|
|
|
|
|
|||||||||||
|
|
|
(раствор) |
|
|
|
|
|
|
Cl- |
-NaCl |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
|
+2OH- |
|
|
|
|
|
- |
|
|
|
|
|||
полимер |
|
SO3- H3NCHRCO2H |
- |
|
|
|
- |
|
|
|
|
H2NCHRCO2 |
|
|
|
|
|||
|
полимер |
|
SO |
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Обычно детекторы определяют количество вещества, находящегося в растворе, по величине поглощения света, однако растворы аминокислот, как правило, не поглощают свет ни в видимой, ни в ультрафиолетовой области. Для того чтобы обнаружить присутствие аминокислоты в растворе, проводят реакцию с нингидрином.
O |
|
R |
CO2H |
O |
|
OH |
NH2 |
OH |
|
|
OH |
|||
|
-NH3 |
-CO2 |
|
|
|
|
|
||
O |
|
|
|
O |
нингидрин
+ RCHO
O |
|
O |
O- NH4+ |
O |
OH |
|
|
N |
|
OH |
+ |
|
OH |
|
|
NH3 |
O |
||
O |
|
O |
O |
|
|
|
|
Как видно из представленной выше схемы, независимо от структуры аминокислоты при взаимодействии с нингидрином образуется одно и тоже соединение, обладающее интенсивной синефиолетовой окраской, концентрация которого зависит от концентрации аминокислоты в исследуемом растворе и легко может быть измерена по величине поглощения света, проходящего через раствор.
Некоторые из природных аминокислот не образуют синего окрашивания при обработке нингидрином. Как вы думаете, какие это аминокислоты?
РЕАКЦИИ АМИНОКИСЛОТ
Химические свойства α-аминокислот определяются наличием в составе их молекулы двух функциональных групп – аминогруппы и карбоксильной группы. Например, для них характерно образование сложных эфиров, которое происходит при пропускании хлористого водорода через раствор аминокислоты в спирте. При этом, разумеется, образуется хлоргидрат сложного эфира, свободное основание можно получить действием на соль триэтиламином или оксидом серебра. Другим способом получения метиловых эфиров аминокислот является реакция с диазометаном, которая происходит по карбоксильной группе.
H |
CO2H |
|
H |
CO2Et |
|
H |
CO2Et |
||
R |
EtOH |
R |
NEt3 |
R |
|||||
|
|
Cl - |
|
||||||
|
NH |
|
+NH |
|
|
|
NH |
||
|
HCl |
3 |
|
|
|||||
|
2 |
|
|
|
|
|
2 |
||
В отличие от этого реакция с галоидными алкилами происходит по аминогруппе. Например, при взаимодействии избытка йодистого метила с глицином в присутствии бикарбоната натрия происходит образование четвертичной соли, от которой при действии избытка основания отщепляется молекула
12

йодистого водорода и образуется бетаин – внутренняя соль. Другой способ получения этого соединения - взаимодействие натриевой соли хлоруксусной кислоты с триметиламином.
+ |
O |
|
|
- H+ |
|
|
O |
|
|
|
|
|
+ |
O |
|
||
H3N |
|
O - |
|
NaHCO3 |
|
H2N |
O - |
|
3 CH3I |
(H3C)3N |
|
O - |
|||||
глицин |
|
|
NaHCO3 |
бетаин |
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
t |
|
N(CH3)3 |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
O |
|
|
|
|
|
|
|
|
ClCH2CO2Na |
||||||
(H3C)2N |
|
- |
|
|
t |
|
O |
|
|
|
|||||||
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
OCH3 |
|
|
|
|
O |
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
(H3C)2N CH3
Бетаин, получивший свое название от свеклы (Beta vulgaris), в соке которой он содержится, дал название классу соединений, которые являются внутренними солями, содержащими анион и катион в составе одной молекулы. Можно сказать, что аминокислоты в кристаллическом состоянии находятся в виде бетаина (см. выше).
Интересной особенностью бетаина является его способность превращаться при нагревании в метиловый эфир диметиламиноуксусной кислоты, причем эта реакция является обратимой. Это превращение представляет собой внутримолекулярное нуклеофильное замещение, где в качестве нуклеофила выступает карбоксилат-анион, а в качестве уходящей группы – диметиламиногруппа. В случае протекания реакции в обратном направлении нуклеофилом является атом азота аминогруппы, а уходящей группой – карбоксилат-анион.
Исходя из структурных формул бетаина и метилового эфира диметиламиноуксусной кислоты можно сделать вывод об их физических свойствах. Используя эти соображения, предложите условия, в которых равновесие взаимопревращения этих соединений сдвигается в ту или иную сторону.
При взаимодействии аминокислот с пятихлористым фосфором образуются хлоргидраты хлорангидридов аминокислот. Свободные основания этих соединений обычно довольно неустойчивы вследствие легкости ацилирования аминогруппы, находящейся в составе молекулы.
H |
CO2H |
|
H |
O |
|
|
PCl5 |
C |
Cl |
||||
|
||||||
R |
R |
|||||
NH2 |
- POCl3 |
|
Cl - |
|||
|
+NH |
|
||||
|
|
3 |
||||
|
|
|
|
|
При взаимодействии аминокислот с ангидридами или хлорангидридами карбоновых кислот происходит ацилирование по аминогруппе с образованием амидов. Например, при взаимодействии глицина с хлористым бензоилом образуется бензоилглицин или гиппуровая кислота. Излишки азота и бензойная кислота, попадающая с пищей, выделяются из организма животных в виде этого соединения.
+ |
O |
|
|
|
O |
|
|
PhCOCl |
|
|
|
H3N |
|
O - |
PhCOHN |
OH |
|
|
|
||||
глицин |
|
|
гиппуровая кислота |
||
При взаимодействии эфиров α-аминокислот с азотистой кислотой образуются диазоэфиры – соединения, относящиеся к классу диазосоединений, простейшим представителем которого является диазометан. Сразу заметим, что эта реакция является характерной только для эфиров α-аминокислот, аминокислоты с другим взаимным расположением аминогруппы и карбоксильной группы, а также их эфиры реагируют с азотистой кислотой по иному, – так же, как и обычные алифатические амины, то есть с образованием неустойчивых солей диазония, разложение которых приводит к спиртам (в данном случае – оксикислотам) наряду с другими продуктами рекции.
13
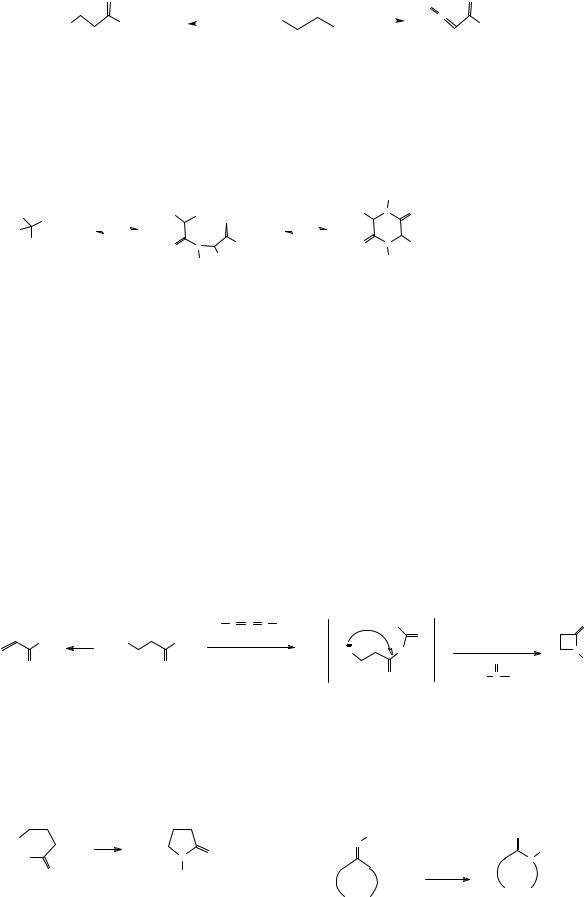
|
O |
|
O |
- |
O |
|||||
|
HNO2 |
H2N |
|
|
|
HNO2 |
N |
N+ |
||
|
|
|
|
|
||||||
HO |
OH |
|
|
|
|
|
|
|
OEt |
|
|
|
|
|
|
OR |
R = Et |
|
|||
|
|
|
||||||||
|
R = H |
|
|
|
|
|
диазоуксусный эфир |
|||
|
|
|
|
|
|
|
|
|
||
Почему не могут существовать диазокислоты?
Интересной особенностью аминокислот является реакция их самоацилирования, которая может происходить при их нагревании и имеет сходство с реакциями, протекающими при нагревании оксикислот. Так, при нагревании α-аминокислот происходит их бимолекулярная циклизация с образованием дикетопиперазинов – соединений родственных по строению лактидам. Аналогичная реакция происходит и с эфирами α-аминокислот в более мягких условиях.
|
|
|
|
|
|
|
|
H |
|
H CO2H |
_ |
R |
NH2 |
O |
|
_ |
R |
N |
O |
+ H2O |
|
|
+ H2O |
|
|
|
|||
2 R |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
t |
|
|
|
t |
|
|
|
|
|
NH2 |
O N |
OH |
|
O |
N |
R |
|||
|
|
|
H |
R |
|
|
|
H |
|
|
|
дипептид |
|
|
дикетопи- |
||||
|
|
|
|
|
|
|
перазин |
|
|
Эфиры аминокислот образуют дикетопиперазины в более мягких условиях, чем сами аминокислоты. Объясните причину этого явления.
При нагревании дикетопиперазинов в кислой (или щелочной) среде происходит размыкание цикла и образуется дипептид – ациклический димер аминокислоты, который в дальнейшем может быть превращен в две молекулы исходной аминокислоты. При нагревании дипептида возможно замыкание цикла с образованием дикетопиперазина. Другое возможное направление реакции – взаимодействие дипептида с еще одной молекулой аминокислоты и так далее, что может привести к полимерному полиамиду – полипептиду. Отметим, что в данном случае это направление реакции имеет меньшее значение, хотя сами полипептиды исключительно важные соединения и будут обсуждены ниже.
β-Аминокислоты при нагревании или при действии кислот подобно β-оксикислотам, превращаются в α,β-непредельные кислоты, а замыкания четырехчленного цикла в результате внутримолекулярного образования амида при этом не происходит. При взаимодействии же β-аминокислот с дициклогексилкарбодиимидом (ДЦК) происходит образование четырехчленного циклического амида – β-лактама. Причиной этого является реакция ДЦК с карбоксильной группой, приводящая к ее активации в результате превращения плохо уходящей группы ОН в хорошо уходящую группу, и последующее внутримолекулярное ацилирование.
|
|
|
|
R N C N R |
|
RHN |
NR |
|
O |
OH |
t |
H2N |
OH |
ДЦК |
|
|
|
|
|
H2N |
O |
|
|
N |
|||||
O |
|
|
O |
R = циклогексил |
|
O |
|||
|
|
|
|
_ |
H |
||||
|
|
|
|
|
|
O |
RHN C NHR |
β-лактам |
ДЦК является широко распространенным конденсирующим реагентом в синтезе пептидов, и с механизмом его действия вы уже ознакомились в разделе, посвященном карбоновым кислотам.
β-Лактамы весьма неустойчивые соединения и легко гидролизуются с образованием исходных аминокислот. β-Лактамный фрагмент входит в состав пенициллина. γ-Лактамы легко образуются при нагревании γ-аминокислот. Лактамы с большим размером цикла получают бекмановской перегруппировкой оксимов циклических кетонов.
H |
+ |
t |
|
OH |
O |
N |
|
N |
|
||
3 |
O- |
-H2O |
N O |
|
N H |
|
|
||||
|
O |
|
H |
|
H2SO4 |
γ-лактам |
(CH2)n |
|
(CH2)n |
14
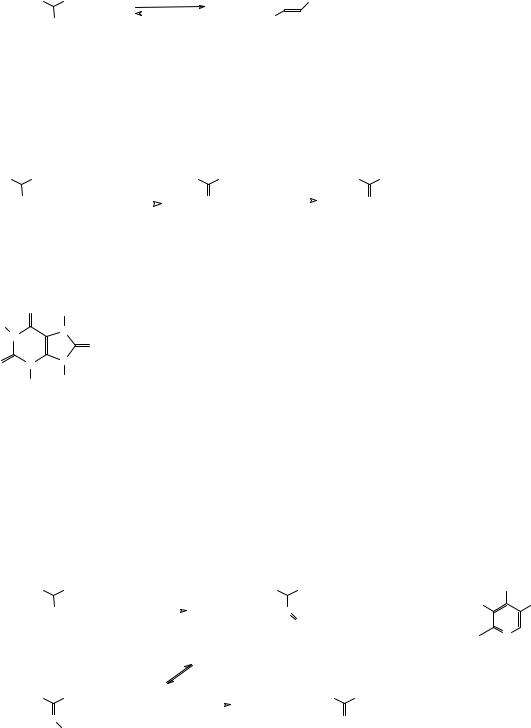
РЕАКЦИИ АМИНОКИСЛОТ IN VIVO
Аминокислоты в организме участвуют не только в синтезе белков, но и в некоторых других превращениях. Эти превращения являются экзотермическими и снабжают организм энергией. Три основных типа превращений аминокислот в организме –дезаминирование, переаминирование и декарбоксилирование. Дезаминирование может происходить окислительным и неокислительным путем. Неокислительное дезаминирование встречается в основном у бактерий и грибков. Например, аспарагиновая кислота превращается в фумаровую кислоту под действием фермента аспартазы.
HO2CCH2C CO2H |
аспартаза |
CO2H |
|
|
HO2C |
NH |
- NH3 |
|
2 |
|
фумаровая |
аспарагиновая |
|
|
|
кислота |
|
кислота |
|
|
|
|
Для протекания окислительного дезаминирования наряду с ферментом (оксидазой) необходим окислитель – акцептор водорода, в качестве которого обычно выступает флавинадениндинуклеотид (ФАД). Эта реакция протекает через стадию образования иминокислоты, которая далее гидролизуется в кетокислоту. Примером такой реакции является превращение аланина в пировиноградную кислоту.
H3C CO2H |
H3C CO2H |
|
H3C |
CO2H |
|
NH2 |
оксидаза |
NH |
+H2O |
|
O |
|
-NH3 |
|
|||
|
|
||||
аланин |
|
|
пировино- |
||
|
|
|
|
градная |
|
|
|
|
|
кислота |
|
|
Реакция дезаминирования, удаляя из организма избыток аминокислот, приводит к накоплению в нем |
||||||||
|
|
|
аммиака и аминов. Эти соединения часто являются токсичными для организма и их |
||||||
|
O |
H |
|||||||
H |
также необходимо удалять. Организмы, обитающие в воде, выделяют аммиак |
||||||||
|
N |
||||||||
N |
|
непосредственно в окружающую среду. Наземные животные используют для этой |
|||||||
|
|
O |
цели главным |
образом |
мочевину |
(млекопитающие) и |
мочевую |
кислоту |
|
O |
N |
N |
(пресмыкающиеся |
и птицы). В организме взрослого человека мочевая |
кислота |
||||
H |
|||||||||
|
H |
вырабатывается в |
качестве |
побочного |
продукта в количестве |
около 0,5 |
г/сутки. |
||
|
|
||||||||
мочевая кислота |
Увеличение концентрации этого соединения приводит к мочекаменной болезни или |
||||||||
подагре. |
|
||||||||
|
|
|
|
|
|
|
|||
|
Реакция переаминирования заключается |
во взаимопревра-щении аминокислот и кетокислот и |
|||||||
происходит под действием ферментов трансаминаз. Эта реакция служит не только для разрушения аминокислот, но и для их биосинтеза. Например, аспартат-α-кетоглутараттрансаминаза катализирует взаимопревра-щение аспарагиновой и α-кетоглутаровой кислот в кетоянтарную и глутаминовую кислоты. Такое превращение помимо фермента требует участия пиридоксальфосфата, роль которого заключается в окислении исходной молекулы аминокислоты, переносе молекулы аммиака к кетокислоте и последующем ее восстановлении. Отметим, что в этом процессе пиридоксальфосфат (RCHO) вначале превращается в пиридоксаминофосфат (RCH2NH2), а затем вновь регенерируется.
HO2CCH2C CO2H |
RCHO |
HO2CCH2C CO2H |
|
|
CHO |
|||||
|
NH2 |
|
N |
|
HO |
CH2OPO3H2 |
||||
|
|
|
|
|
|
|
|
|||
аспарагиновая |
|
|
|
|
CHR |
|
|
|
||
|
|
|
|
|
|
|
N |
|||
кислота |
|
|
|
|
|
|
|
пиридоксальфосфат (RCHO) |
||
HO CCH C |
CO H |
|
H2O |
|
HO CCH C |
CO H |
|
|||
2 |
2 |
2 |
|
|
|
|
2 |
2 |
2 |
|
|
N |
CH2R |
- RCH2NH2 |
|
|
|
O |
|
||
|
|
|
|
|
|
кетоянтарная кислота |
|
|||
|
|
|
|
|
|
|
|
|||
15