Материал: Резников В.А., Штейнгарц В.Д. Аминокислоты PDF
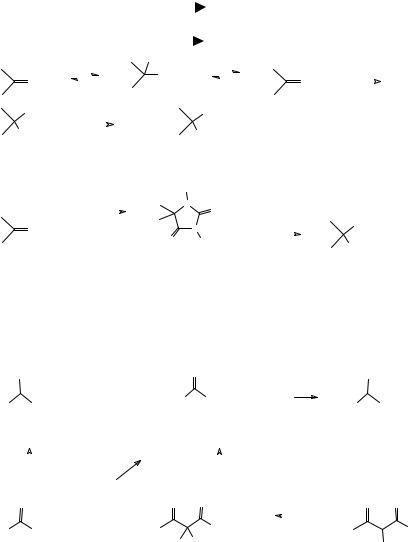
Историческое значение имеет синтез аминокислот по методу Штрекера, основанному на взаимодействии карбонильных соединений с цианистым натрием и хлоридом аммония. При взаимодействии неорганических компонент образуется цианистый водород и аммиак. Первая стадия реакции – образование имина в результате реакции присоединения-отщепления аммиака с карбонильным соединением. Цианистый водород присоединяется по связи C=N с образованием геминального аминонитрила (α-аминонитрила), последующий гидролиз нитрильной группы завершается образованием аминокислоты.
|
NH4Cl + NaCN |
|
|
|
|
|
|
NH4CN + NaCl |
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
NH4CN |
|
|
|
|
NH3 |
+ HCN |
|
|
|
|||||||
|
|
|
|
|
|
|
|
||||||||||||||
|
±NH3 |
NH2 |
|
|
|
|
- H O |
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
OH |
|
+ 2 |
|
|
|
HCN |
|||||||
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
H O+ |
|
|
|
|
|
|
CO2H |
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
CN |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
||
α-амино- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
нитрил |
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NaCN |
|
|
|
|
N |
|
|
O |
|
|
|
|
|
|
||||
|
|
|
(NH4)2CO3 |
|
|
|
|
|
|
|
H O+ |
|
CO H |
||||||||
O |
|
|
|
|
|
|
N |
|
|
||||||||||||
|
|
|
|
|
|
|
O |
|
3 |
|
2 |
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
H |
|
или OH- |
|
NH2 |
||||||
|
|
|
|
|
|
|
|
гидантоин |
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
Интересной модификацией этого метода является взаимодействие карбонильных соединений с цианистым натрием и карбонатом аммония в качестве донора аммиака. При этом образуется гетероциклическое соединение, которое называется гидантоином. Гидролиз гидантоина в кислой или щелочной среде легко приводит к аминокислоте с высоким выходом.
NH2 |
|
NX |
|
|
NH2 |
||
|
|
|
[H] |
||||
|
|
R |
CO2H |
|
|||
R |
CO2H |
|
R |
CO2H |
|||
X = OH, NHR1 |
|
||||||
|
|
|
|
|
|||
|
NH3 |
XNH2 |
|
1. OH- |
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
||
|
H2 |
|
|
+ |
|
|
|
|
|
|
|
2. H |
|
|
|
O |
|
O |
O |
PhN2+ Cl- |
O O |
||
R |
CO2H |
|
OEt |
|
|
OEt |
|
R |
N=NPh |
|
|
R |
|||
|
|
|
|
||||
α-Аминокислоты могут быть получены из кетокислот или их производных – гидразонов и оксимов. Для получения аминокислот из кетокислот используют реакцию восстановительного аминирования. Оксимы и гидразоны кетокислот образуют аминокислоты при восстановлении.
Фенилгидразоны α-кетокислот могут быть получены из ацетоуксусных эфиров при взаимодействии с солями фенилдиазония. Последующее расщепление образующихся азосоединений в щелочной среде и нейтрализация приводят к фенилгидразонам. Предложите механизм этого превращения.
Для синтеза α-аминокислот используется также малоновый эфир. По одному из методов на замещенный малоновый эфир действуют одним молем гидразина. При этом образуется моногидразид малоновой кислоты. Это соединение действием азотистой кислоты превращают в азид, который далее при нагревании претерпевает перегруппировку Курциуса с образованием эфира α-аминокислоты.
6
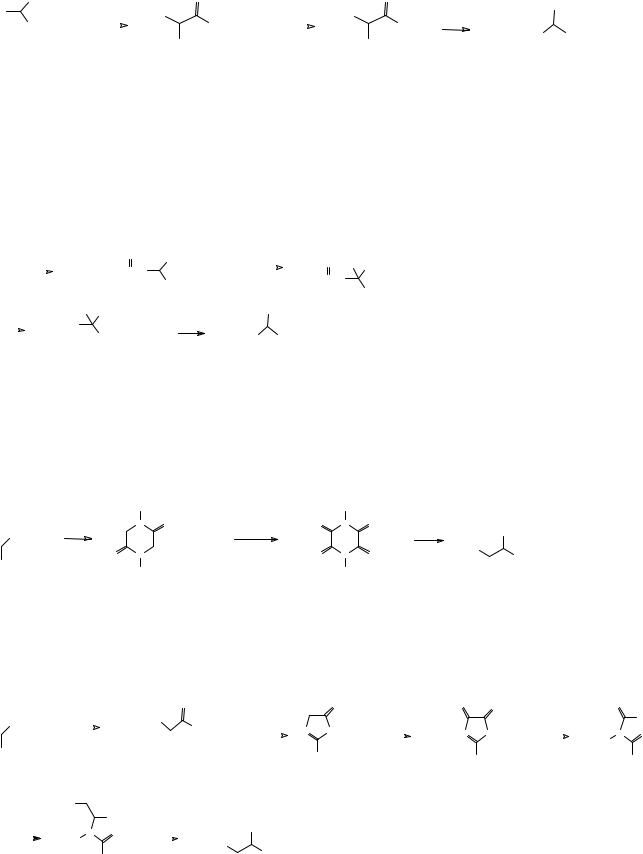
R |
CO2Et |
|
O |
|
NaNO2 |
|
O |
NH2 |
|
|
N2H4 |
R |
|
|
R |
|
|||
|
CO2Et |
|
|
|
NHNH2 |
|
|
N3 |
t |
|
|
|
|
|
|
||||
|
|
|
|
CO2Et |
|
HCl |
|
CO2Et |
R CO2H |
|
|
|
|
|
|
|
|
||
Другой возможностью использования малонового эфира в синтезе α-аминокислот является реакция нитрозирования, которая приводит к оксиму. Оксимная группа может быть восстановлена в аминогруппу с сохранением сложноэфирных групп водородом на никелевом катализаторе. Полученный эфир аминомалоновой кислоты ацилируют по аминогруппе уксусным ангидридом. Образующееся ацетамидное производное способно депротони-роваться под действием металлического натрия с образованием натриевой соли, которая реагирует с галоидными алкилами. Таким образом, получается замещенный ацетамидомалоновый эфир. Последующий гидролиз ацетамидной и сложноэфирных групп дает аминомалоновую кислоту, которая декарбоксилируется при нагревании как и всякая β-дикислота.
(CH3CO)2O |
|
O |
CO2Et |
|
1. Na |
|
O R CO2Et |
||
|
H CCHN |
|
|
||||||
|
|
2. RBr |
|||||||
|
|
|
|
3 |
CO Et |
|
H3CCHN |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
CO2Et |
|
|
|
|
|
|
|
|
|
|
|
H O+ |
H2N |
R CO2H |
t |
|
NH2 |
|
||
|
3 |
|
CO2H |
R CO2H |
|
||||
|
|
|
|||||||
|
|
|
|
|
|
||||
Существуют методы синтеза различных аминокислот исходя из простейшей – аминоуксусной кислоты (глицина). Один из них это превращение глицина в дикетопиперазин (подробнее об этом изложено в разделе, посвященном химическим свойствам аминокислот), который способен вступать во взаимодействие с ароматическими альдегидами с образованием продуктов конденсации кротонового типа. Последующее расщепление полученного продукта конденсации действием йодистоводородной кислоты в присутствии фосфора с высоким выходом приводит к другой аминокислоте. Ниже приведена схема синтеза фенилаланина этим методом.
|
|
H |
|
H |
|
|
|
|
t |
N O |
PhCH |
N |
O |
|
|
NH2 |
2 PhCHO |
|
|
|
HI, P |
NH2 |
|
|
|
O N |
O |
N |
CHPh |
H2O |
Ph |
CO2H |
|
|
CO2H |
||||
|
H |
|
H |
|
|
фенилаланин |
|
глицин |
|
дикетопиперазин |
|
|
|
|
|
|
|
|
|
|
|
Азлактонный метод синтеза аминокислот заключается в конденсации гиппуровой кислоты с альдегидами в уксусном ангидриде. Исходное соединение – гиппуровая кислота - легко может быть получено при взаимодействии глицина с хлористым бензоилом.
|
|
|
|
|
|
|
|
O |
|
|
O |
|
RCH |
O |
|
RCH |
|
|
NH2 |
PhCOCl |
|
PhCOHN |
|
(CH3CO)2O |
|
RCHO |
|
|
H2O |
CO2H |
|||||
|
|
|
|
|
|
|
|
OH |
|
N O |
N |
O |
N O |
||||
|
|
|
|
|
|
гиппуровая |
|
|
|
|
|
H |
|||||
CO2H |
|
|
|
|
Ph |
|
|
|
Na2CO3 |
|
|||||||
|
|
кислота |
|
|
|
|
Ph |
|
|
Ph |
|||||||
|
|
|
|
|
|
|
|
азлактон |
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
|
|
|
|
|
|
|
|
|
|
|
|
Na/Hg |
|
CO2H |
|
NH2 |
|
|
|
|
|
|
|
||||||
N |
O |
|
H O+ |
|
|
|
|
|
|
|
|
||||||
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
H |
|
|
|
|
R |
|
|
|
|
|
|
|
|
|
H2O |
Ph |
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
CO2H |
|
|
|
|
|
|
|
|
Вначале гиппуровая кислота под действием уксусного ангидрида превращается в азлактон. В составе молекулы этого соединения содержится активная метиленовая группа, вследствие чего оно
7

способно вступать в реакцию конденсации с альдегидами (предложите механизм этой реакции; примечание: вспомните конденсацию Перкина). Продукт конденсации восстанавливают амальгамой натрия и получают N-безоильное производное другой аминокислоты, которое превращается в аминокислоту в результате кислотно-катализируемого гидролиза.
В промышленном масштабе рацемические аминокислоты обычно не синтезируют химическим путем, а используют микробиологические технологии с применением генной инженерии и выделяют аминокислоты из белковых молекул, продуцируемых специально выведенными микроорганизмами. Исключение составляют лишь несколько аминокислот, которые производятся в промышленности химическим путем. Например, десятками тысяч тонн в год производится L-глутамат натрия – соль глутаминовой кислоты. Синтез осуществляется по следующей схеме:
NC |
CO, H2 (водяной газ) |
|
H |
1. NaCN + NH4Cl |
HO2C |
CO2Na |
|
|
|
|
|||||
|
|
NC |
O |
|
2.H3O+ |
|
NH2 |
|
|
|
|
3. NaOH |
глутамат натрия |
||
|
|
|
|
|
|
||
Один из перспективных методов синтеза лизина основан на использовании в качестве исходного соединения доступного и дешевого циклогексена. Синтез проводят по следующей схеме:
|
NO |
NOH |
HO C |
(CH ) |
-NH |
|
|
|
2 |
2 4 |
2 |
NaNO2 |
NH3 |
|
H3O+ |
NH |
|
HCl |
Cl |
NH2 |
|
2 |
|
лизин |
|
||||
|
|
|
|
||
По механизму реакции последняя стадия процесса сходна с перегруппировкой Бекмана. Предложите ее механизм.
Интересно отметить, что при пропускании электрического разряда через смесь метана, аммиака, воды и водорода наряду с другими продуктами образуются различные аминокислоты. Поскольку полагают, что аналогичные условия могли существовать на древней Земле, то нельзя исключить, что именно таким путем на нашей планете возникли первые аминокислоты – основа будущей белковой жизни.
СИНТЕЗ ДРУГИХ АЛИФАТИЧЕСКИХ АМИНОКИСЛОТ
В этом разделе рассматриваются методы синтеза аминокислот с иным, нежели в α-аминокислотах расположением аминогруппы. β-Аминокислоты синтезируют главным образом из α,β-ненасыщенных карбоновых кислот при взаимодействии их с аммиаком. Модификацией этого метода является взаимодействие малоновой кислоты с альдегидами и аммиаком, которое можно рассматривать как последовательное образование α,β-ненасыщенной дикислоты, затем присоединение аммиака по связи С=С и декарбоксилирование, завершающееся образованием аминокислоты.
OH |
|
NH3 |
H2N |
O |
- |
|
|
|
|
|
|
O |
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- |
|
|
|
- |
|
NH3 |
R |
CO2- |
|
H2N |
O- |
|
|
|
|
|
|
|
|
|
|||
CO2 |
+ RCHO |
R |
CO2 |
|
|
H2N |
CO2- |
- CO2 |
|
R O |
|
|
|
|
|||||||||
- |
|
CO- |
|
|
|
|
|
|
|
||
CO2 |
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Вместо аммиака в реакции присоединения к α,β-непредельным кислотам или их производным можно использовать фталимид в присутствии каталитических количеств основания. При этом образуется фталимидное производное, которое легко может быть гидролизовано в β-аминокислоту.
8
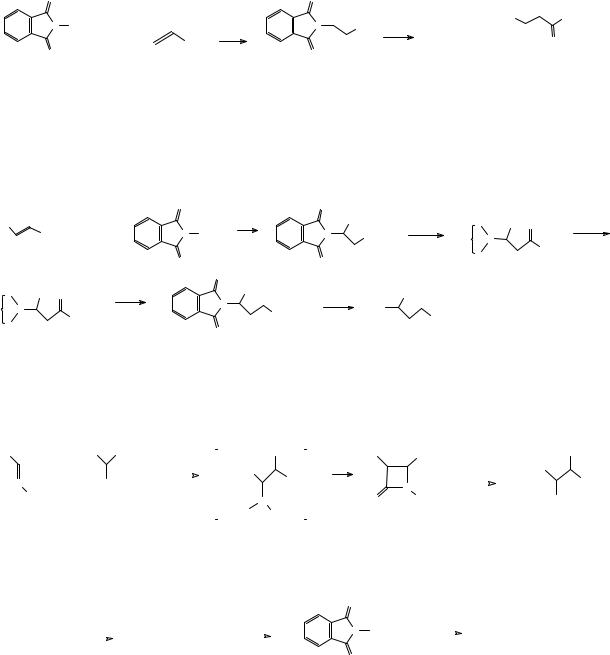
O |
|
O |
|
|
|
N H |
+ |
N |
CN H O+ |
H2N |
OH |
|
CN |
3 |
|
O |
|
|
|
|
|
||
O |
|
|
|
|
|
|
O |
|
|
|
Кроме того, фталимидное производное может быть использовано для синтеза других аминокислот с большим расстоянием между аминогруппой и карбоксильной группой гомологизацией по реакции Арндта-Айстерта. Это превращение можно, разумеется, осуществлять многократно, однако для синтеза соединений с большим удалением аминогруппы и карбоксильной группы лучше использовать другие методы.
|
|
O |
|
|
O |
|
|
|
|
R |
+ |
N |
H |
|
N |
R |
1. H3O+ |
R O |
CH2N2 |
CO2CH3 |
|
|
CO2CH3 |
2. PCl5 |
N |
|
|||
|
|
|
|
|
Cl |
||||
|
|
O |
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
O |
|
|
|
|
|
|
R O |
|
Ag O |
N |
R |
H3O |
+ |
R |
|
|
N |
|
2 |
|
H N |
|
|
|
||
|
EtOH |
|
CO2Et |
|
CO |
H |
|
||
CHN |
2 |
|
|
2 |
|
||||
|
|
O |
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
β-Аминокислоты могут быть также получены по реакции, аналогичной реакции Фаворского – взаимодействием иминов с эфирами α-бромкарбоновых кислот и цинком. Образующийся на первой стадии аддукт самопроизвольно циклизуется, давая β-лактам, гидролиз которого в щелочной или кислой среде завершается образованием β-аминокислоты.
R |
|
Br |
CO2Et |
|
|
|
CO2Et |
|
R" |
R |
R" |
|||||||
|
|
|
|
|||||||||||||||
|
+ |
|
|
|
|
Zn |
|
|
R |
|
R" |
|
|
|
|
H3O+ |
R'HN |
|
N |
|
R" |
|
|
|
|
|
N |
CO H |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
R' |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
BrZn |
N |
|
O |
R' |
R |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
R' |
|
β-лактам |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
γ-Аминокислоты, например γ-аминомасляную кислоту, синтезируют из 1,3-дигалогенпропанов по |
|||||||||||||||||
следующей схеме: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
KCN |
|
|
|
фталимид |
|
N (CH2)3CN |
|
H O+ |
H2N(CH2)3COOH |
||||||
Cl(CH2)3Br |
|
Cl(CH2)3CN |
калия |
|
|
|
3 |
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
O
Предложите метод синтеза 1-бром-3-хлорпропана.
Иной метод синтеза γ-аминомасляной кислоты – гидролиз γ-бутиролактама, который может быть получен либо взаимодействием γ-бутиролактона с аммиаком, либо электрохимическим восстановлением сукцинимида.
9
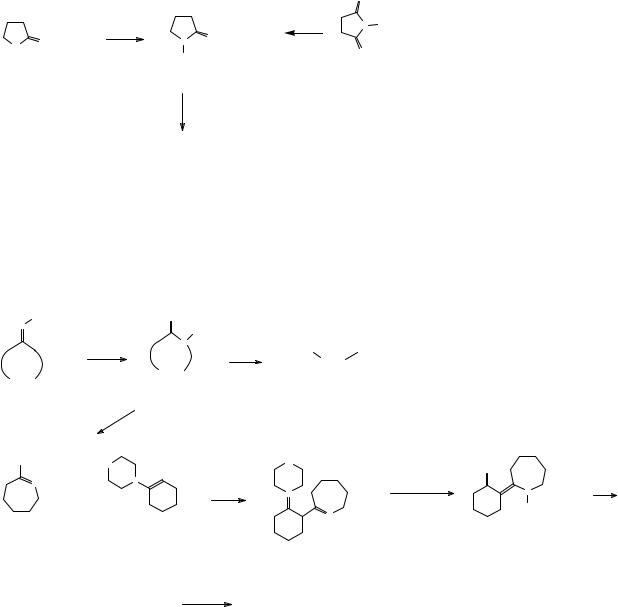
|
|
|
|
|
O |
|
|
[NH3] |
|
O |
N H |
|
O |
N |
|
||
O |
|
|
|||
|
|
O |
|||
|
|
H |
|
||
|
|
|
|
||
|
|
|
|
сукцинимид |
|
бутиролактон |
|
бутиролактам |
|||
|
|
||||
|
|
|
H O+ |
|
|
|
|
|
|
3 |
|
H2N(CH2)3COOH
γ-аминомасляная кислота
Одним из общих методов синтеза ω-аминокислот, аминогруппа в которых находится на конце цепи, заключается в гидролизе соответствующих лактамов, которые получают по бекмановской перегруппировке циклических кетонов. Таким способом в промышленности из оксима циклогексанона получают капролактам - исходное соединение в синтезе капрона и ε-аминокапроновую кислоту (n = 5).
OH |
|
O |
|
|
|
|
N |
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
H2SO4 |
N |
|
NH2 |
|
|
|
H3O+ |
HOOC |
|
|
||
|
|
(CH2)n |
|
(CH2)n |
|
|
(CH2)n |
|
|
|
|
|
|
|
|
ω-аминокислота |
|
|
||
|
PCl5 |
|
|
|
||
|
|
|
|
|
|
|
|
(n =5) |
|
|
|
|
|
Cl |
O |
|
O |
|
O |
|
|
N |
|
|
AcOH (разб.) |
OH- |
|
N |
|
+ |
N |
|||
|
+ |
|
N |
|
|
|
|
N |
H |
|
енаминокетон |
|
имидоил |
|
|
иминиевая соль |
|
|
-хлорид |
|
|
|
|
1. N2H4
H2N(CH2)5CO(CH2)4CO2H 2. OH-, t H2N(CH2)11CO2H
3. H+
Для синтеза аминокислот с большим расстоянием между карбоксильной и аминогруппой в качестве исходных соединений используются лактамы. Выше на примере капролактама приведена реализуемая при этом последовательность реакций. При взаимодействии капролактама с пентахлоридом фосфора образуется имидоилхлорид – циклический аналог хлорангидрида карбоновой кислоты, соответствующий тому, что атом кислорода заменен атомом азота. Обладая реакционной способностью, близкой к реакционной способности хлорангидридов, соединения этого типа реагируют с енаминами с образованием иминиевой соли, гидролиз которой разбавленной уксусной кислотой приводит к енаминокетону. Енаминокетоны – соединения близкие по реакционной способности к β-дикетонам и поэтому, способные при взаимодействии с концентрированными щелочами вступать в обратную реакцию Кляйзена, в результате чего в данном случае углеводородная цепь аминокислоты удлиняется на шесть углеродных атомов, которые ранее находились в циклогексановом кольце используемого енамина.
СВОЙСТВА АМИНОКИСЛОТ.
СТЕРЕОХИМИЯ
10