Материал: Резников В.А., Штейнгарц В.Д. Аминокислоты PDF
O
H2N CH C OH
CH2
N
NH
hƒK!=……/å ãë="/ ,ƒ *3!“= œn!ã=…,÷å“*= .,ì, B
АМИНОКИСЛОТЫ
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
||
H2N |
|
|
CH |
|
|
C |
|
OH |
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
H2N |
|
|
CH |
|
|
C |
|
OH |
|
|
|
|
CH2 |
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HN
OH
lhmhqŠepqŠbn nap`gnb`mh“ pnqqhiqjni tedep`0hh
НОВОСИБИРСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ ФАКУЛЬТЕТ ЕСТЕСТВЕННЫХ НАУК
hƒK!=……/å ãë="/ ,ƒ *3!ñ= œn!ã=…,÷åñ*=ÿ .,ì,ÿB
`ì,…%*,ñë%2/
Пособие для студентов специализаций “ХИМИЯ” и “ЭКОЛОГИЯ”
III и IV семестры
Новосибирск
1999
Составители:
Проф. В. А. Резников Проф. В. Д. Штейнгарц
Рецензент канд. хим. наук К. Ю. Колтунов
Пособие представляет собой часть курса лекций “Органическая химия”, читаемого студентам второго курса специализаций “химия” и “экология”, рекомендуется также студентам отделения “биология и медбиология” и другим студентам, изучающим органическую химию.
Новосибирский государственный университет, 1999
2

СОДЕРЖАНИЕ
α-Аминокислоты |
4 |
Синтез алифатических аминокислот. Синтез α-аминокислот |
7 |
Синтез других алифатических аминокислот |
16 |
Свойства аминокислот. |
|
Стереохимия |
21 |
Кислотно-основные свойства |
22 |
Реакции аминокислот |
25 |
Реакции аминокислот in vivo |
30 |
Ароматические аминокислоты |
34 |
Пептиды и белки |
38 |
Синтез пептидов |
39 |
Анализ пептидов |
46 |
Пространственное строение белков |
49 |
АМИНОКИСЛОТЫ
Аминокислоты, как видно из названия, – это любые органические кислоты, в состав молекулы которых входит аминогруппа, хотя чаще всего под этим названием подразумевают α-аминокислоты вследствие их исключительного значения как составляющей части биополимеров – белков. Белки имеют очень важное и разнообразное значение в функционировании живого организма – они являются питательными веществами, регулируют обмен веществ, являются основой мышечной ткани, участвуют в передаче генетической информации и т. д.
α-Аминокислоты
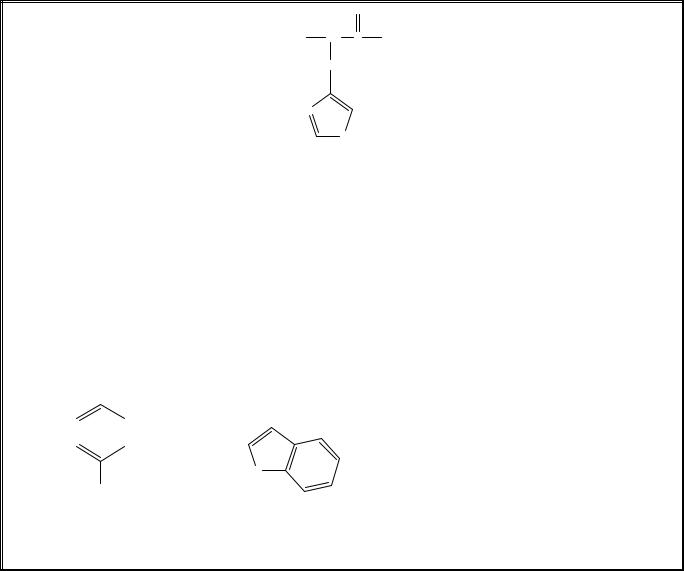
В природе встречается более 70 аминокислот, почти все они за исключением пролина и оксипролина имеют структуру типа RCH(NH2)CO2H. Структурные формулы и названия наиболее распространенных α-аминокислот приведены в таблице.
Название |
Структурная |
Изоэлек- |
|
Название |
Структурная |
Изоэлек- |
||
(сокращение) |
формула |
трическая |
|
(сокращение) |
формула |
трическая |
||
|
|
|
точка (pI) |
|
|
|
|
точка (pI) |
Глицин (gly) |
H2NCH2CO2H |
5,97 |
|
Лейцин (leu) |
H C |
CO2H |
5,98 |
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
CH3 NH2 |
|
Аланин (ala) |
H3C |
CO2H |
6,02 |
|
Изолейцин (ile) |
H3C |
CH3 |
6,02 |
|
|
NH2 |
|
|
|
CO H |
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
Валин (val) |
H3C |
CO2H |
5,97 |
|
Пролин (pro) |
|
|
6,10 |
|
H3C |
|
|
|
N |
CO2H |
|
|
|
|
NH2 |
|
|
|
H |
|
|
3
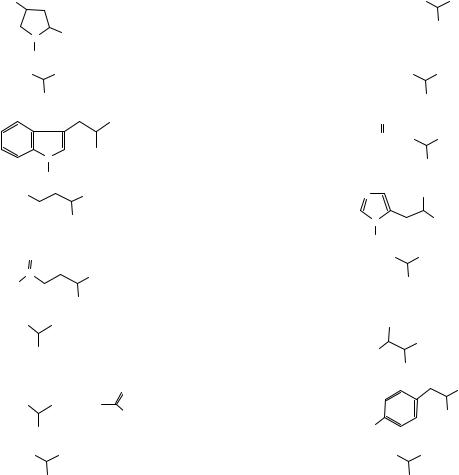
Название |
Структурная |
Изоэлек- |
|
Название |
|
Структурная |
|
Изоэлек- |
|||
(сокращение) |
формула |
|
трическая |
|
(сокращение) |
формула |
|
|
трическая |
||
|
|
|
|
точка (pI) |
|
|
|
|
|
|
точка (pI) |
Оксипролин |
HO |
|
|
5,78 |
|
Метионин (met) |
H3CSH2CH2C |
CO2H |
5,75 |
||
(hypro) |
|
|
|
|
|
|
|
|
NH2 |
|
|
|
N |
|
CO2H |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
||
Фенилаланин |
H |
|
|
5,88 |
|
Аспарагиновая |
|
|
|
2,87 |
|
PhH2C |
|
CO2H |
|
HO2CCH2C |
CO2H |
||||||
(phe) |
|
NH2 |
|
|
кислота (asp) |
|
NH2 |
|
|
||
|
|
|
|
|
|
|
|
|
|||
Триптофан |
|
|
CO |
5,88 |
|
Аспарагин |
|
O |
|
|
5,41 |
(try) |
|
|
NH2 |
|
|
(asp(NH2)) |
|
H2NCCH2C |
CO2H |
|
|
|
|
N |
|
|
|
|
|
NH2 |
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
Глутаминовая |
|
|
3,22 |
|
Гистидин (his) |
|
|
|
7,58 |
||
HO2C |
|
CO2H |
|
N |
NH2 |
|
|||||
кислота(glu) |
|
|
NH2 |
|
|
|
|
N |
CO2H |
|
|
|
|
|
|
|
|
|
|
||||
Глутамин |
|
|
|
5,65 |
|
Серин (ser) |
|
H |
|
|
5,68 |
O |
|
CO2H |
|
|
HOH2C |
CO2H |
|
||||
(gluNH2) |
C |
|
|
|
|
|
NH2 |
|
|
||
|
H2N |
|
NH2 |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
Лизин (lys) |
HO2C |
(CH2)4-NH2 |
9,74 |
|
Треонин (thr) |
OH |
CO2H |
|
6,53 |
||
|
NH2 |
|
|
|
|
|
H3C |
|
|
||
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
NH2 |
|
|
|
Аргинин |
HO2C |
(CH2)4-NH |
N10,76 |
|
Тирозин (tyr) |
|
|
CO2 |
5,65 |
||
(arg) |
|
|
|
|
|
NH2 |
|
||||
|
NH2 |
|
|
|
|
|
HO |
|
|||
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
||
Цистеин |
HSH2C |
|
CO2H |
5,02 |
|
Цистин |
(cyS- |
2(-SH2C |
CO2H |
|
5,06 |
(cysH) |
|
NH2 |
|
|
Scy) |
|
NH2 |
|
|
||
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
Незаменимыми называются α-аминокислоты, которые не могут быть синтезированы организмом из веществ, поступающих с пищей в количествах, необходимых для поддержания жизнедеятельности. К незаменимым для человека аминокислотам относятся лейцин, изолейцин, лизин, метионин, фенилаланин, треонин, триптофан и валин. Кроме того, бывают заболевания, при которых организм не способен вырабатывать еще какие-либо аминокислоты, в результате чего они становятся индивидуально незаменимыми. Примером является фенилкетонурия – генетическое заболевание, приводящее, в частности, к нарушению умственной деятельности и связанное с нарушением обмена веществ. Люди, страдающие этим заболеванием, нуждаются в тирозине, который не вырабатывается их организмом.
СИНТЕЗ АЛИФАТИЧЕСКИХ АМИНОКИСЛОТ
Синтез α-аминокислот
Почти все природные α-аминокислоты имеют в составе молекулы асимметрический атом углерода, связанный с аминогруппой. Учитывая, что в их синтезе участвуют ферменты – сложные оптически активные органические соединения, природные аминокислоты также являются оптически активными и относятся к L-ряду. Более того, организм может оперировать только тем оптическим изомером, который ему характерен, противоположный энантиомер в обмене веществ не участвует. Учитывая сложность синтеза оптически активных соединений in vitro (“в пробирке”), в лабораторных условиях и вообще
4
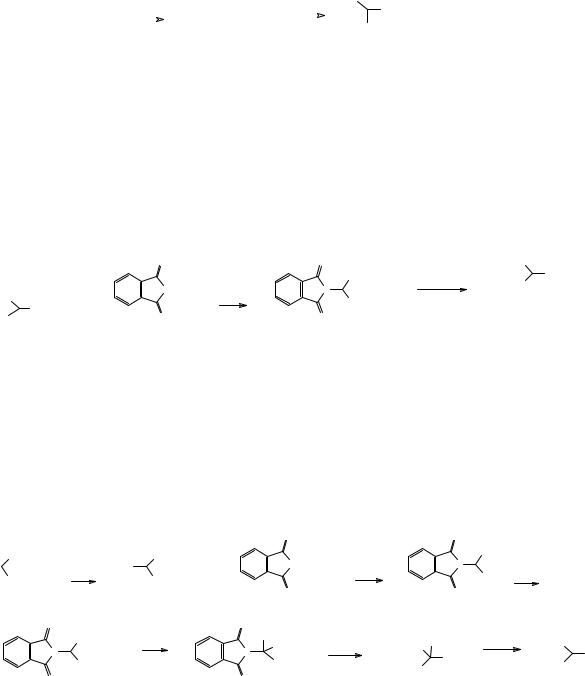
химическим путем синтезируют рацемические аминокислоты, которые далее могут быть разделены на энантиомеры уже известными вам методами. Сначала мы рассмотрим именно эти методы синтеза.
В качестве исходных соединений в синтезе α-аминокислот могут быть использованы α- галоидкарбоновые кислоты, синтез которых проводят по методу Гелля-Фольгарда-Зелинского действием брома в присутствии красного фосфора или каталитического количества пиридина на карбоновые кислоты. При взаимодействии α-бромкарбоновых кислот с избытком аммиака образуются соответствующие аминокислоты.
|
|
|
NH3 |
R |
RCH2CO2H + Br2 |
P |
RCHBrCO2H |
CO H |
|
|
2 |
|||
|
|
|
|
NH2 |
Почему в синтезе α-аминокислот из галоидкарбоновых кислот необходимо использовать
избыток аммиака? К какому типу относится эта реакция, какие побочные продукты могут в ней образовываться?
Как вы помните, аммонолиз алкилгалогенидов является не лучшим методом синтеза аминов. Для селективного синтеза первичных аминов предпочтительным является метод Габриэля, заключающийся во взаимодействии алкилгалогенидов c фталимидом калия и последующем гидролизе фталимидного производного. Этот метод неприменим к галоидкарбоновым кислотам (почему?), однако в реакцию можно вводить α-галоидзамещенные эфиры карбоновых кислот или галоидзамещенные малоновые эфиры.
|
|
O |
|
|
O |
|
R |
NH3+ Cl- |
|
|
|
- |
K |
+ |
R |
HCl / H2O |
HO C |
|
|
Br |
|
N |
|
N |
|
2 |
|
|
|
CO2Et |
+ |
|
|
CO2Et |
|
хлоргидрат |
α- |
||
|
|
|
|
||||||
R |
O |
|
|
O |
|
||||
|
|
|
|
аминокислоты |
|
||||
|
|
|
|
|
|
|
|
||
Броммалоновые эфиры получают бромированием малоновых эфиров бромом в неполярном органическом растворителе. При взаимодействии броммалонового эфира с фталимидом калия образуется фталимидное производное. При этом один из “кислых” атомов водорода малонового эфира остается незамещенным, и, следовательно, полученное фталимидное производное является СН-кислотой, которая образует анион при действии сильного основания, например этилата натрия. Алкилирование этого аниона приводит к замещенному малоновому эфиру А, кислотный гидролиз которого затрагивает как фталимидную, так и обе сложноэфирные группы, и завершается образованием аминодикислоты. Являясь производным малоновой кислоты, это соединение легко декарбоксилируется при нагревании с образованием аминокислоты в виде хлоргидрата.
|
|
|
|
|
|
|
|
O |
|
|
|
|
O |
|
|
|
|
CO2Et |
|
|
|
CO2Et |
|
- |
K |
+ |
|
|
|
CO2E |
|
|
|
||
|
|
|
Br2 |
Br |
|
|
+ |
N |
|
|
|
|
N |
OEt- |
|
|
|
CO |
Et |
|
|
CO |
Et |
|
|
|
|
|
|
CO2E |
|
|
|||
2 |
|
|
CCl4 |
|
2 |
|
|
O |
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
O |
|
|
|
|
|
O |
R |
|
|
|
|
|
|
|
|
|
|
|
|
CO2Et |
RBr |
|
|
|
|
H O+ |
HO C R |
|
t |
|
R |
|
||
|
N |
- |
|
N |
CO Et |
|
|
|
|
+ |
|||||||
|
|
|
|
|
|
2 |
|
|
3 |
2 |
NH |
+ |
|
|
NH3 |
||
|
|
CO |
Et |
|
|
CO2Et |
|
|
t |
HO |
C |
||||||
|
|
|
|
|
|
|
|
HO2C |
|
3 |
|
||||||
|
O |
|
2 |
|
|
O |
|
|
|
|
|
|
2 |
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
А
При использовании броммалонового эфира может быть синтезирован фенилаланин с выходом 60%. Напишите последовательность необходимых для этого реакций. Предложите механизм каждой из стадий реакции.
5