Материал: Растворимость малорастворимых соединений
Нетрудно
заметить, что
![]()
![]() (4)
(4)
Точно также, как мы рассчитывали долю определенной ионной формы при каком-то значении рН раствора при учете кислотно-основного равновесия, так и тут необходимо рассчитать долю свободных ионов металла (незакомплексованных), находящихся не в форме комплекса, а в форме просто ионов при той концентрации лиганда, которая наблюдается в растворе. То есть если раньше мы задавали рН и определяли разные доли, то при учете комплексообразования, надо задавать концентрацию лиганда и определять разные доли комплексов и свободных ионов.
УМБ по катиону металла будет следующим:
![]()
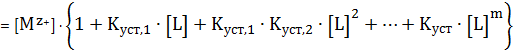
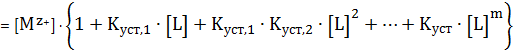 (5)
(5)
В
произведении растворимости учитывается концентрация ионов металла
![]()
![]() (6)
(6)
Доля ионов металла рассчитывается, как и в распределительных диаграммах в кислотно-основных равновесиях:
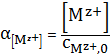
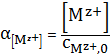 (7)
(7)
Процесс растворения осадка передается уравнением:
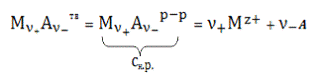 (8)
(8)
Закон равновесия
![]()
![]() (9)
(9)
Растворимость
найдется из выражения:
![]()
![]() (10)
(10)
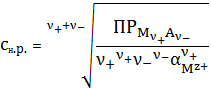
5.3 Расчет растворимости осадков с учетом одновременного влияния различных факторов
Этот
вопрос является довольно сложным и требует глубокого понимания процессов,
происходящих в водных растворах малорастворимых соединений. Допустим, что
осадок![]()
![]() образован анионом слабой кислоты
образован анионом слабой кислоты ![]()
![]() , а
катион осадка образует комплексные ионы как с посторонним реагентом L,
так и с осадителем A. Тогда растворимость осадка будет определяться
суммарным содержанием всех равновесных частиц, содержащих катион осадка [2]:
, а
катион осадка образует комплексные ионы как с посторонним реагентом L,
так и с осадителем A. Тогда растворимость осадка будет определяться
суммарным содержанием всех равновесных частиц, содержащих катион осадка [2]:
![]()
![]() (1)
(1)
Выразим равновесные концентрации комплексных ионов через их константы
устойчивости, а концентрацию ионов металла через произведение растворимости,
получим:
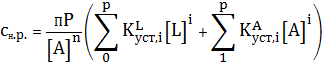
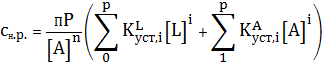 (2)
(2)
.4 Расчет минимальной растворимости осадков
Уменьшение растворимости осадков, которые не растворяются в избытке
осадителя и в составе которых только один из ионов может участвовать в
сопряженных протолитических равновесиях, обеспечивается введением в насыщенный
раствор соответствующего избытка одноименного иона. Растворимость же осадков
гидроксидов металлов и малорастворимых соединений, у которых катионы и анионы
могут одновременно участвовать в сопряженных протолитических реакциях, зависит
от кислотности раствора и достигает минимального значения при определенном рН.
Наименьшая растворимость осадков в избытке осадителя - комплексанта также
наблюдается при строго определенной его концентрации. Создание условий
,обеспечивающих наименьшую растворимость таких осадков, является важным для
практических экологических и аналитических целей.
.4.1 Растворимость осадка, образованного анионом слабой кислоты и катионом слабого основания
Иногда малорастворимая соль состоит из аниона слабой кислоты и катиона слабого основания. Если константы протонирования аниона осадка и гидроксообразования катиона резко отличаются между собой, то протолиз осадка практически определяется протолизом того иона, который образует наиболее прочные соединения.
Растворимость
осадков, катионы и анионы которых одновременно участвуют в сопряженных
протолитических реакциях, зависит от рН насыщенного раствора. В кислых
растворах с уменьшением рН увеличивается протонирование аниона и растворимость
осадка возрастает, в щелочных растворах с повышением рН растворимость осадков
также увеличивается вследствие образования растворимых гидроксокомплексов.
Наименьшая растворимость осадка наблюдается при таком значении рН, при котором,
влияние депротонирования аниона уравновешивается влиянием
гидроксокомплексообразования катиона осадка. Если оценивать растворимость
осадка, привлекая долевые концентрации ![]()
![]() и
и ![]()
![]() , то
очевидно, что наименьшая растворимость осадка будет наблюдаться при том рН, при
котором будет наибольшим произведение долевых концентраций аниона и катиона.
, то
очевидно, что наименьшая растворимость осадка будет наблюдаться при том рН, при
котором будет наибольшим произведение долевых концентраций аниона и катиона.
Если растворимость осадка представить в виде функции зависимой от рН, то на зависимости растворимости этого малорастворимого соединения от величины рН появляется минимум.
5.4.2 Влияние комплексообразования на растворимость солей
Растворимость многих солей в присутствии общего иона значительно выше,
чем это следует из произведения растворимости. Это обычно обусловлено
образованием комплексов между анионом и катионом соли и обязательно должно быть
учтено в случае, если концентрации аниона высокие.
Практическая часть
1.
Ag2SO4тв, H2O, ![]()
![]() =1, 24∙10-5
=1, 24∙10-5
Ag2SO4тв = 2Ag+ + ![]()
![]()
C 2Ag+ =2 SI
![]()
![]() = SI
= SI
ПP Ag2SO4=1,24∙10-5
ПP Ag2SO4=
![]()
![]() ∙
∙
![]()
![]() =4
SI3
=4
SI3
SI = ![]()
![]() =
0,677(моль/л)
=
0,677(моль/л)
. Ag2SO4тв,
KBr, H2O, ПPAgBr=1,24∙10-5=
2Ag+ + ![]()
![]() -SII
-SII
KBr = K+ + Br- x2 = C KBr,0
C Ag+ = 2SII
![]()
![]() = SII
= SII
C K+ = x2 = C KBr,0
C Br-= x2 = C KBr,0
ПPAg2SO4= ![]()
![]() ∙ C Br- ∙ г ±2= 4SII3∙
г ±3
∙ C Br- ∙ г ±2= 4SII3∙
г ±3
SII = ![]()
![]()
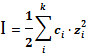
![]()
Пример
расчета: (CNaNO3 = 0,0001 моль/л)
SII =
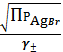
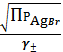 = 7,37
= 7,37![]()
![]() (моль/л)
(моль/л)
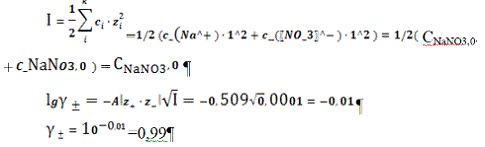
Таблица
1
CNaNO3,моль/л
I,моль/м3
lgг ±
г ±
SII, моль/л
0,0001
0,0001
-0,01
0,99
7,37 0,0005
0,0005
-0,01
0,97
7,47 0,005
0,005
-0,04
0,92
7,91 0,001
0,001
-0,02
0,96
7,55 0,01
0,01
-0,05
0,90
8,10 0,05
0,05
-0,09
0,81
9,02 0,1
0,1
-0,11
0,77
9,42 0,5
0,5
-0,16
0,69
1,05 1
1
-0,15
0,70
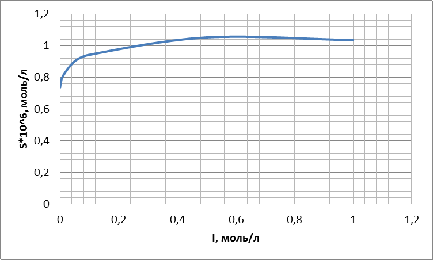
1,03 Построим график зависимости растворимости от ионной силы
раствора:
Рисунок
1 - график При
повышении концентрации NaNO3 в водном
растворе и, тем самым увеличивая ионную силу раствора, растет растворимость AgBrтв. Начиная с CNaNO3=0,5
моль/л растворимость AgBrТВ падает.
.
В зависимости от ионной силы раствора среднеионный коэффициент активности
рассчитывается по следующим уравнениям:
· · · 0,0005
0,0005
-0,011
0,974
0,01
0,01
-0,051
0,889
0,12
0,12
-0,176
0,666
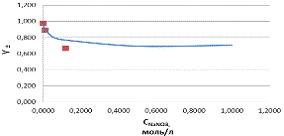
Полученные
значения нанесены на график зависимости Рисунок
2 - график зависимости При
увеличении концентрации NaNO3
среднеионный коэффициент активности уменьшается. Расчетные значения
среднеионного коэффициента активности приблизительно равны справочным
значениям.
4.
CaF2тв Пример
расчета (при рН=1):
Таблица 2
pH
S
lg S
1
1∙10-13
148,06
0,01
0,99
5,71∙10-3
-2,24
2
1∙10-12
15,71
0,06
0,94
1,28∙10-3
-2,89 1∙10-11
2,47
0,40
0,60
3,73∙10-4
-3,43
4
1∙10-10
1,15
0,87
0,13
2,24∙10-4
-3,65
5
1∙10-9
1,01
0,99
0,01
2,06∙10-4
-3,69
6
1∙10-8
1,00
0,999
1,47∙10-3
2,04∙10-4
-3,69
7
1∙10-7
1,00
0,9999
1,47∙10-4
2,04∙10-4
-3,69
8
1∙10-6
1,00
0,99999
1,47∙10-5
2,04∙10-4
-3,69
9
1∙10-5
1,00
0,999999
1,47∙10-6
2,04∙10-4
-3,69
10
1∙10-4
1,00
0,9999999
1,47∙10-7
2,04∙10-4
-3,69
11
1∙10-3
1,00
0,99999999
1,47∙10-8
2,04∙10-4
-3,69
12
1∙10-2
1,00
0,999999999
1,47∙10-9
2,04∙10-4
-3,69
Построим график зависимости логарифма растворимости CaF2 от pH:
Рисунок
3 - график При
рН от 1 до растворимость понижается, при рН > 5 растворимость не
изменяется.
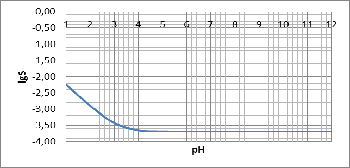
Также
построим график зависимостей долевых концентраций различных комплексов от рН:
Рисунок
4 - график зависимостей б=f(pH)
При
рН=2 начинает увеличиваться доля .
AgCNтв, NaCN, ПРAgCN=1,4∙10-16
1. AgCNтв= Ag++ CN- s
2. NaCN = Na+ + CN-
. Ag++ 2CN-= AgCN2- K1.2
4. Ag++ 3CN-= AgCN3
2- K1,2,3
5. Ag++ 4CN-= AgCN43- K1,…,4
C Ag+ = s∙б
Ag+
C CN-=2s + cNaCN,0
+2x2 +3x3 +4x4
ПPAgCN= s= K1,2 C AgCN2-=
K1,2∙ K1,2,3 C AgCN3 2-=
K1,2,3∙ K1,…,4 C AgCN43-=
K1,…,4∙ вкомпл=1+K1,2
∙ C2CN-+K1,2,3∙
C3CN-+K1,…,4 ∙
C4CN-= C Ag+∙
вкомпл
б Ag+= б AgCN2- = б AgCN3 2-= б AgCN43-
= Пример расчета ( вкомпл =1+K1,2 ∙ C2CN-+K1,2,3∙ C3CN-+K1,…,4 ∙ C4CN-=1+1019,85∙
0,00012+ 10 20,55∙ 0,00013+ 10 19,42∙ 0,00014=1
б
Ag+= б AgCN2- = б AgCN3 2-= б AgCN43-
= s= Таблица
3
10-15
1
0,9999999999
7,08∙10-11
3,55∙10-25
2,63∙10-41
0,14
-0,85
-15
10-14
1
0,99999999
7,08∙10-9
3,55∙10-22
2,63∙10-37
0,014
-1,85
-14
10-13
1
0,999999
7,08∙10-7
3,55∙10-19
2,63∙10-33
1,4∙10-3
-2,85
-13
10-12
1
0,9999
7,08∙10-5
3,55∙10-16
2,63∙10-29
1,4∙10-4
-3,85
-12
10-11
1,01
0,99
7,03∙10-3
3,52∙10-13
2,61∙10-25
1,41∙10-5
-4,85
-11
10-10
1,71
0,59
0,41
2,08∙10-10
1,54∙10-21
2,39∙10-6
-5,62
-10
10-9
71,79
0,01
0,99
4,94∙10-9
3,66∙10-19
1,01∙10-5
-5,00
-9
10-8
7080,46
1,41∙10-4
0,9999
5,01∙10-8
3,71∙10-17
9,91∙10-5
-4,00
-8
10-7
707947,14
1,41∙10-6
0,999998
5,01∙10-7
3,72∙10-15
9,91∙10-4
-3,00
-7
10-6
70794934,25
1,41∙10-8
0,99999
5,01∙10-6
3,72∙10-13
9,91∙10-3
-2,00
-6
10-5
7079812658
1,41∙10-10
0,9999
5,01∙10-5
3,72∙10-11
9,91∙10-2
-1,00
-5
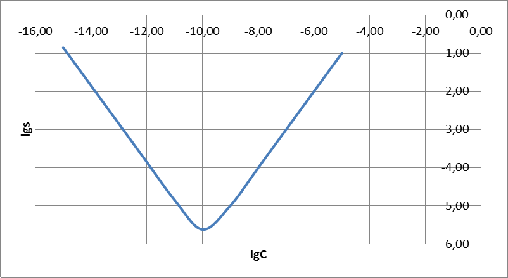
Построим график зависимости логарифма растворимости AgCN от концентрации NaCN:
Рисунок
5 - график По
графику видно, что наименьшую растворимость AgCN в водных растворах NaCN
имеет при концентрации Также
построим графики зависимостей долевых концентраций различных комплексов серебра
и цианита от логарифма концентрации NaCN:
Рисунок
6 - график зависимостей При
Выводы
В работе была рассчитана растворимость при различных условиях:
. растворимость осадка малорастворимого соединения AgBr в чистой воде SI
= 7,28∙10-7 (моль/л);
2.
растворимость осадка малорастворимого соединения AgBr, в водном растворе NaNO3,
содержащем в избытке ион NO-3. Растворимость достигает максимального значения
s= 1,05 .
растворимость осадка при гидролизе катиона малорастворимой соли CaF2. Анион F-
подвергается гидролизу, что приводит к повышению растворимости осадка, в состав
которого он входит;
.
растворимость осадка малорастворимого соединения AgCN при наличии
комплексообразования с ионами СN-, входящими в состав соли NaCN. При повышении
концентрации CN- растворимость начинает расти. Мы получили минимальную
растворимость Список литературы
1. Краткий справочник физико-химических величин / Под ред.
А.А. Равделя и А.М. Пономаревой Л.; Химия. 1983. 232 с.
. Расчеты равновесий в аналитической химии. М.И. Булатов. Л.:
Химия. 1984.
. Ионные равновесия. Дж.Н. Батлер.Л.: Химия,1973.
. Химический анализ. Г.А. Лайтинен, В.Е. Харрис, М.: Химия.
1979.
. Основы аналитической химии. Том 1. Д. Скуг, Д. Уэст. М.:
Мир. 1979.
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() -
предельное уравнение Дебая-Хюккеля,
-
предельное уравнение Дебая-Хюккеля, ![]()
![]()
![]()
![]() -
расширенное уравнение Дебая-Хюккеля,
-
расширенное уравнение Дебая-Хюккеля, ![]()
![]()
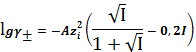
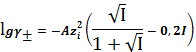 -
уравнение Дэвиса,
-
уравнение Дэвиса, ![]()
![]()
![]()
![]() , моль/лI, моль/лlg г±г±
, моль/лI, моль/лlg г±г±
![]()
![]() ,
представленный ниже:
,
представленный ниже:
![]()
![]() . Точки -
расчетные значения среднеионного коэффициента активности
. Точки -
расчетные значения среднеионного коэффициента активности
![]()
![]()
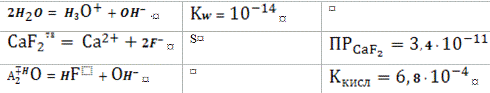
![]()
![]() =
=![]()
![]()
![]()
![]()
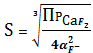
![]()
![]()
![]() =
=![]()
![]() =
=![]()
![]()
![]()
![]()
![]() =
=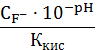
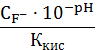
![]()
![]() =
=![]()
![]()
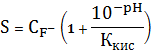
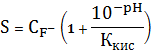 =
=![]()
![]()
![]()
![]()
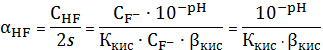
![]()
![]() =1+
=1+![]()
![]() 148,06
148,06
![]()
![]() =
=![]()
![]()
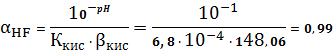
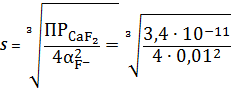
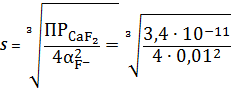 =5,71∙10-3 (моль/л)
=5,71∙10-3 (моль/л)
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() и
уменьшается доля
и
уменьшается доля ![]()
![]() . При
рН=6 доля частиц
. При
рН=6 доля частиц ![]()
![]() достигает
максимума. При рН=3,2 доли
достигает
максимума. При рН=3,2 доли ![]()
![]() и
и ![]()
![]() равны.
При высоких значениях рН преобладает доля
равны.
При высоких значениях рН преобладает доля ![]()
![]() .
.
![]()
![]() =
C Ag+ ∙ C CN-
=
C Ag+ ∙ C CN-![]()
![]() = s∙б
Ag+∙
= s∙б
Ag+∙ ![]()
![]() =
s∙б Ag+∙
=
s∙б Ag+∙ ![]()
![]()
![]()
![]() =
CAg+ + C AgCN2- +
C AgCN3 2- + C AgCN43-
=
CAg+ + C AgCN2- +
C AgCN3 2- + C AgCN43-
![]()
![]()
![]()
![]() C
Ag+ ∙ C2CN-
C
Ag+ ∙ C2CN-
![]()
![]()
![]()
![]() C
Ag+ ∙ C3CN-
C
Ag+ ∙ C3CN-
![]()
![]()
![]()
![]() C
Ag+ ∙ C4CN-=
C Ag+(1+K1,2 ∙ C2CN-+K1,2,3∙ C3CN-+K1,…,4 ∙ C4CN-)
C
Ag+ ∙ C4CN-=
C Ag+(1+K1,2 ∙ C2CN-+K1,2,3∙ C3CN-+K1,…,4 ∙ C4CN-)
![]()
![]() =
=![]()
![]()
![]()
![]() =
=![]()
![]()
![]()
![]() =
=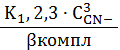
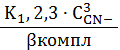
![]()
![]() =
= 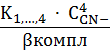
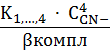
![]()
![]() =10-15 моль/л):
=10-15 моль/л):
![]()
![]() =
=![]()
![]() =0,9999999999
=0,9999999999
![]()
![]() =
=![]()
![]() =
=![]()
![]() = 7,08∙10-11
= 7,08∙10-11
![]()
![]() =
=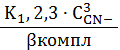
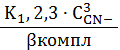 =
=![]()
![]() = 3,55∙10-25
= 3,55∙10-25
![]()
![]() =
= 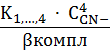
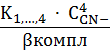 =
=![]()
![]() = 2,63∙10-41
= 2,63∙10-41
![]()
![]() = 0,14 (моль/л)
= 0,14 (моль/л)
![]()
![]() , моль/лвкомплб Ag+б AgCN2-б AgCN3 2-б AgCN43-slgslgc
, моль/лвкомплб Ag+б AgCN2-б AgCN3 2-б AgCN43-slgslgc
![]()
![]()
![]()
![]() моль/л
моль/л
![]()
![]() .
.
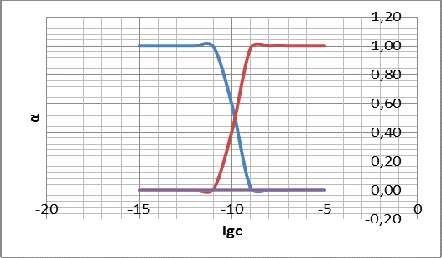
![]()
![]()
![]()
![]() начинает
понижаться доля частиц Ag+ и
повышаться доля AgC
начинает
понижаться доля частиц Ag+ и
повышаться доля AgC![]()
![]() . Долевые
концентрации AgC
. Долевые
концентрации AgC![]()
![]() и AgC
и AgC![]()
![]() В районе
точки со значением
В районе
точки со значением ![]()
![]() доли
частиц Ag+ и AgC
доли
частиц Ag+ и AgC![]()
![]() равны.
равны.
![]()
![]() (моль/л)
при CNaNO3=0,5 моль/л, далее при повышении концентрации растворимость AgBrТВ
падает;
(моль/л)
при CNaNO3=0,5 моль/л, далее при повышении концентрации растворимость AgBrТВ
падает;
![]()
![]() при
при ![]()
![]() моль/л.
моль/л.