Материал: Растворимость малорастворимых соединений
![]()
![]() (4)
(4)
Привлекая
(3) и (4) в (2), получим:
![]()
![]() =
= ![]()
![]() (5)
(5)
Из
уравнения (5) нетрудно выразить концентрацию насыщенного раствора
![]()
![]() =
=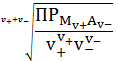
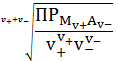 . (6)
. (6)
3. Растворимость осадка малорастворимого соединения в водном растворе,
содержащем в избытке одноименный ион
Влияние одноименного иона предсказывается принципом Ле-Шателье. Рассмотрим в общем виде влияние на растворимость малорастворимого соединения одноименного аниона, а затем в примерах и одноименного аниона и одноименного катиона.
Имеем
систему, представляющую собой водный раствор малорастворимого соединения![]()
![]() и хорошо
растворимую соль, содержащую такой же анион, например, NaA .
и хорошо
растворимую соль, содержащую такой же анион, например, NaA .
Уравнение
равновесия будет таким же, как и у случае растворимости осадка в чистой воде:
Mv+ Av-тв= Mv+ Av-р-р = v+Mz++v-Az- . (1)
cн.р.
Запишем закон равновесия
![]()
![]() =
=![]()
![]() . (2)
. (2)
Допустим, что активности ионов равны их концентрациям. При значительной концентрации электролитов в воде это допущение не верно, но для того, чтобы пояснить влияние на растворимость именно одноименного аниона или катиона, пока примем, что это допущение справедливо. Равновесные концентрации ионов в растворе с одноименным электролитом, будут другими, чем в чистой воде:
Если
концентрация катиона может быть выражена также
![]()
![]() , (3)
, (3)
то концентрация аниона будет определяться концентрацией соли, дающей при
растворении этот анион
![]()
![]() . (4)
. (4)
Обычно концентрацией насыщенного раствора в выражении (4) по сравнению с
концентрацией соли можно пренебречь, тогда
![]()
![]() =
= ![]()
![]() (5)
(5)
Из уравнения (5) нетрудно выразить концентрацию насыщенного раствора:
![]()
![]() =
=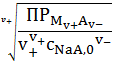
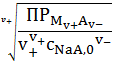 . (6)
. (6)
Из (6) видно, что растворимость малорастворимого соединения в присутствии в растворе одноименного аниона будет уменьшаться.
4. Растворимость осадка малорастворимого соединения в водном растворе,
содержащем в избытке ионы, не входящие в осадок
Экспериментально установлено, что осадки обычно более растворимы в растворе электролита, чем в воде (при условии, конечно, что электролит не содержит одноименных с осадком ионов). В этом случае увеличится ионная сила раствора, уменьшатся коэффициенты активности и увеличится растворимость малорастворимого соединения. Влияние электролита на растворимость объясняется электростатическим притяжением между ионами осадка и противоположно заряженными посторонними ионами. Такие взаимодействия вызывают сдвиг равновесия реакции растворения. Математически эти взаимодействия можно учесть, используя такую формулу произведения растворимости, в которую входят коэффициенты активности.
Формально в выражение закона равновесия для насыщенного раствора
малорастворимого соединения концентрация посторонних электролитов не входит,
поэтому выражение реакции будет таким же:
Mv+ Av-тв= Mv+ Av-р-р = v+Mz++v-Az- . (1)
cн.р.
Запишем закон равновесия
![]()
![]() =
=![]()
![]() . (2)
. (2)
Растворимость найдется из выражения
![]()
![]() =
=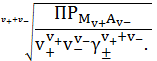
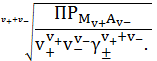 . (3)
. (3)
5. Влияние конкурирующих равновесий на растворимость осадков
Растворимость осадка увеличивается в присутствии ионов или молекул
веществ, образующих с ионами осадка слабодиссоциирующие соединения или
комплексы. Например, растворимость фторида кальция в кислой среде выше, чем в
нейтральной, поскольку фторид-ион реагирует с ионами водорода. Вследствие этого
в насыщенном растворе фторида кальция устанавливаются два равновесия:
Ca2тв=Са2++2F- (1)
F- + Н2О=HF + OH- (2)
В соответствии с принципом Ле-Шателье добавление кислоты приведет к
увеличению концентрации фтористого водорода. Вызванное этим понижение
концентрации фторид-иона частично компенсируется сдвигом первого равновесия
вправо, в результате чего растворимость осадка возрастает. В качестве примера
соединения, в состав которого входит катион с кислотными свойствами, приведем
иодид висмута. В насыщенном растворе устанавливаются равновесия: BiI3
BiI3тв =Bi+3 + 3I- ; (3)
Bi3++ Н2О = BiOH2++H3O+. (4)
Растворимость иодида висмута в отличие от растворимости фторида кальция с увеличением кислотности уменьшается.
Другим примером повышения растворимости в присутствии веществ,
реагирующих с ионами осадка, служат равновесия в насыщенном растворе бромистого
серебра с присутствием в этом растворе аммиака.
AgBrтв= Ag++Br-; (5)
Ag+ +2NH3=Ag(NH)2+. (6)
Молекулы аммиака понижают концентрацию ионов серебра в растворе, в результате чего равновесие реакции растворения сдвигается вправо и растворимость бромида серебра увеличивается.
Приведенные примеры - растворение фторида кальция или бромида серебра в присутствии аммиака относятся к часто встречаемым на практике случаям, когда в водных растворах устанавливаются конкурирующие равновесия. Иногда в дополнительных равновесиях участвуют и катион и анион осадка. Для определения растворимости малорастворимого соединения в подобных системах необходимо знать константы равновесия всех равновесий.
5.1 Растворимость осадка малорастворимого соединения с учетом протолитических реакций их ионов
.1.1 Растворимость осадка, образованного анионом слабой кислоты
Если анион малорастворимого соединения является анионом слабой кислоты,
то в водном растворе он будет участвовать не только в равновесии с твердым
малорастворимым соединением, но и в равновесии между ионными формами этой
слабой кислоты. То есть будут наблюдаться следующие реакции (рассмотрим для
простоты случай, когда анион - однозарядный):
MAтв = M++А-; (1)
А- +H3О+ = HA + H2О. (2)
Образующийся за счет растворения осадка анион сразу же начинает участвовать во втором равновесии и его концентрация уменьшается , так как он перераспределяется и существует в виде двух ионных форм: аниона и недиссоциированной слабой кислоты.(Удобный способ расчета мольных долей каждой из этих форм будет приведен при описании примера).
Следовательно, равновесная концентрация аниона малорастворимого
соединения, входящая в выражение ПР, будет уменьшена, она будет учитывать
мольную долю той ионной формы, которая получается при растворении
мало-растворимого соединения:
![]()
![]() (3)
(3)
Здесь
![]()
![]() - доля
общей концентрации аниона, находящейся именно в форме А. Для одноосновной
кислоты эта величина найдется
- доля
общей концентрации аниона, находящейся именно в форме А. Для одноосновной
кислоты эта величина найдется![]()
![]()
![]()
![]() (4)
(4)
где:
![]()
![]() -
константа ионизации слабой кислоты.
-
константа ионизации слабой кислоты.
Закон
равновесия:
![]()
![]() (5)
(5)
Предположим, что коэффициент активности равен 1:
![]()
![]() (6)
(6)
Выразим равновесные концентрации ионов:
![]()
![]() (7)
(7)
![]()
![]() (8)
(8)
![]()
![]() (9)
(9)
Из уравнения (9) нетрудно выразить концентрацию насыщенного раствора:
![]()
![]() (10)
(10)
Осадки, содержащие анионы - основания ( например, оксалат кальция) или
катионы-кислоты (например, иодид висмута) вносят свой вклад в концентрацию
ионов водорода в водном растворе. Поэтому, если только концентрация ионов
водорода не поддерживается постоянной при помощи какого-либо дополнительного
равновесия, она зависит от растворимости осадка. При расчете растворимости
таких осадков нужно учитывать, какая величина рН устанавливается в растворе.
.1.2 Растворимость осадка, образованного катионом слабого основания
Катионы многих тяжелых металлов действуют как кислоты и подвергаются
гидролизу, что приводит к повышению растворимости осадков, в состав которых они
входят. Рассмотрим простейшие реакции, происходящие при протолизе катиона:
![]()
![]() (1)
(1)
![]()
![]() (2)
(2)
Протолиз катиона сопровождается образованием различных гидроксокомплексов
и увеличением растворимости осадка. Если рассматривать константы равновесия
этих реакций как последовательные ступенчатые константы кислотной ионизации
гидратированного катиона n+M, то по аналогии с рассмотренными
ранее долевыми концентрациями ионов можно определить и долевую концентрацию
металла, находящегося в гидратированном состоянии, то есть
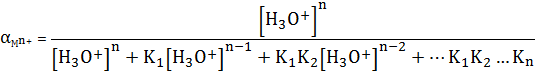
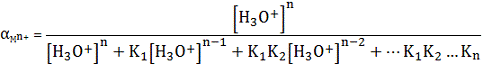 (3)
(3)
где
![]()
![]() (4)
(4)
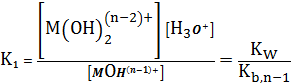
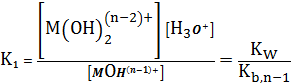 (5)
(5)
где
в свою очередь,![]()
![]() ,
, ![]()
![]() -
ступенчатые константы нестойкости гидроксокомплексов.
-
ступенчатые константы нестойкости гидроксокомплексов.
5.2 Растворимость осадка малорастворимого соединения при наличии в растворе комплексующих агентов
Если
в растворе есть комплексующий агент, например, ![]()
![]() лиганд
(он может иметь заряд, может быть нейтральной частицей. Мы рассмотрим
нейтральную частицу), то возможно образование комплексных соединений,
комплексов по схеме:
лиганд
(он может иметь заряд, может быть нейтральной частицей. Мы рассмотрим
нейтральную частицу), то возможно образование комплексных соединений,
комплексов по схеме:
![]()
![]()
![]()
![]() (1)
(1)
![]()
![]()
![]()
![]() (2)
(2)
![]()
![]() -
ступенчатые константы устойчивости или константы образования комплексных
соединений. Другое обозначение
-
ступенчатые константы устойчивости или константы образования комплексных
соединений. Другое обозначение ![]()
![]()
Можно записать полную реакцию:
![]()
![]()
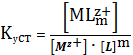
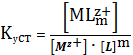 (3)
(3)