Материал: Производство лака ПФ-060
Расчет ρсмеси, кг/м3:
ρcм= ρ2=![]() ; (4.5)
; (4.5)
Где:
Gi - массовая доля компонента в смеси, кг;
ρi- плотность компонента, кг/м3 ;
Vр=6,3 м3;
ρ2= ρподсол.масла=925 кг/м3, [2];
Кзап=0,8.
G2 =6,3• 925•0,8=7284,375 кг
Q2=7284,375• 1,84•(150-20)=1742422,5кДж
Расчет тепла, необходимого на нагрев реактора Q3, кДж
Q3 = G3·C3·(t3б -t3м ) (4.6)
Где:
G3 -масса пустого реактора;
С3 - теплоемкость стали , кДж/кг·К;
t3б - большая температура реактора;
t3м - меньшая температура реактора ;
G3= 5800кг;
С3 =504 Дж/кг·К=0,504 кДж/кг·К;
Q3=5800·0.504·(155-20)=394632 кДж.
Расчет количества выделяемого/поглощаемого тепла в ходе химической реакции Q4, кДж
4 = G4·q4 ; (4.7)
Где:
G4 - масса веществ, участвующих в реакции, кг;
q4- тепловой эффект реакции, Дж/кг;
q4= О Дж/кг, так как нет реакции;
Q4 =0 кДж
Расчет количества потерь тепла в окружающую средуQ5, кДж
Принимается равным 5% от суммы полезно затраченного тепла.
Q5=0,05![]() ; (4.8)
; (4.8)
Q5 =0.05·(1742422,5+39462)=106852,3 кДж;
Расчет суммарного расхода тепла Q1, кДж
Q1 =1742422,5+39462+106852,255 =2243907,3кДж;
Расчет теплового потока Qсек, кВт
Тепловой поток- это расход тепла в единицу времени
Qсек
=![]() (4.9)
(4.9)
Где:
τ - время нагрева, ч.
Qсек =![]() =139 кВт
=139 кВт
Расчет теплового баланса на стадии нагрева реакционной массы от 150 до 250о С
Здесь нагрев производится электроиндуктором
Q1
=Q2+Q3
±Q4 +Q5
(4.10)
Где:
Q1 -суммарный расход тепла, кДж;
Q2 -суммарный расход тепла на нагрев смеси, кДж;
Q3 -тепло на нагрев реактора, кДж;
Q4 -количество тепла, выделяющегося или поглощаемого в ходе химической реакции, кДж;
Q5 -потеря в окружающую среду, кДж.
Расчет Q2 суммарного расхода тепла на нагрев смеси считаем по формуле (4.2)
Расчет ρ смеси проводим по формуле (4.5):
ρподсол.масла=925 кг/м3, [2];
ρпентаэритрита =1400 кг/м3, [2];
ρ2=![]() =
=![]() =969,77кг/м3;
=969,77кг/м3;
Теплоёмкость смеси считаем по формуле (4.3);
хподсол. масла=![]() = 0,864;
= 0,864;
хпентаэритрит=1-0, 864=0,136;
Сподсол. масла=1,84 кДж/кг·К, [2];
Спентаэритрит=2,27 кДж/кг·К, [2];
С2=1,84·0,864+2,27·0,136=1,898 кДж/кг·К;
Массу смеси считаем по формуле (4.4);
G2=6.3·969,77·0.8=4887,641 кг;
Q2 = 4887,641•1,898 (250-150)=927674,22 кДж;
Расчет тепла на нагрев реактора Q3 по формуле (4.6)
Q3=5800·0,504·(255-150)=306936 кДж;
Расчёт количества тепла, выделяющегося или поглощаемого в ходе химической реакции Q4по формуле (4.7);
Q4 =0 кДж, так как нет реакции;
Расчет потери тепла в окружающую среду Q5 по формуле (4.8)
Q5=0,05·(927674,22 +306936)=61730,511 кДж;
Расчет суммарного расхода тепла Q1 по формуле (4.10)
Q1=927674,22 +306936+61730,511 =1296340,371кДж;
Расчет теплового потока Qсек, кВт по формуле (4.9)
Qсек = ![]() = 111 кВт;
= 111 кВт;
Расчет теплового баланса на стадии выдержки (реакция переэтерификации)
Q1
=Q2+Q3
±Q4 (4.11)
Где:
Q1 - общий расход тепла, кДж;
Q2 - расход тепла на выдержку реакционной массы, кДж;
Q3 - расход тепла на реактор, кДж;
Q4 - расход тепла выделяющееся или поглощаемое в ходе химической реакции, кДж;
Расчет суммарного расхода тепла на нагрев смеси Q2по формуле (4.2)
Q2=0 кДж;
Чтобы исключить нагрев реакционной массы (должны поддерживать 250о С).
Расчет тепла на нагрев реактора Q3по формуле (4.6)
Q3=0 кДж;
Чтобы не было перегрева.
Расчет количества тепла, выделяющегося или поглощаемого в ходе химической
реакции Q4по формуле (4.7)
Q4=G4·q4;
q4=-10771,47 Дж/кг ;
4=Vр•ρсм•Кзап;
(4.12)
Где:
Vр- вместимость реактора, м3;
ρ2 -плотность масла, кг/м3;
Кзап- коэффициент заполнения реактора.;
Расчет ρ смеси проводим по формуле (4.5):
ρподсол.масла=925 кг/м3;
ρпентаэритрита =1400 кг/м3;
ρ2= ![]() =
=![]() =969,77кг/м3;
=969,77кг/м3;
Расчет массы смеси по формуле (4.4);
G4=6,3•969,77•0,8=4887,641кг
Q4=-10771,47•4887,641= -52647081,28Дж= -52647,081кДж
Q1= Q4 =-52647,081кДж
Расчет теплового баланса на стадии охлаждения переэтерификата от 250 до
180оС
Q1
=Q2+Q3
±Q4 (4.13)
Где:
Q1 - общий расход тепла, кДж;
Q2 - расход тепла на охлаждение переэтерификата, кДж;
Q3 - расход тепла на охлаждение реактора, кДж;
Q4 - расход тепла выделяющееся или поглощаемое в ходе химической реакции, кДж;
Расчет Q2 суммарного расхода тепла на охлаждение переэтерификата по формуле (4.2)
ρ2==969,77кг/м3;
С2=1,898 кДж/кг·К;
G2=4887,641 кг;
Q2 = 4887,641•1,898 (250-180)=649371,98 кДж;
Расчет тепла на нагрев реактора Q3 по формуле (4.6)
Q3=5800·0,504·(255-180)=219240 кДж;
Расчёт количества тепла, выделяющегося или поглощаемого в ходе химической реакции Q4, кДж
Q4 =0 кДж, так как нет реакции;
Расчет суммарного расхода тепла Q1по формуле (4.13)
Q1=649371,98 +219240=868611,98кДж;
Расчет теплового потока Qсек, кВт по формуле(4.9)
Qсек = ![]() = 193 кВт;
= 193 кВт;
Расчет теплового баланса на стадии нагрева реакционной массы от 180 до
250о С, (реакция этерификации)
Q1
=Q2+Q3
±Q4 +Q5
(4.14)
Где:
Q1 -суммарный расход тепла, кДж;
Q2- расход тепла на нагрев реакционной массы, кДж;
Q3 -расход тепла на нагрев реактора, кДж;
Q4 -количество тепла, выделяющегося или поглощаемого в ходе химической реакции, кДж;
Q5 -потеря в окружающую среду, кДж.
Расчет Q2 суммарного расхода тепла на нагрев смеси считаем по формуле (4.2)
Расчет ρ смеси проводим по формуле (4.5):
ρподсол.масла=925 кг/м3;
ρпентаэритрита =1400 кг/м3;
ρфталевого ангидрида =1530 кг/м3, [2];
ρ2=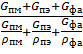 =
=![]() =1057,318 кг/м3;
=1057,318 кг/м3;
Теплоёмкость смеси считаем по формуле (4.3);
хподсол. масла=![]() = 0,669;
= 0,669;
хпентаэритрит=![]() =0,105;
=0,105;
хфталевого ангидрида=![]() =0,266;
=0,266;
Сподсол. масла=1,84 кДж/кг·К;
Спентаэритрит=2,27 кДж/кг·К;
Сфталевого ангидрида=1,07 кДж/кг·К;[…]
С2=1,84·0,669+2,27·0,105+1,07·0,226=1,711 кДж/кг·К;
Расчет массы смеси по формуле (4.4);
G2=6.3·1057,318·0.8=5328,883 кг;
Q2 = 5328,883•1,711 (250-180)=638240,32 кДж;
Расчет тепла на нагрев реактора Q3по формуле (4.6)
Q3=5800·0,504·(255-180)=219240 кДж;
Расчёт количества тепла, выделяющегося или поглощаемого в ходе химической
реакции Q4по формуле (4.7)
Q4=G4·q4;
q4=219178,08 Дж/кг ;
4=Vр•ρсм•Кзап
Где:
G4=6,3•1057,318•0,8=5328,883кг
Q4=5328,883•219178,08= 1167974,356кДж
Расчет потери тепла в окружающую среду Q5 по формуле (4.8)
Q5=0,05·(638240,32 +219240+1167974,356)=101272,73 кДж;
Расчет суммарного расхода тепла Q1по формуле (4.14)
Q1=638240,32 +219240+1167974,356+101272,73 =2126727,41кДж;
Расчет теплового потока Qсек, кВт по формуле (4.9)
Qсек = ![]() = 197 кВт;
= 197 кВт;
Расчет теплового баланса на стадии выдержки (реакция п поликонденсации)
Q1
=Q2+Q3
±Q4 +Q5
(4.15)
Где:
Q1 - общий расход тепла, кДж;
Q2 - расход тепла на выдержку реакционной массы, кДж;
Q3 - расход тепла на реактор, кДж;
Q4 - расход тепла выделяющееся или поглощаемое в ходе химической реакции, кДж;
Q5 - потери тепла в окружающую среду, кДж.
Расчет суммарного расхода тепла на нагрев смеси Q2 (по формуле (4.2)
Q2=0 кДж;
Чтобы исключить нагрев реакционной массы (должны поддерживать 250о С).
Расчет тепла на нагрев реактора Q3 по формуле (4.6)
Q3=0 кДж;
Чтобы не было перегрева.
Расчет количества тепла, выделяющегося или поглощаемого в ходе химической
реакции Q4по формуле (4.7)
Q4=G4·q4;
q4=-35787,67 Дж/кг ;
4=Vр•ρсм•Кзап
4=6,3•1057,318•0,8=5328,883кг
Q4=35787,67•5328,883= 190708,306 кДж
Расчет потери тепла в окружающую среду Q5 по формуле (4.8)
Q5=0,05•190708,306=9535,415 кДж
Расчет суммарного расхода тепла Q1 по формуле (4.15)
Q1= 190708,306 +9535,415 =200243,721 кДж
Расчет теплового потока Qсек, кВт по формуле (4.9)
Qсек = ![]() = 9 кВт;
= 9 кВт;
Расчет стадии охлаждения готового алкида от 250о до 180оС
Q1= Q2 + Q3±Q4
(4.16)
Q1 - общий расход тепла, кДж;
Q2 - расход тепла, на охлаждение алкида, кДж;
Q3 - расход тепла на охлаждение реактора, кДж;
Q4 - расход тепла выделяющееся или поглощаемое в ходе химической реакции, кДж;
Расчет суммарного расхода тепла на охлаждение алкидаQ2 (по формуле (4.2)
G2=592,6 кг (таблица 2.7)
Теплоёмкость алкида считаем по формуле:
С=![]() (4.17)
(4.17)
Где:
ai- количество атомов итого компонента;
Сi-теплоемкость итого компонента, кДж/(кг•К), [2];
Ммалкида-молекулярная масса алкид;
|
Компонент |
Количество атомов компонента в алкиде |
Атомарная теплоемкость компонентов, кДж/(кг•К) |
|
С |
234 |
11,7 |
|
О |
43 |
25,1 |
|
Н |
362 |
18 |
Ммалкида=3858
С=![]() =2,678 кДж/(кг•К);
=2,678 кДж/(кг•К);
Q2=592,6•2,678•(250-180)=111088,796 кДж;
Расчет тепла на охлаждение реактора Q3по формуле (4.6)
Q3=5800•0,504•(250-180)=204624 кДж;
Расчёт количества тепла, выделяющегося или поглощаемого в ходе химической реакции Q4по формуле (4.7)
Q4 =0 кДж, так как нет реакции;
Расчет суммарного расхода тепла Q1по формуле (4.16)
Q1= 111088,796 +204624=315712,796 кДж
Расчет теплового потока Qсек, кВт по формуле (4.9)
Qсек = ![]() = 103,17 кВт;
= 103,17 кВт;
Расчет змеевика
Расчет поверхности теплообмена змеевика, м
F=![]() (4.18)
(4.18)
Где:
Qсек- тепловой поток стадии охлаждения, кВт;
Qсек =103,17 кВт;
Δtср- разница между температурой алкида и температурой теплоносителя на данной стадии, о С;
К- коэффициент теплопередачи, принимаем 190 Вт/(м2•градус),
[2];
Δtср=tср(алкида)-tср(воды);
Δtср= ![]() =155 о С
=155 о С
F=![]() =3,5 м2
=3,5 м2
Расчет длины змеевика, м
=![]() ; (4.19)
; (4.19)
Где:
dтрубы - наружный диаметр трубы, м;
F - поверхность теплообмена змеевика, м;
dтрубы=0,06 м;
L=![]() = 18,5м;
= 18,5м;
Расчет диаметра витка змеевика, м
dвитка= ![]() + dм; (4.20)
+ dм; (4.20)
Где:
D - внутренний диаметр реактора;
dм - диаметр, который описывает мешалка, м;
м =0.5•D;
м =0.5•2.5=1.25 м;
dвитка=![]() +1.25=1,875м;
+1.25=1,875м;
Расчет длины одного витка
l=dвитка·π; (4.21)
Где:
dвитка - диаметр витка змеевика, м;
l= 1,875·3,14=5,89 м;
Расчет числа витков
n=L/l; (4.22)
Где:
L-длина змеевика, м;
l-длина витка змеевика, м;
n=18.5/5.89=3.14
Расчет шага витка (расстояние
между витками), м
t=(1.5..2)·dтр (4.23)
Где:
dтр - наружный диаметр трубы змеевика м;
t=2·0.06=0.12 м;
Расчет высоты змеевика , м
Hзм = n·t (4.24)
Где:
n - число витков змеевика
t - шаг змеевика, м;
Hзм
=3.14·0,12=0,38 м
4.2 Механические расчеты
4.2.1 Расчет мощности привода мешалки
Выбираем лопастную мешалку с вертикальными прямыми высокими лопатками.
μ=0,497 Па•с, [2];
n=0.5 сек-1, [3];
Мощность привода мешалки рассчитывается по формуле:
м=KN•ρc•n3•dм5 (4.25)