Материал: Проект организации производства серной кислоты
Осушку печного газа проводят в сушильной башне - снизу вверх поднимается печной газ, а сверху вниз льётся концентрированная серная кислота. На выходе из сушильной башни печной газ уже не содержит ни частичек огарка, ни паров воды. Печной газ теперь представляет собой смесь оксида серы SO2 и кислорода О2.
2) Вторая стадия - окисление SO2 в SO3 кислородом. Протекает в контактном аппарате.
Уравнение реакции этой стадии
2SO2
+ O2 ![]() 2SO3 + Q
2SO3 + Q
Сложность второй стадии заключается в том, что процесс окисления одного оксида в другой является обратимым. Поэтому необходимо выбрать оптимальные условия протекания прямой реакции (получения SO3).
а) температура;
Прямая реакция является экзотермической +Q, согласно правилам по смещению химического равновесия, для того, чтобы сместить равновесие реакции в сторону экзотермической реакции, температуру в системе необходимо понижать. Но, с другой стороны, при низких температурах, скорость реакции существенно падает. Экспериментальным путём химики-технологи установили, что оптимальной температурой для протекания прямой реакции с максимальным образованием SO3 является температура 400-500°С. Это достаточно низкая температура в химических производствах. Для того, чтобы увеличить скорость реакции при столь низкой температуре в реакцию вводят катализатор. Экспериментальным путём установили, что наилучшим катализатором для этого процесса является оксид ванадия V2O5.
б) давление;
Прямая реакция протекает с уменьшением объёмов газов: слева 3V газов (2V SO2 и 1V O2), а справа - 2V SO3. Раз прямая реакция протекает с уменьшением объёмов газов, то, согласно правилам смещения химического равновесия давление в системе нужно повышать. Поэтому этот процесс проводят при повышенном давлении.
Прежде чем смесь SO2 и O2 попадёт в контактный аппарат, её необходимо нагреть до температуры 400-500°С. Нагрев смеси начинается в теплообменнике, который установлен перед контактным аппаратом. Смесь проходит между трубками теплообменника и нагревается от этих трубок. Внутри трубок проходит горячий SO3 из контактного аппарата. Попадая в контактный аппарат смесь SO2 и О2 продолжает нагреваться до нужной температуры, проходя между трубками в контактном аппарате.
Температура 400-500°С в контактном аппарате поддерживается за счёт выделения теплоты в реакции превращения SO2 в SO3. Как только смесь оксида серы и кислорода достигнет слоёв катализатора, начинается процесс окисления SO2 в SO3.
Образовавшийся оксид серы SO3 выходит из контактного аппарата и через теплообменник попадает в поглотительную башню.
3) Третья стадия - поглощение SO3 серной кислотой. Протекает в поглотительной башне.
Уравнение реакции этого процесса
nSO3
+ H2SO4 ![]() H2SO4·nSO3
H2SO4·nSO3
Образовавшийся
олеум сливают в металлические резервуары и отправляют на склад. Затем олеумом
заполняют цистерны, формируют железнодорожные составы и отправляют потребителю.
2.2
Нитрозный способ производства серной кислоты
В нашей стране используется и другой, так называемый нитрозный, способ её получения.
На первой стадии, одинаковой для обоих методов, получают сернистый ангидрид SO2. Исходным сырьём может быть, в принципе, любое вещество, содержащее серу: природные сульфиды железа (прежде всего, пирит FeS2), а также сульфиды меди и никеля, сульфидные полиметаллические руды, гипс CaSO4.2H2O и элементарные сера. Всё больше и больше используют газы, которые выделяются при переработке и сжигании горючих ископаемых (угля, нефти), содержащих соединения серы.
Полученный SO2 окисляют до H2SO4, используется для этого в нитрозном методе используется окислы азота. С этой стадии оба метода отличаются друг от друга.
В
специальной окислительной башне 3 смешивают окись азота NO и NO2 с
воздухом в таком соотношении, чтобы половина имеющихся NO и NO2.
NO + O2
2NO2
В результате газовая смесь содержит равные NO и NO2. Она подаётся в башни 4 и 5, орошаемые 75% - ной серной кислотой; здесь смесь окислов азота поглощается с образованием нитрозиллерной кислоты:
+ NO2 + 2H2SO4 2NO(HSO4) + H2O
Раствор нитрозиллерной кислоты в серной кислоте, называемый нитрозой, орошает башни 1 и 2, куда противотоком поступает SO2 и добавляется вода. В результате гидролизанитрозиллерной кислоты образуется азотная кислота:
NO(HSO4)
+ H2OH2SO4 + HNO2
Она - то и окисляет SO2 по уравнению:
2
+ 2HNO2H2SO4 + 2NO
В нижней части башен 1 и 2 накапливается 75%-ная серная кислота, естественно, в большем количестве, чем её было затрачено на приготовление нитрозы (ведь добавляется «новорождённая» серная кислота). Окись азота NO возвращается снова на окисление. Поскольку некоторое количество её меряется с выхлопными газами, приходится добавлять в систему HNO3, служащую источником окислов азота.
Недостаток
башенного метода состоит в том, что полученная серная кислота имеет
концентрацию лишь 75% (при большей концентрации плохо идёт гидролиз
нитрозиллернойкислоты). Концентрирование же серной кислоты упариванием
представляет дополнительную трудность. Преимущество этого метода в том, что
примеси содержащиеся в SO2, не влияют на ход процесса, так что исходный SO2
достаточно очистить от пыли, т.е. механических загрязнений. Естественно,
башенная серная кислота бывает недостаточно чистой, что ограничивает её
применения.
.3
Охрана окружающей среды, связанная с производством серной кислоты
Основным сырьем для производства серной кислоты, является сера. Она относится к числу наиболее распространенных числу химических элементов на нашей планете.
Производство серной кислоты происходит в три стадии на первой стадии получают SO2, путем обжига FeS2, затем SO3, после чего на третьей стадии получают серную кислоту.
Научно-техническая революция и связанный с ней интенсивный рост химического производства, вызывает существенные негативные изменения в окружающей среде.Например отравление пресных вод, загрязнение земной атмосферы, истребление животных и птиц. В результате мир оказался в тисках экологического кризиса.
Вредные выбросы сернокислых заводов следует оценивать не только по действию содержащегося в них оксида серы на расположенные вблизи предприятия зоны, но и учитывать другие факторы - увеличение количества случаев респираторных заболеваний человека и животных, гибель растительности и подавление ее роста, разрушение конструкций из известняка и мрамора, повышение коррозионного износа металлов. По вине “кислых” дождей повреждены памятники архитектуры (Тадж-Макал).
В зоне до 300 км от источника загрязнения (SO2) опасность представляет серная кислота, в зоне до 600 км. - сульфаты. Серная кислота и сульфаты замедляют рост с/х культур. Закисление водоемов (весной при таянии снега, вызывает гибель икр и молоди рыб. Помимо экологического ущерба налицо экономический ущерб - громадные суммы каждый год теряются при раскисление почв.
Рассмотрим химические метода отчистки от наиболее распространенных газообразных загрязняющих воздух веществ. Известно более 60 методов. Наиболее перспективны методы, основанные на поглощение оксида серы известняком, раствором сульфита - гидросульфита аммония и щелочным раствором алюмината натрия. Интерес также представляют каталитические методы окисления оксида серы в присутствии оксида ванадия. Особое значение имеет очистка газов от фторсодержащих примесей, которые даже в незначительной концентрации вредно влияют на растительность. Если в газах содержится фтороводород и фтор, то их пропускают через колоны с насадкой противотоком по отношению к 5-10% раствору гидроксида натрия. В течении одной минуты протекают следующие реакции:
F2+2NaOH-> O2+H2O+2NaF
HF+NaOH->NaF+H2O;
Образующийся фторид натрия обрабатывают для регенерации гидроксида
натрия:
NaF+CaO+H2O->CaF2+2NaOH
.4 Хранение
Для уменьшения возможности кристаллизации серной кислоты при перевозке и
хранении установлены стандарты на товарные сорта серной кислоты, концентрация
которых соответствует наиболее низким температурам кристаллизации. Содержание
серной кислоты в техн. сортах (%): башенная (нитрозная) 75, контактная
92,5-98,0, олеум 104,5, высокопроцентный олеум 114,6, аккумуляторная 92-94.
Серную кислоту хранят в стальных резервуарах объемом до 5000 м3. Олеум и серную
кислоту перевозят в стальных железнодорожных цистернах. Концентрированную и
аккумуляторную серную кислоту перевозят в цистернах из кислотостойкой стали.
Цистерны для перевозки олеума покрывают теплоизоляцией и перед заливкой олеум
подогревают.
2. Расчетная часть
Основные технико-экономические характеристики технологического оборудования
|
Наименование |
Тип оборудования |
Производительность тонн/час |
Продолжительность ремонта, час. |
Период между ремонтами |
||||
|
|
|
|
средний |
текущий |
капитальный |
средний |
текущий |
капитальный |
|
Контактный аппарат |
К-39-4 |
2,92 |
96 |
8 |
600 |
17280 |
720 |
34560 |
|
|
К-39-4 |
9,34 |
96 |
8 |
600 |
17280 |
720 |
34560 |
|
|
К-85-5 |
14,00 |
96 |
8 |
600 |
17280 |
720 |
34560 |
|
Печь для сжигания серы |
КС-200 |
5,79 |
300 |
12 |
720 |
17280 |
720 |
34560 |
|
|
ДКСМ |
3,76 |
300 |
12 |
720 |
17280 |
720 |
34560 |
|
Брызгоулавливатель |
ПБ |
3,45 |
240 |
12 |
720 |
8640 |
720 |
34560 |
|
Сушильная башня |
СБ |
3,45 |
96 |
8 |
360 |
8640 |
720 |
34560 |
|
Абсорбер для технич. кислоты |
АТ |
3,45 |
120 |
8 |
600 |
17280 |
720 |
86400 |
|
Абсорбер для реакт. кислоты |
АР |
0,14 |
48 |
8 |
120 |
8640 |
2160 |
17280 |
Планируемая производственная программа
|
Наименование продукции |
Ед.измер. |
Плановый годовой объём производства продукции |
|
Серная кислота, техническая |
т. |
15000 |
|
Серная кислота, реактивная |
т. |
27500 |
Исходные данные для проектирования участка фасовки и комплектации готовой продукции
|
Наименование показателей |
Ед. измер. |
Вар. 10 |
|
Объем заказываемой партии |
тыс. литр |
2,25 |
|
Емкость тары (бутыли) |
15 |
|
|
Вместимость контейнера |
бут. |
12 |
|
Грузоподъемность транспорта |
конт. |
1 |
|
Емкость исходного сборника |
литр |
400 |
|
Продолжительность выполнения операций: |
||
|
Розлив в тару |
мин/литр |
0,4 |
|
Закупорка и маркировка тары |
мин/бут |
0,5 |
|
Укладка в контейнер |
сек./бут. |
25 |
|
Погрузка и доставка контейнера на склад |
мин./конт. |
8 |
|
Установка контейнера |
мин./конт. |
1,2 |
|
Возврат транспорта |
мин. |
6 |
Технической серной кислоты планируется выпустить 15000 т. в год, как и рективной - 27500 т.
Пересчет на 100% моногидрат:
Техническая: 15000 * 0,925 = 13875 т.
Реактивная: 27500 * 0,94 = 25850 т.
Вгод = 13875 + 25850 = 39725 т. (в пересчете на 100% моногидрат H2SO4)
![]() ч.
ч.
1. Контактный аппарат К-39-4
Расчетное
количество ремонтов 1 - го типа (![]() ) в
течение ремонтного цикла (РЦ) определяется по формуле:
) в
течение ремонтного цикла (РЦ) определяется по формуле:
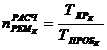
где
![]() - продолжительность ремонтного цикла,
- продолжительность ремонтного цикла,
![]() - пробег
между двумя смежными ремонтами одного типа.
- пробег
между двумя смежными ремонтами одного типа.
) ![]()
) ![]()
Общее
количество планируемых средних ремонтов (![]() ) в
течение ремонтного цикла, не совмещенных с проведением более крупных ремонтов
может быть рассчитано следующим образом:
) в
течение ремонтного цикла, не совмещенных с проведением более крупных ремонтов
может быть рассчитано следующим образом:
![]()
где 1 - количество капитальных ремонтов в межремонтном цикле.
![]()
) ![]()
Общее
количество планируемых текущих ремонтов (![]() ) в
течение ремонтного цикла расчитывается:
) в
течение ремонтного цикла расчитывается:
![]()
![]()
4) m - продолжительность ремонтного цикла (лет)
![]()
) ![]() ч.
ч.
) Эффективный
фонд времени работы оборудования в среднем за год (Тэф) определяется по формуле:
![]()
![]() ч.
ч.
)
Расчет требуемого количества оборудования j-го типа для
выполнения производственной программы (Вгод) может производиться по следующей
формуле:
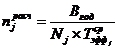
где:
![]() - расчетное количество оборудования j-го
типа,
- расчетное количество оборудования j-го
типа,
Nj - часовая производительность единицы оборудования j-го типа,
![]() -
эффективный фонд времени работы оборудования j-го типа в среднем
за год в течение межремонтного цикла.
-
эффективный фонд времени работы оборудования j-го типа в среднем
за год в течение межремонтного цикла.
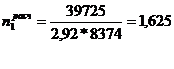
![]()
2. Печь для сжигания серы КС-200
1) ![]()
) ![]()
![]()
) ![]()
![]()
) ![]()
) ![]() ч.
ч.
) ![]() ч.
ч.
) 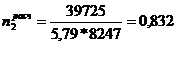
![]()
3. Промывная башня
1) ![]()
![]()
![]()
![]()
![]()
) ![]()