Материал: природный газ среднего состава
СПБГУАП группа 4736 https://new.guap.ru/i03/contacts
Таким образом, повышение температуры будет способствовать не только смещению равновесия реакции в сторону продуктов, но и увеличению скорости процесса.
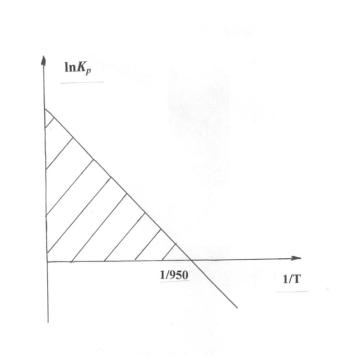
Рис. 1. Зависимость величины константы равновесия реакции паровой конверсии метана от температуры.
При сравнительно невысоких температурах, например, при 950 0С равновесный выход монооксида углерода достигает 99 %, но из-за высокого значения энергии активации реакции (Еа = 272 кДж/моль) скорость процесса мала.
Проведение процесса при более высоких температурах позволяет увеличить скорость основной реакции (1), однако наряду с этой реакцией при высоких температурах возможно протекание побочной реакции (9)
разложения (крекинга) метана:
СН4 ↔ С + 2Н2 (9) (∆Н = + 75,6 кДж)
А так как энергия активации реакции разложения метана больше энергии активации основной реакции (1), то и скорость реакции (9) в
большей степени возрастает с увеличением температуры.
8
СПБГУАП группа 4736 https://new.guap.ru/i03/contacts
Как же сделать возможным проведение процесса с достаточной скоростью при температурах ниже температуры разложения метана (t0 < 10000 С) ?
Очевидный ответ - понизить энергию активации основной реакции (1),
применив селективный катализатор.
3.1.3. Выбор оптимальных условий для проведения паровой конверсии метана
3.1.3.1. Катализатор и температура
В качестве катализатора может быть применен любой металл VIII группы периодической системы. В промышленности используют никелевые катализаторы на носителе (α-Al2O3). В качестве промоторов ─ оксиды кальция и магния. Данный катализатор понижает энергию активации основой реакции до 92 кДж/моль. Содержание никеля в катализаторе может изменяться в широких пределах – от 4 до 35 % (масс.). Удельная поверхность катализаторов от 5 до 50 м2/г. Рабочая температура - 800 – 1000 0С.
Восстановление нанесенного на поверхность носителя оксида никеля до металлического никеля происходит водородом или метаном.
Катализатор легко отравляется сернистыми соединениями, вследствие образования на его поверхности сульфидов никеля, совершенно неактивных в реакции конверсии метана и его гомологов. Поэтому предварительно необходимо проведение очистки поступающего газа от серусодержащих соединений.
Для примера приведем состав катализатора марки ГИАП-16, % (масс.): NiО - 25; Al2O3 - 57; СаО - 10; MgO - 8. Срок службы катализатора при правильной эксплуатации около 3 лет.
3.1.3.2. Давление
Несмотря на то, что понижение давления по принципу Ле-Шателье смещает равновесие реакции (1) вправо, процесс проводят при повышенном давлении (примерно 2 - 5 МПа), что позволяет:
1) увеличить скорость процесса и его интенсивность;
9
СПБГУАП группа 4736 https://new.guap.ru/i03/contacts
2)уменьшить объем оборудования;
3)использовать давление природного газа в магистральных трубопроводах;
4)уменьшить расход энергии при последующей компрессии газов, направляемых, например, на синтез аммиака или синтез метанола;
5)создавать более компактные и эффективные системы утилизации
тепла.
При температуре 900 0С и давлении ≈ 4 МПа равновесный выход реакции (1) близок к 100 %
3.1.3.3.Соотношение исходных веществ
Процесс ведут с избытком водяного пара - Н2О/ СН4 = 2 3/1, который необходим:
1)для увеличения степени превращения метана;
2)для предотвращения образования отложений кокса на поверхности катализаторе. Взаимодействие водяного пара с углистыми отложениями происходит по реакции;
С+ Н2О СО + Н2 (10)
3) для последующей паровой конверсии монооксида углерода.
Таким образом, оптимальные условия процесса паровой
конверсии метана:
-Ni - катализатор;
-800 - 900 0С;
-соотношение Н2 O/СН4 2-3;
-Р = 2 - 5 МПа
Впромышленности паровую конверсию метана (I этап конверсии метана) для получения азотоводородной смеси обычно комбинируют с паровоздушной конверсией (вторичный риформинг) – II этап конверсии метана.
10
СПБГУАП группа 4736 https://new.guap.ru/i03/contacts
3.2. Паровоздушная конверсия метана
Применение паровоздушной конверсии метана позволяет уменьшить энергетические затраты путем совмещения в одном реакторе эндотермической:
СН4 + Н2О (пар) ↔ СО+3Н2 |
(1) |
(∆Н = + 206,4 кДж) |
и экзотермической реакции: |
|
|
СН4 + 0,5О2 → СО + 2Н2 |
(3) |
(∆Н = - 35,6 кДж), |
а также ввести в состав получаемого газа соответствующего количества азота, необходимого для синтеза аммиака.
Реакция (3) - необратимая, экзотермическая, является суммарной. На первой стадии процесса часть метана окисляется до диоксида углерода и воды:
СН4 + 2О2 → СО2 + 2Н2О (11) (∆Н = - 800 кДж)
Далее метан реагирует с продуктами окисления в соответствии с
реакциями (1) и (2): |
|
|
СН4 |
+ Н2О (пар) ↔ СО+3Н2 |
(1) |
СН4 |
+ СО2 ↔ 2СО + 2Н2 |
(2) |
Отметим, что применение исключительно |
кислородной (воздушной) |
конверсии не позволяет получить нужное |
соотношение Н2/N2. По |
стехиометрии реакции (3): СН4 + 0,5О2 → СО + 2Н2 при получении 1
объема Н2 с кислородом воздуха вводится около 1 объема азота, что не соответствует стехиометрии азотоводородной смеси для синтеза аммиака.
Совмещение в одном реакторе противоположных по знаку теплового эффекта реакций позволяет проводить процесс в автотермическом режиме,
11
СПБГУАП группа 4736 https://new.guap.ru/i03/contacts
т.е. без дополнительного обогрева реактора, как это имеет место на стадии паровой конверсии метана.
На первой ступени (при паровой конверсии) природного газа превращается около 90 % метана и соответственно на второй (паровоздушной конверсии) – около 10 % метана.
III этап – паровая конверсия монооксида углерода.
3.3. Паровая конверсия монооксида углерода
|
3.3.1. Термодинамика процесса |
|
|
|
|
|
||||
|
|
СО + Н2О (пар) ↔ СО2 + Н2 (4) |
|
(∆Н = - 41,3 кДж) |
||||||
|
Процесс паровой конверсии монооксида |
углерода |
- сложный, с |
|||||||
побочными реакциями: |
|
|
|
|
|
|
|
|||
|
|
2СО СО2 + С |
(11) |
|
|
|
|
|
||
|
|
СО + 3Н2 СН4 |
+ Н2О (12) |
|
|
|
|
|
||
|
Реакция (4) обратима в широком интервале температур (табл.2), |
|||||||||
экзотермическая, протекает без изменения числа молей. |
|
|
||||||||
|
|
|
|
|
|
|
|
|
Таблица 2. |
|
Зависимость величины константы равновесия (Кр) реакции (4) от температуры. |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
Т, К |
|
400 |
500 |
|
600 |
700 |
|
800 |
|
900 |
|
|
|
|
|
|
|
|
|
|
|
Кр |
|
1,5∙103 |
1,3∙102 |
|
2,7∙10 |
9,0 |
|
4,0 |
|
2,2 |
|
|
|
|
|
|
|
|
|
|
|
Для смещения равновесия вправо необходимо уменьшить температуру, изменение давления не влияет на положение равновесия.
3.3.2. Кинетика процесса
Для увеличения скорости процесса необходимо увеличивать температуру и давление, т.е. имеет место часто встречающийся случай –
12