Материал: Принципы технологии получения противоопухолевых препаратов на основе моноклональных антител
. Плотность полученной смеси доводят до 1-5)-105 клеток/мл, после чего по 1 мл суспензии осторожно разливают в лунки 24-луночного планшета (или 96-луночного). Планшет переносят в термостат с регулируемым составом атмосферы и увлажнением [4].
День проведения эксперимента по слиянию
обозначают как нулевой день - день 0. На 1-й, 2-ой, 3-ий день после слияния
осторожно заменяют по 1 мл среды из каждой лунки на 1 мл среды ГАТ. Важно не
потревожить клетки в лунках, в частности, избежать перемещения клеток на одну
сторону лунки при добавлении свежей среды. Кроме того, чрезвычайно важно
избежать перекрестного переноса клеток из одних лунок в другие. Если клетки не
повреждаются во время смены среды, то начавшие расти гибридомы должны
образовывать достаточно обособленные колонии, что видно под микроскопом [2].
.3 СТАДИЯ ВЫРАЩИВАНИЯ ГИБРИДОМ В КУЛЬТУРЕ
В первое время наличие больших количеств клеточных обломков, а также несинхронность гибели в среде ГАТ неслившихся миеломных клеток затрудняет обнаружение гибридных клеток. Однако через 7-9 дней начинают появляться небольшие кластеры клеток, имеющих типичную морфологию гибридом. В зависимости от изначальной плотности клеток в рассеваемой смеси в каждой лунке может оказаться один или более кластеров. В этот период надо следить не только за ростом гибридов и изменением цвета среды в лунках, но также и за наличием зараженных лунок, которые необходимо соответствующим образом обрабатывать.
Когда кластеры гибридных клеток достигнут размера 2-3 мм в диаметре, супернатанты (надосадочная жидкость) можно будет тестировать на наличие антительной активности. Иногда при использовании высокоиммуногенных антигенов при скрининге наблюдается высокий уровень фона, обусловленный антителами, синтезированными нормальными плазматическими клетками, которые не слились, но оказались в лунках на начальной стадии и продолжали секретировать антитела в течение нескольких дней после рассева. Эти остаточные антитела негибридомного происхождения можно удалить до проверки на активность, если при «подкармливании» хотя бы один раз полностью сменить среду и провести анализ через 1--3 дня - время, необходимое для того, чтобы в среде появилось достаточное количество антител, секретированных гибридомой [4].
.4 СТАДИЯ ПОЛУЧЕНИЯ МОНОКЛОНАЛЬНЫХ АНТИТЕЛ
В зависимости от того, каким образом планируется использовать моноклональные антитела, их можно выделять множеством различных способов.
Полученную продуцирующую гибридому дважды клонируют на фидере из клеток селезенки и тимуса мышей. Для приготовления фидера кусочки тимуса и селезенки измельчают на гомогенизаторе Поттера в ростовой среде (например, RPMI-1640), взвесь клеток фильтруют через ткань и полученную суспензию клеток разливают по 0,1 мл в лунки 96 ячейкового микропланшета. Через несколько дней (3-7) содержимое лунок используют как фидер.
Клетки продуцирующего клона снимают пипетированием, подсчитывают и разводят ростовой средой до конечной концентрации 50 клеток в 10 мл. Полученную взвесь разливают по 0,1 мл в лунки фидера. Видимые колонии появляются через 10-14 дней.
Существует возможность консервирования гибридом при низкой температуре. Гибридомы необходимо замораживать на ранних стадиях во время развития культур, не дожидаясь получения массовой культуры, желательно в середине логарифмической фазы. Таким образом, получают банк культур, что позволяет возобновить культуру в случае ее гибели. Стабильные культуры гибридом выдерживают замораживаем в течение нескольких раз. Затем гибридомы суспендируют в среде RPMI-1640 с добавлением 20% сыворотки плода коровы и ДМСО в количестве 50-70 г/л. Клетки первоначально охлаждают до 2-4°С, а затем выдерживают в сосуде Дьюара в течение 1-3 ч и переносят в жидкий азот [7].
МкАТ выделяют из асцитической жидкости мышей,
которым внутрибрюшинно инокулируют клетки продуцируемой гибридомы. Получение
асцитической жидкости состоит в следующем: за 3-10 дней до инокуляции клеток гибридомами
мышам внутрибрюшинно вводят мл вазелинового масла (полужидкого парафина или
пристана - 2,6,10,14 - тетраметилпептадекан) для индукции роста гибридом в
асцитной среде. 107 клеток гибридомы инокулируют мышам внутрибрюшиннои через
7-8 дней, в зависимости от накопления асцита, собирают асцитную жидкость.
Асцитную жидкость, полученную от разных мышей, объединяют и центрифугируют в
течение 20 мин при 2500 g (при 4°С). Супернатант асцитической жидкости,
содержащей неочищенный раствор МкАТ хранят при -50°С. В асцитической жидкости
мышей концентрация МкАТ может достигать - 5-10 мг/мл. На данной стадии
необходимо обращать внимание на генотип и пол животных. Замечено, что
использование гибридов мышей позволяет увеличить выход МкАТ в асцитической
жидкости. Использование гибридов также позволяет уменьшить скорость роста
опухолей. Увеличению выхода МкАТ способствует обработка полостей органов
(брюшной, грудной, сердечной) 0.3 М раствором натрия хлорида [7].
.5 ВЫДЕЛЕНИЕ И ОЧИСТКА МКАТ
Выделяют МкАТ путем аффинной хроматографии на
сорбенте А-сефароза. Асцитную жидкость размораживают и центрифугируют в течение
20 мин при 2500 g (4°С). Супернатант диализуют против 0,1 М натрий фосфатного
буфера, рН 8,0 в течение 12-16 ч при 4°С. Полученный диализат наносят на колонку
с протеин-А-сефарозой. После этого связавшиеся с сорбенотом иммуноглобулины
элюируют 0,1М цитратным буфером, рН 3,0. Полученный концентрат элюируют,
например, ультрафильтрацией и используют для получения лекарственных препаратов
[7].
.6 ПОЛУЧЕНИЕ ГОТОВОГО ПРЕПАРАТА
После проведения контроля (ВЭЖХ анализ) и
подтверждения соответствия раствора МкАТ предъявляемым требованиям раствор
стабилизируют полисорбатом 80, проводят стерилизующую фильтрацию через мембраны
с размером пор 0,22 мкм и разливают в первичную упаковку в асептических
условиях.
.7 КОНТРОЛЬ ГОТОВОГО ПРЕПАРАТА
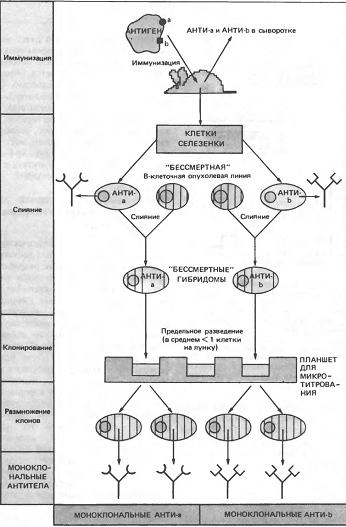
Необходимо отметить, что получение препаративного количества МкАТ возможно не только из асцитической жидкости мышей, но и путем культивирования гибридом в культуральной среде. После отбора гибридомных клеток, синтезирующих необходимые антитела, можно приступить к их массовому производству. Гибридомы переносят на ростовую среду и начинают культивирование. При культивировании можно проводить добавление питательной среды или ее отдельных компонентов. С производством МкАТ в ростовой среде связан вопрос с отмиранием клеток в зависимости от условий культивирования. Клетки в культуре гибнут, используя 2 механизма. Первый механизм - некроз, связанный с пассивной гибелью клеток под воздействием экстремальных факторов. Второй механизм - апоптоз, связанный с программированием клеточной гибели. Этот ответ клетки является результатом реализации ее генетической информации под влиянием индукторов апоптоза, таких как уровень истощения в среде глюкозы, витаминов и аминокислот. Данный фактор должен учитываться при разработке оптимальных условий производства МкАТ (рис. 1) и требует всесторонней валидации процессов производства.
Основные методы контроля препаратов МкАТ позволяют полностью оценить качество предлагаемых препаратов:
. Чистота и примеси - определение проводят методом ВЭЖХ.
. Активность. Определение проводят биологическими методами с обязательным использованием стандартного образца.
. Гомогенность. Определение проводят одним из вариантов электрофореза, например, электрофорезом в полиакриаламидном геле с додецилсульфатом при сравнении со стандартным образцом. Препарат считают гомогенным, если основные полосы образца и эталона совпадают по интенсивности.
. Значение рН (проводят потенциометрически).
. Содержание белка. Проводят УФ-спектрофотометрией.
. Бактериальные эндотоксины определяют с помощью LAL-теста.
. Стерильность.
. Вода - определяется для лиофилизированных препаратов по методу Фишера.
. Прозрачность, цветность, механические
включения.
3. КЛАССИФИКАЦИЯ ТЕРАПЕВТИЧЕСКИХ МКАТ
Среди препаратов, получаемых на основе моноклональных антител, выделяют 4 поколения, используемых в терапевтической практике Терапевтические МкАТ первого поколения по происхождению и составу представляют собой иммунноглобулины животных (в основном мыши). Несмотря на низкий уровень побочных эффектов, это поколение МкАТ имеет 3 основных недостатка:
ограниченная эффективность - Fc-фрагмент МкАТ животных не способен из-за видовых различий полноценно участвовать в иммунологических реакциях в организме человека;
развитие толерантности - чужеродное происхождение приводит к распознаванию МкАТ I поколения иммунной системой человека и выработке на них блокирующих антител (HAMA ответ);
«слабая» фармакокинетика - МкАТ животных нестабильны в кровотоке человека, быстро метаболизируются и выводятся.
После расшифровки последовательности генов иммуноглобулина человека и развития технологии получения синтетической кДНК на смену МкАТ первого поколения пришли химерные МкАТ - второе поколение. В этих препаратах антитело «собрано» из фрагментов молекул Ig человека и мыши, причем в приблизительно равных соотношениях. Данные антитела также могут приводить к HAMA-ответу.
Во второй половине 1990-х годов было разработано третье поколение МкАТ, в которых доля мышиных антиген-распознающих последовательностей составляет от 5 до 10%, а более 90% молекулы антитела представлены Ig человека.
Наконец, МкАТ четвертого поколения представляют собой полностью реконструированные молекулы Ig человека. Антитела четвертого поколения можно вводить многократно практически без риска развития блокирующего иммунного ответа, а фармакокинетические параметры этих препаратов приближены к эндогенным Ig человека (то есть продолжительность действия 4-8 нед, а период полувыведения в среднем составляет 20 дней)
В рамках III-IV поколения были разработаны несколько структурных модификаций МкАТ. К наиболее перспективным для клинического использования МкАТ можно отнести следующие:
Токсические МкАТ - антитела с пришитыми на Fc-фрагмент бактериальным токсином или радиоизотопом.фрагменты - моноспецифические участки МкАТ, способные связывать лиганд;
Биспецифические МкАТ - каждый из Fab-фрагментов антитела имеет свою специфичность, и эти антитела способны связывать два различных лиганда одновременно.
Фузион-протеины - химерные молекулы, в которых Fab-фрагменты антитела заменены последовательностями из других белков (например, этанерцепт представляет собой соединение рецепторов к фактору некроза опухолей с Fc-фрагментом молекулы IgG1.
Рассмотрим немного подробнее токсические МкАТ.
Иммунотоксины являются препаратами направленного действия и предназначены для
избирательной элиминации клеточных популяций. Иммунотоксины состоят из
векторной молекулы и цитотоксического агента. Из цитотоксических агентов
наиболее часто применяются растительные рибосоминактивирующие белки второго
типа (РИБ II), к которым относится рицин (R60) и вискумин (ML I). Несмотря на
то, что R60 синтезируются в семенах клещевины, а ML I - в листьях омелы белой,
оба белка имеют сходную третичную структуру и механизм действия. В составе ML I
и R60 входит связывающая (В) и каталитическая (А) субъединицы. В-субъединица
имеет галактосвязывающие центры и взаимодействуют с клеточными рецепторами,
содержащими терминальную галактозу. Каталитическая субъединица токсинов
проникает в цитоплазму и модифицирует 28 S РНК эукариотических клеток,
останавливая синтез белка на уровне трансляции. Замена В-цепи на векторную
молекулу в ряде случаев позволяет получить высокоэффективный препарат
направленного действия [5].
4. МЕХАНИЗМ ПРОТИВООПУХОЛЕВОГО ДЕЙСТВИЯ
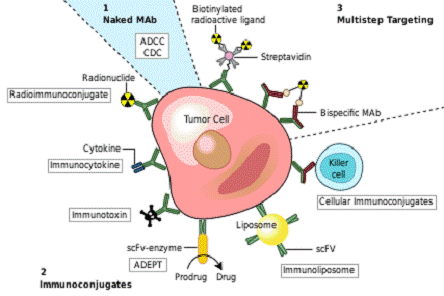
Одним из возможных способов для лечения рака
является использование препаратов, полученных на основе моноклональных антител,
которые связываются только с клеточными антигенами раковых клеток и индуцируют
иммунологическую реакцию против клетки мишени рака. Такое моноклональное
антитело может быть также модифицирован для доставки токсина, радиоизотопа,
цитокина или другого активного конъюгата (рис. 2).
Одним из широко используемых в терапии раковых заболеваний прпаратов является Ритуксимаб (ТМ «МАБТЕРА»). Антитело ритуксимаб представляет собой сконструированное генно-инженерным способом гибридное моноклональное антитело, направленное против эпитопа во внеклеточной части трансмембранной молекулы CD20. Антитело является гибридом антитела человека и мыши, в котором фрагмент антигенсвязывающей части (Fab) является мышиным, а фрагмент части Fc получен от человека. Белок CD20 экспрессируется на В-лимфоцитах, но не на стволовых клетках или на зрелых плазматических клетках. CD20 экспрессируется также на подавляющем большинстве В-клеточных лимфом. CD20 вовлечен в регуляцию трансмембранной проводимости кальция и прогрессии клеточного цикла, но точная его функция неизвестна.
При связывании ритуксимаба с CD20 опосредуется иммунологическое уничтожение клеток путем связывания комплемента с частью Fc-фрагмента с активацией каскада комплемента, а также путем активации антителозависимой клеточной цитотоксичности.
Особый интерес представляет препарат Авастин
(Бевацизумаб), который является первым препаратом МкАТ, ингибирующих ангиогенез
- рост сети кровеносных сосудов, поставляющих опухоли питательные вещества и
кислород. Мишенью препарата является белок, называемый фактором роста эндотелия
сосудов. (VEGF), который является важнейшим фактором ангиогенеза. Авастин
представляет собой рекомбинантные гуманизированные (химерные) МкАТ IgG1 с
молекулярной массой 149 кДа. Антитела образуют комплекс с VEGF и тем самым
блокируют его активность, в результате чего прекращается поставка крови к
опухоли.

Препарат РеоПро (Абциксимаб) ингибирует агрегацию тромбоцитов путем связывания с интактным глюкопротеиновым рецептором (GP II/IIIa), принимающим активное участие в агрегации тромбоцитов (рис. 3).
РеоПро ингибирует агрегацию тромбоцитов путем предупреждения связывания фибриногена, фактора Виллебранда и других адгезивных молекул с рецепторным участком GP II/IIIa на активированных тромбоцитах.
Пролиферация опухолевых клеток частично опосредована мембранными рецепторами и факторами роста, обнаруженными в организме и являющимися мишенями для нового класса таргетных препаратов, одним из которых является Цетуксимаб. Цетуксимаб представляет собой химерные МКАТ IgG1, которые связываются с экстрацеллюлярным доменом EGFR (рис.4).
противоопухолевый моноклональный антитело
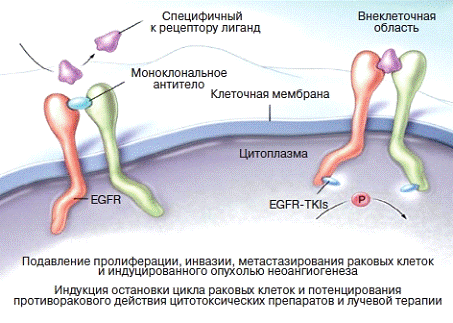
представляет собой трансмембранный гликопротеин. Его экспрессия определяется в 80-89% случаев рака толстой кишки. В роли лигандов EGFR наиболее часто выступают ростовые факторы EGF и фактор некроза опухоли-α (TGF-α), а также амфирегулин, эпирегулин, HB-EGF и β-целлюлин. Они взаимодействуют с рецептором, вызывая его гомодимеризацию (связывание лигандом двух идентичных рецепторов) или гетеродимеризацию (связывание мономера EGFR с другим представителем семейства, например HER2 или HER3). В результате происходит активация тирозинкиназы во внутриклеточном домене с последующим аутофосфорилированием рецептора и инициацией каскадов сигнальной трансдукции, участвующих в процессе пролиферации и опухолевой прогрессии. Цетуксимаб обладает высокой специфичностью и примерно в 10 раз большей аффинностью к рецепторам эпидермального фактора роста, чем его естественные лиганды EGF и TGF-α. Связывание цетуксимаба с EGFR приводит к димеризации рецепторов с последующим эндоцитозом и внутриклеточной деградацией комплекса антитело-рецептор, в результате чего плотность EGFR на поверхности клеток снижается.
Другой механизм наблюдается при структурном несовершенстве Fc-фрагментов МКАТ, а также при использовании в качестве лекарственных препаратов Fab-фрагментов и фузион-протеинов. Эти препараты играют роль рецепторных или химических антагонистов, препятствуя связыванию эндогенного лиганда со своим рецептором и активации внутриклеточной системы передачи сигнала. В результате происходит модификация биологического ответа (отсюда и название этой подгруппы - модификаторы биологических реакций). МКАТ, к Fc-фрагментам которых присоединены токсины или радиоизотопы (гемтузумаб озогамицин и ибритумомаб), представляют собой систему целевой доставки токсических агентов к определенной популяции клеток. После связывания с клеточным рецептором они интернализуются и создают внутри клетки-мишени концентрацию токсина или изотопа, несовместимую с ее жизнью. При этом они не проникают в нормальные клетки, и их максимальная концентрация в тканях и жидкостях организма значительно ниже токсической.