Материал: Похідні антранілової (2-амінобензойної) кислоти
Похідні антранілової (2-амінобензойної) кислоти
Міністерство освіти та науки України
Ніжинський державний університет імені Миколи Гоголя
Кафедра хімії
КУРСОВА РОБОТА
з органічної хімії
на тему: "Похідні антранілової (2-амінобензойної) кислоти"
Студента (ки) ІІІ курсу БХ-31 групи
напряму підготовки - бакалавр
спеціальності "Біологія та хімія"
Паладич Дар’ї Леонідівни
Керівник професор Суховеев В.В.
м. Ніжин - 2014 рік
Зміст
Вступ
І. Антранілова (2-амінобензойна) кислота її характеристика
1.1 Добування антранілової (2-амінобензойної) кислоти
1.2 Фізичні антранілової (2-амінобензойної) кислоти
1.3 Застосування антранілової (2-амінобензойної) кислоти.
II. Похідні антранілової (2-амінобензойної) кислоти
III. Похідні антранілової (2-амінобензойної) кислоти по карбоксильній групі
3.1 Добування та властивості похідних антранілової (2-амінобензойної) кислоти по карбоксильній групі
IV. Похідні антранілової (2-амінобензойної) кислоти по аміногрупі
4.1 Добування та властивості похідних антранілової (2-амінобензойної) кислоти по аміногрупі
V. Похідні антранілової (2-амінобензойної) кислоти по бензойному кільцю
5.1 Добування та властивості похідних антранілової (2-амінобензойної) кислоти по бензойному кільцю
Висновки
Список використаної літератури
Вступ
Актуальність теми: нині пошук біологічно активних речовин серед похідних антранілової кислоти має важливе значення. Ці сполуки широко поширені в природі, вони зустрічаються у складі ефірних масел і алкалоїдів деяких рослин, є продуктами життєдіяльності мікроорганізмів, у ряді живих організмів антранілова кислота і її похідні беруть участь у метаболізмі.
Завдяки наявності широкого спектру фармакологічної дії, який обумовлений різної структурної модифікацією, похідні антранілової кислоти знайшли застосування в медичній практиці.
Основою для поповнення арсеналу лікарських препаратів є синтез речовин, що володіють високою активністю і малої токсичністю. Пошук, вивчення і впровадження в клінічну практику відносно нешкідливих препаратів є одним з основних завдань фармацевтичної хімії. У цьому напрямку особливий інтерес представляють похідні N - заміщених антранілової кислоти, у зв'язку з їх низькою токсичністю і багатогранністю біологічних ефектів, а саме, наявності протизапальної та аналгетичної дії.
Мета роботи: Розглянути головні похідні антранілової кислоти, їх способи добування, фармакологічні властивості та застосування. Короткий огляд перспективних речовин для отримання ефективних лікарських засобів з протизапальною, аналгетичною дією і низькою токсичністю.
Завдання роботи:
1. Ознайомитися з антраніловою кислотою як ароматичною амінокислотою;
. Розглянути основні сфери застосування антранілової кислоти;
. Класифікувати похідні антранілової кислоти для полегшення огляду;
. Побачити взаємозв’язок будови та застосування похідних антранілової кислоти.
Об’єкт дослідження: антранілова кислота та її похідні.
Предмет дослідження: похідні антранілової кислоти.
Наукова новизна роботи: за останні роки синтезовано багато нових похідних антранілової кислоти, які знайшли своє застосування в фармацевтиці, медицині та промисловості.
Проведено аналіз результатів дослідження та синтезу, різними країнами, біологічно активних речовин в порівнянні з еталонними речовинами, анестезуючої та знеболюючої дії.
Таким чином, похідні антранілової кислоти мають важливе значення саме в медицині, адже більшість похідних відносяться до не стероїдних протизапальних препаратів.
Також, окрім медичного направлення похідні можуть
застосовуватися в залежності від однієї важливої властивості, а сама
антранілова кислота легко адсорбується різного роду сорбентами, тому вона може
бути рекомендована для використання у вимірювальних трансформаторах, силових
трансформаторах, не обладнаних термосифонного фільтрами, а також в
маслонаповнених приводах і реакторах.
І. Антранілова (2-амінобензойна) кислота її характеристика
Антранілова кислота (2-амінобензойна кислота) NH2C6H4COOH,
молярна маса 137,14 г/моль. Антранілова кислота амфотерна, (lgK1 =
5, lgK2 = 12) тобто проявляє як кислотні так і основні властивості.
Аміногрупа і карбоксильна група, приєднані в кільцеву структуру [54].
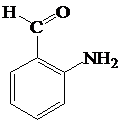
Оскільки ці дві групи є полярні, це органічна сполука високо розчинна у воді. Її іноді називають вітамін Л. Антранілова кислота, амінокислота групи заміщених бензойної кислоти в орто-положенні. Вперше отримана російським хіміком академіком Фрицше при дії їдкого калію (КОH) на індиго [55].
Антранілова кислота має 3 ізомери: п-амінобензойну кислоту
та м-амінобензойну кислоту:
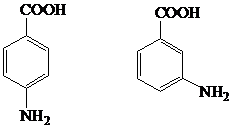
Антранілова кислота має суттєве біологічне значення. 2-амінобензойна кислота слугує інтермедіатором в різних шляхах біосинтезу. Ізомери антранілової кислоти отримують відновленням відповідних нітробензойних кислот. П-амінобензойна кислота бере участь в комплексі біосинтезу вітамінів групи В і слугує бактеріальним фактором росту, для якого сульфамідні препарати є антагоністами [55].
Як вже відомо антранілова кислота це орто-похідна бензойної
кислоти, отже антранілова кислоти передбачено буде мати інші властивості ніж
бензойна. Це явище досліджував М.І. Шейх-Заде в своїй роботі " Оценка
энергии димеризации антраниловой кислоты", ця робота також пояснює
властивості антранілової кислоти. Задачею роботи Шейх-Заде є вимірювання
константи димеризації КД, зміна ентальпії антранілової кислоти в
розчині ССl4 з метою пояснення впливу внутрішньо водневого зв’язку і
електронних ефектів замісника в отро-положенні на значення ентальпії, яку можна
вважати енергією димеризації. Ця робота показала, що у використанні
екстремальних умов, як мономери, так і циклічні димери антранілової кислоти
знаходяться в конформації з внутрішньо водневими зв’язками і існує рівновага
між димерами і мономерами антранілової кислоти:
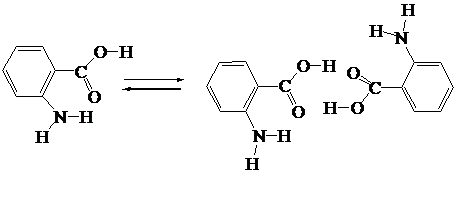
Цю рівновагу можна визначити двома різними способами. Ця рівновага кількісно дорівнює одиниці [57].
На основі цього можна зробити висновок, що в антраніловій
кислоті зменшення електронодонорної здатності карбоксильної групи, зумовлене
участю цієї групи в внутрішньо водневих зв’язках і впливом електронних ефектів
замісника в отро-положенні, яка компенсується збільшенням протодонорної
здатності аміногрупи. Ці результати можна застосувати лише для
орто-амінобензойної кислоти, для її ізомерів, вони будуть невірні [58]. Зміна
термодинамічних характеристик міжмолекулярних водневих зв’язків дозволяє
говорити про протодонорних і протоакцкпторних властивостях антранілової
кислоти. В ролі донора виступає карбоксильна група, в ролі акцептора -
аміногрупа. Між цими групами виникають внутрішньо водневі зв’язки типу N-H….
O=C, N-H…. O, O-H…. N. Можна говорити, що мономерні молекули антранілової
кислоти можуть існувати, по меншій мірі, в чотирьох конформація (само
асоціацій), які залежать від агрегатного стану (газ, рідина, тверде тіло), від
виду розчинника, концентрації, температури [57].
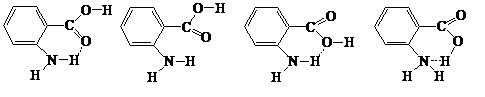
І ІІ ІІІ
ІV
В звичайних умовах в розчині існує лише структура І, і не реалізується 3 структури. Це може бути обумовлено:
. При утворенні внутрішньо водневого зв’язку N-H…. O=C відбувається збільшення електронної щільності на атомі водню групи N-H і протонодонорна здатність цієї групи зменшується.
. Розбавлений розчин не сприяє утворенню таких самоасоціатів [55].
1.1 Добування антранілової (2-амінобензойної) кислоти
В промисловості антранілову кислоту отримують:
1) дією водного розчину NH3 на фталевий ангідрид
(рН 7,5-8,5; 40°C) і наступною взаємодією отриманої Na-солі фталамінової
кислоти з розчином NaOCl
<#"822490.files/image005.gif">
) дією лужного розчину фталіміда NaOCl <#"822490.files/image006.gif">
Лабораторний метод синтезу:
Нагрівають суміш, яка складається з 7,5 тонко подрібненого
фталевого ангідриду і 3г сечовини, в колбі на 100 мл на повітряній бані при
температурі 130-135°C. Реакція починається вспіненням, причому температура
піднімається до 160°C. По закінченню реакції отримують тверду пористу масу,
яку, з добавкою невеликої кількості води, подрібнюють і відфільтровують в
воронці Бюхнера. Осад добре віджимають на фільтрі і сушать. Вихід 6г [62].
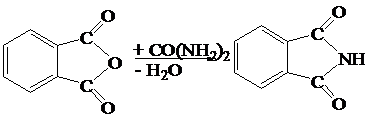
В порцеляновий стакан на 100 мл поміщають розчин 8г їдкого натру в 40 мл води і охолоджують до - 5°C. При перемішуванні до нього приливають 2 мл брому, а потім суспензію 6 г фталіміда в 8 мл води.
Після цього охолоджену суміш видаляють і реакційну масу
залишають при кімнатній температурі, періодично перемішуючи. Коли температура
реакційної суміші досягне 15-20°C, вносять 4,8г твердого їдкого натра,
подрібненого в порошок і нагрівають до 80°C. Гарячий розчин фільтрують через
складчастий фільтр і після охолодження розчин нейтралізують 12,8 мл
концентрованої соляної кислоти. Антранілову кислоту осаджують 6 мл льодяної
ацетатної кислоти і залишають не менше ніж на 2 години кристалізуватися.
Підкислення реакційної суміші треба проводити обережно, так як проходить сильне
зпінення при нейтралізації соди яка утворилась в результаті реакції. Випавши
антранілову кислоту відділяють на воронці Бюхнера, промивають холодною водою і
сушать на повітрі. Вихід 4,8г. Тпл =144°C [43].
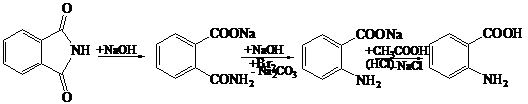
Альтернативні і більш детальні способи добування антранілової кислоти:
За запропонованим способом процес здійснюють шляхом змішування розчину фталіміду натрію або фталаміната натрію з лужним розчином гіпохлориту натрію при мольному співвідношенні фталімід натрію або фталамінат натрію: гіпохлорит натрію: гідроксид натрію в межах 1: 1,005-1,06: 2,0-2,05 при температурі від - 15 до +15°C з наступною нейтралізацією надлишку гіпохлориту натрію відновлює агентом при 15-35°C і витримкою реакційної суміші при 40 - 85°C. Як розчин фталіміду натрію використовують розчин з масовою часткою фталіміду натрію в межах 23-28,7 %, а в якості розчину фталаміната натрію використовують розчин з масовою часткою фталаміната натрію в межах 25-35 % [43]. Пропонований спосіб дозволяє збільшити вихід цільового продукту в середньому на 4,6-8,3 % і знизити видаткову норму гіпохлориту натрію на 0,5-29,3 % [45].
Відомий безперервний спосіб отримання антранилової кислоти, що включає взаємодію фталаміната або фталіміду лужного металу з гіпогалогенідом у водному середовищі в присутності лугу і каталізатора: брому, йоду або аміду формули XNRR ', де Х = С1, Br або Н; R = SO3Н, сульфонатні або сульфонамідні група; R '= H, алифатический залишок, С1 або Вr. Недоліками даного способу є використання додаткового сировинного компонента - каталізатора і підвищена видаткова норма восстанавливающего агента - NaHSO3 [2].
Відомий спосіб отримання АК, що включає взаємодію лужного розчину фталіміду з надлишком розчину гіпогалогеніда лужного металу при мольному співвідношенні фталімід: гіпогалогенід в межах 1: 1,2-2,2, краще 1: 1,6-1,9, при температурі не більше 40°C, краще при 25°C, з наступним дією відновлюючого агента, краще Na2S2O5, взятого в кількості 0,1-1 різниці мольного надлишку гіпогалогеніда лужного металу щодо фталіміду. Концентрація фталіміду в лужному розчині знаходиться в межах 10-35%, Краще 10-22% При мольному співвідношенні фталімід: луг в межах 1: 1,2-3,5, краще в межах 1: 2,2-2,8.
Недоліками цього способу є використання великого надлишку гіпогалогеніду - від 20 до 120%, необхідність його нейтралізації відновником і утворення значної кількості стічних вод з високим солевмістом [4].
Найбільш близьким за технічною сутністю до пропонованого є спосіб отримання антраниловой кислоти, що включає взаємодію розчину фталіміду або фталаміната лужного металу з надлишком гіпохлориту лужного металу при температурі близько 0°C в присутності лугу, зазвичай у вигляді 40 % водного розчину, яку додають до реакційної суміші поступово, частинами, причому надлишок гіпохлориту усувають до досягнення 50 % конверсії фталіміду або фталаміната лужного металу, але після додавання останньої порції лугу, за допомогою відновника: аміаку, амінів і їх солей, сечовини, похідних і солей сечовини, нітрилів і амідів карбонових кислот, меламіну, перекисів та інших речовин. Мольне співвідношення фталімід або фталамінат лужного металу: гіпохлорит знаходиться в межах 1: 1,01-1,3, а мольне співвідношення фталімід або фталамінат лужного металу: луг - в межах 1: 1,9-3,5. Цільовий продукт виділяють з розчину дією сірчаної кислоти [23].
Недоліками цього способу є відносно невисокий вихід цільового продукту (79,3%), досить значний надлишок (до 30 % від теорії) гіпохлориту лужного металу і пов'язана з ним підвищена видаткова норма відновника [3].
1.2 Фізичні антранілової (2-амінобензойної) кислоти
Антранілової кислоти - безбарвні кристали; температура плавлення 145°C; переганяється. Розчинність (г в 100 г розчинника): у воді - 0,35 (14 C), 90% етанолі - 10,7 (9,6°C), бензолі - 1,8 (12°C), ефірі - 16 (6,8°C); добре розчинна у гарячих хлороформі, етанолі, піридині. Ця речовина помірно токсична. Може бути шкідливо для здоров'я при вдиханні або абсорбція через шкіру. Це може викликати роздратування шкіри і очей. При нагріванні розкладається і виділяє токсичні гази карбон (ІІ) оксид, карбон (ІV) оксид і оксиди азоту [33].
Симптоми отруєння антраніловою кислотою можуть включати нудоту, блювоту, ацидоз, висип, лихоманка, і, можливо, гепатит, алергічні реакції і ціаноз (посиніння шкіри). Контакт зі шкірою може викликати подразнення, свербіж, дерматити. Потрапляння очі може викликати роздратування. Вплив антранілової кислоти може викликати подразнення дихальних шляхів, подразнення слизової оболонки, кон'юнктивіт і запалення печінки [27].
Допомога при потраплянні антранілової кислотою на:
Очі: промити очі водою або фізіологічним розчином протягом 20-30 хвилин, одночасно викликаючи в лікарні або в токсикологічний центр. Не наносити ніяких мазей, масел, ліки чи потерпілого очі без вказівок лікаря. Негайно звернутись, після промивання очей, в лікарню, навіть якщо ніяких симптомів (таких як почервоніння або подразнення) не має [61].
Шкіру: акуратно вимити всі уражені ділянки шкіри водою з милом. Якщо симптоми, такі як почервоніння або подразнення розвиваються, викликати лікаря.
При вдиханні: глибоко подихати свіжим повітрям. Якщо симптоми (такі як свистяче дихання, кашель, задишка, або печіння в роті, горлі або грудей) проявляються, звернутися до лікаря [19].
При проковтуванні: не викликати блювоту. Якщо потерпілий знаходиться у свідомості і не має судом, дають 1 або 2 склянки води. Подзвонити в лікарню або в токсикологічний центр. Якщо спостерігаються судоми або жертва в несвідомому стані не вливати нічого в рот людині, переконатися, що дихальні шляхи відкритими і покласти потерпілого на бік голову нижче, ніж тіло [17].
антранілова амінобензойна кислота карбоксильний
1.3 Застосування антранілової (2-амінобензойної) кислоти.
Антранілова кислота і її похідні широко застосовуються при отриманні лікарських засобів, харчових добавок, пестицидів, а також у синтезі різноманітних гетероциклічних сполук. Проміжний продукт при синтезі індиго і інших азобарвників. Похідні застосовуються в виробництві азобарвників і парфумерних речовин [21]. Для парфумерії найбільш важливі ефіри NH2C6H4COOR - метилантранілат, які мають запах квітів апельсинового дерева. Антранілова кислота застосовується в якості напівпродукту у виробництві різних барвників, лікарських і запашних речовин [30].