Материал: Перспективные композиционные и керамические материалы
вижность дислокаций и диффузионную подвижность. Своеобразная кристаллическая структура накладывает отпечаток на характер взаимодействия Si3N4 с тугоплавкими соединениями и металлами, сказывается на анизотропии некоторых физических свойств. Наконец, небольшой температурный коэффициент линейного расширения и низкая плотность делают нитрид кремния особенно привлекательным в качестве термопрочного и жаропрочного материала с высокимиудельными характеристиками.
Плотность α-Si3N4 составляет 3,148 г/см³, β-Si3N4 – 3,211 г/см³; средний температурный коэффициент линейного расширения в интервале температур 0–1000 °С равен 3,64·10–6 К–1 для α-Si3N4 и 3,39·10-6 К–1 для β-Si3N4. Термическое расширение нитрида кремния анизотропно.
Микротвердость β-Si3N4 ниже микротвердости α-Si3N4. Значения микротвердости для α-Si3N4 анизотропны: максимальная микротвердость (34,85 ГПа) наблюдается для плоскостей (1010), минимальная (26,2 ГПа) – для плоскостей (0001). Зависимость твердости от температуры изучена мало, отмечена практически линейная зависимость в ин-
тервале 20–1600 °С.
Для получения порошков Si3N4 характерны обычные для порошковой металлургии приемы – методы прямого синтеза в различных вариантах, карботермическое восстановление, газофазные реакции синтеза и разложения, а также механическое измельчение как дополнительный вид обработки. В табл. 2.1 приведены этиметоды и некоторые их разновидности.
Таблица 2.1
Основные методы синтеза порошков нитрида кремния и их разновидности
Метод |
Основные реакции |
Основные разновидности |
|
метода |
|||
|
|
||
Прямой синтез |
3Si+2N2→Si3N4 |
Самораспространяющийся |
|
высокотемпературный |
|||
компонентов |
3Si+4NH3→Si3N4+6H2 |
синтез (СВС) |
|
|
|
Плазмохимический синтез |
|
Карботермическое |
3SiO2+6C+2N2→Si3N4+6CO |
– |
|
восстановление |
|||
|
3SiCl4+16NH3→ |
Плазмохимический синтез. |
|
Газофазный синтез |
Si3N4+12NH4Cl |
||
Лазерный синтез |
|||
|
3SiH4+4NH3→Si3N4+12H2 |
||
|
|
||
Диссоциация |
3Si(NH)2→ |
|
|
Si3N4+2NH3(1/n)[SiR2–NR]n→ |
Лазерное индуцирование |
||
(пиролиз) |
Si3N4+RH+H2 |
|
|
|
|
36
Синтез Si3N4 из простых веществ осуществляется взаимодействием кремния с азотом или аммиаком в печах сопротивления, плазмохимическим синтезом и самораспространяющимся высокотемпературным синтезом.
Прямое азотирование Si проводят в атмосфере N2, N2/H2 или NH3 в печах сопротивления при температурах выше 1100 °C, но ниже точки плавления кремния (1412 °С). Данная реакция является экзотермической и должна строго контролироваться, чтобы предотвратить плавление кремния.
В России для получения порошка Si3N4 большое распространение получил метод СВС, поскольку не требует сложной аппаратуры и характеризуется высокой производительностью. Особенностью продукта, получаемого в результате СВС, является его неравновесность из-за высокой концентрации структурных дефектов, возникающих в условиях значительных градиентов температуры (до 2000 К), экстремально высоких скоростей нагрева и охлаждения. При СВС-процессе выход Si3N4 определяется давлением азота и дисперсностью исходного кремния.
Метод плазмохимического синтеза (ПХС) позволяет изготавливать порошки с повышенной химической активностью по сравнению с грубодисперсными порошками, получаемыми другими методами. Высокая скорость движения компонентов в струе низкотемпературной плазмы (5000–10000 К) обеспечивает закаливание продуктов реакции, в результате чего формируются порошки с большой долей аморфного Si3N4 и нанокристаллитов α- и β-фазы (~ 20 нм).
Метод газофазного синтеза используют преимущественно для получения наноразмерных порошков нитрида кремния, широко применяя реакции взаимодействия галогенидов кремния (SiCl4, SiB4) или силана SiH4 с аммиаком, осуществляемые в условиях плазмохимического, лазерного или обычного теплового нагрева.
В реакционную камеру аммиак и смесь SiCl4 –H2 вводят раздельно. Синтез паровой фазы происходит в диапазоне температур от 800 до 1400 °C с образованием аморфного Si3N4. Кристаллизация аморфного порошка осуществляется при температуре 1300–1500 °С.
Процесс термической диссоциации диимида кремния Si(NH)2 состоит из трех основных этапов: а) синтеза Si(NH)2; б) термического разложения Si(NH)2; в) кристаллизации. На первом этапе, тетрахлорид кремния (SiCl4) и аммиак (NH3) вступают в реакцию при 1550 °C
37
ватмосфере азота с образованием Si(NH)2 и хлорида аммония. На следующем этапе Si(NH)2 термически разлагается при температуре около 1000 °C для получения аморфного порошка нитрида кремния. На заключительном этапе аморфный порошок подвергается кристаллизации
вдиапазоне температур 1300–1500 °С с образованием α-Si3N4 порошка. Карботермическое восстановление оксида кремния в среде азота
давно привлекает к себе внимание исследователей как метод, позволяющий использовать недефицитное сырье (например, рисовую шелуху). Получение Si3N4 восстановлением оксида кремния углеродом с одновременным азотированием известно с конца XIX века. В качестве исходных веществ используют либо кремниевую кислоту, либо кремнозем, а восстановителями служат: аморфный углерод, графит, карбид кремния, нефтяной кокс, смолы.
Процесс включает в себя азотирование смеси углерода и кремния в атмосфере азота при температуре в диапазоне от 1400 до 1500 °C. Характеристики порошков Si3N4, полученные в результате карботермического восстановления, зависят от многих факторов, а именно соотношения C/SiO2, скорости потока азота, температуры реакции, размера частиц и удельной поверхности диоксида кремния иуглерода и примесей.
Возможность получения высокоплотных нитридкремниевых материалов и параметры технологических процессов определяются в значительной степени характеристиками исходных порошков. Общими требованиями, предъявляемыми к порошкам Si3N4, являются следующие:
–высокая дисперсность и однородность частиц. Для большинства технологий требуются порошки с удельной поверхностью 10–25 м2/г, позволяющие получать высокоплотные материалы с мелкозернистой структурой;
–высокое содержание α-фазы, так как процессы уплотнения
иструктурообразования нитридкремниевой керамики связаны с сопут-
ствующим фазовым превращением α-Si3N4 → β-Si3N4, которое происходит по механизму перекристаллизации через жидкую фазу;
–контролируемое содержание кислорода. Кислород как основная примесь присутствует в порошке нитрида кремния в адсорбированном
виде, а также в виде SiО2. Содержание кислорода определяет количество жидкой фазы при спекании, влияет на фазовый состав и структуру
исвойства материала;
–минимальное содержание металлических примесей и углерода. Наличие в порошке железа, кальция и магния приводит к снижению вязкости жидкой фазы при спекании, повышает конечную плотность на
38
1–5 %, но способствует росту зерен Si3N4 и образованию более грубой зернистой структуры керамики, определяет уменьшение высокотемпературной прочности и увеличение скорости деформации при воздействии механических напряжений. Присутствие углерода уменьшает количество жидкой фазы и изменяет ее состав, подавляет уплотнение и способствует укрупнению структуры.
Также оговаривается содержание свободного кремния, которое может доходить до 1–2 %. Высоким содержанием свободного кремния особенно отличаются порошки, полученные азотированием кремния. Примеси галогенов могут также приводить к деградации свойств порошков. Содержание фтора и хлора для большинства марок оговаривается на уровне 0,001–0,009 мас.%.
В последнее время в связи с развитием работ в области нанокристаллических материалов особое внимание уделяется такой характеристике, как агломерируемость. Наличие агломератов сказывается на образовании в структуре спеченных материалов довольно крупных межчастичных пор, ухудшающих физико-механические и другиесвойства.
Характеристики порошка нитрида кремния определяются методом его синтеза и качеством исходных реагентов (табл. 2.2).
|
|
|
|
Таблица 2.2 |
Некоторые характеристики порошков нитрида кремния |
||||
|
|
|
|
|
Характеристика |
Прямое |
Газофазный |
Карботермиче- |
Диссоциация |
ское восста- |
||||
|
азотирование |
синтез |
новление |
Si(NH)2 |
|
|
|
|
|
Удельная |
8–25 |
3,7 |
4,8 |
1 |
поверхность, м2/г |
|
|
|
|
Содержание |
1,0–2,0 |
1,0 |
1,6 |
1,4 |
кислорода, мас.% |
|
|
|
|
Содержание |
0,1–0,4 |
– |
0,9–1,1 |
0,1 |
углерода, мас.% |
|
|
|
|
Примеси металлов, |
0,07–0,15 |
0,03 |
0,06 |
0,005 |
мас.% Σ Fe, Al, Ca |
|
|
|
|
Кристалличность, % |
100 |
60 |
100 |
100 |
Содержание |
95 |
95 |
95 |
85 |
α фазы, % |
|
|
|
|
В начале 70-х годов прошлого века появились материалы, названные по буквам составляющих элементов – Si, Al, О, N – сиалонами. Алюминий может быть заменен другими металлами – Be, Ga, Sc т.д. Поэтому этот класс соединений называют симонами.
39
Сиалоны представляют собой сложные фазы типа (Si, Al)(O, N)4, которые можно рассматривать как алюмосиликаты, в которых кислород частично замещен азотом.
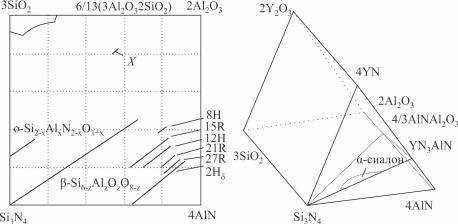
Сиалон был получен при изучении системы Si3N4-SiО2-Al2O3-AlN. В системе выделяют несколько видов сиалонов: гексагональный β-сиалон, аналогичный β-Si3N4, имеющий состав Si6-xAlxOхN8-x, где 0 < x ≤ 4,2; гексагональный α-сиалон, аналогичный α-Si3N4 (рис. 2.6). Фаза α-сиалона стабилизируется соответствующими добавками и имеет состав: Мех(Si, Al)12(O, N)16, где 0 < x ≤ 2, Me – Li, Na, Ca, Mg, Y или РЗЭ.
а |
б |
Рис. 2.6. Расположение сиалоновых фаз на диаграмме состояния: а – четырехэлементной системы Si-Al-O-N; б – пятиэлементной системы Y-Si-Al-O-N
Наиболее широко используют β-сиалоны. Структура β-сиалона представляет собой твердый раствор алюминия и кислорода в кристаллической решетке Si3N4. Практически β-сиалоны получаются синтезом из порошков Si3N4 – Al2O3 – AlN или Si3N4 – SiО2 – Al2O3 .
Сиалоновые порошки получают смешиванием с последующим спеканием компонентов, содержащих элементы сиалоновой системы
(Si, SiO2, Si3N4, Si2ON2, Al, Al2O3, AlON, AlN) в различных соотноше-
ниях в зависимости от требуемого состава сиалона. После спекания при температуре примерно 1700 °C в течение 1–3 ч полученный материал подвергается размолу.
40