Материал: Ответы экзамен горения и взрыва
–вещество полностью сгорает (недожог отсутствует);
– потери теплоты отсутствуют
(процесс адиабатный).
24. Расчет адиабатической температуры продуктов стехиометрически полного горения техногенного вещества.
Температура горения зависит от концентрации горючего в горючей смеси. Если горение происходит с избытком воздуха, т.е. при α > 1, то выделившееся в результате сгорания тепло частично затрачивается на нагрев этого лишнего воздуха. В горючей смеси с α < 1 из-за недостатка воздуха полное сгорание горючего вещества произойти не может, поэтому и тепловыделение в такой смеси будет неполным. В следствии этого, максимальная температура горения будет при сгорании стехиометрической смеси, т.е. при α = 1. Адиабатическую температуру горения рассчитывают для стехиометрической смеси, т.е. при условии α = 1 по формуле Qн = ∑ { Hпгi(TАД) – Hпгi(T0)}* Vпгi, (см.22)
где Qн – низшая теплота сгорания вещества; Hпгi(TАД) и Hпгi(T0) – значения теплосодержания (энтальпии) i-го продукта горения при температуре горения и начальной температуре; Vпгi – объем i-го продукта горения. Методом интерполяции находят TАД, которая является решением уравнения для Qн , с допустимой погрешностью.
25. Воспламенение горючей газообразной смеси.
Тепловое самовоспламенение
Горение в горючих смесях ( воспламенение) может возникнуть в результате их самовоспламенения, зажигания внешним источником или самовозгорания. Самовоспламенение и зажигание характерны для газообразных, жидких и твердых веществ. Самовозгорание характерно для твердых материалов (особенно находящихся в мелкораздробленном состоянии) или высококипящих жидкостей, распределенных на материалах с развитой поверхностью.
Теория самовоспламенения (теория теплового взрыва) рассматривает стационарное в тепловом отношении состояние системы «горючее вещество – окислитель», при котором теплоотвод равен тепловыделению. Эта теория (ак. Семенов Н. Н.) позволяет определить условия достижения критического состояния, при дальнейшем развитии которого, происходит самовоспламенение. Рассматривается сосуд объёмом V, в котором находится горючая смесь. Температура стенок сосуда поддерживается постоянной и равна Т0. При температуре смеси Т в ней будет протекать химическая реакция со скоростью W, подчиняющаяся закону Аррениуса: W = К0спехр (—E/RT)где с — концентрация кислорода; п — порядок реакции; Е — энергия активации; R — универсальная газовая постоянная.
Скорость выделения тепла в результате протекания реакции q1 равна: q1= q К0 сп ехр (—E/RT)V,
где q — тепловой эффект реакции. Выделившееся тепло расходуется на нагрев смеси и на потери в окружающую среду. Количественно потери тепла q2 оцениваются: q2 = α S (T-T0), где α –коэффициент теплоотвода; S — площадь поверхности стенок сосуда.
Изменение подвода и отвода тепла в зависимости от температуры, выражаемое приведенными соотношениями иллюстрируется на рис. Три кривые q2 (Т) соответствуют трем значениям Т0. При установившемся состоянии системы q1 равно q2, и температура в сосуде определится как абсцисса точек пересечения кривых q1 (Т) и q2 (Т). Из рис. видно, что кривые прихода и отвода тепла пересекаются в двух точках, а иногда в одной.
В первом случае: нагрев смеси,
имевшей начальную температуру Т0. Нагревание смеси
прекратится и система достигнет равновесного состояния, когда температура газа
станет равной Та, соответствующей точке пересечения а
кривых q1 и q2. Такое равновесие будет
устойчивым. Вторая точка пересечения кривых б находится в области
более высоких температур, и тепловой режим в этом случае 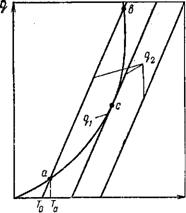 будет неустойчивым. При отклонении
от равновесного состояния, соответствующего точке б, система в
него уже не возвращается. Повышение начальной температуры Т0 стенок
сосуда приводит к смещению вправо кривой теплоотвода q2. Значение стационарной температуры
Та будет при этом плавно возрастать. При некоторой
температуре стенки кривые подвода и отвода тепла будут касаться одна другой,
как это показано при среднем положении кривой теплоотвода на рис. Точка касания
кривых с является граничной точкой существования стационарного
режима. Небольшое повышение температуры стенки будет сопровождаться превышением
прихода тепла над отводом, что вызовет повышение температуры смеси и
соответственно увеличение скорости взаимодействия горючего с окислителем. Процесс,
характеризующийся переходом от медленно протекающей реакции к прогрессивно
ускоряющемуся выгоранию смеси, является процессом самовоспламенения.
будет неустойчивым. При отклонении
от равновесного состояния, соответствующего точке б, система в
него уже не возвращается. Повышение начальной температуры Т0 стенок
сосуда приводит к смещению вправо кривой теплоотвода q2. Значение стационарной температуры
Та будет при этом плавно возрастать. При некоторой
температуре стенки кривые подвода и отвода тепла будут касаться одна другой,
как это показано при среднем положении кривой теплоотвода на рис. Точка касания
кривых с является граничной точкой существования стационарного
режима. Небольшое повышение температуры стенки будет сопровождаться превышением
прихода тепла над отводом, что вызовет повышение температуры смеси и
соответственно увеличение скорости взаимодействия горючего с окислителем. Процесс,
характеризующийся переходом от медленно протекающей реакции к прогрессивно
ускоряющемуся выгоранию смеси, является процессом самовоспламенения.
Процессы самовоспламенения могут иметь тепловой, цепной и комбинированный цепочечно-тепловой характер. Формулировка основных положений теории цепных реакций дана в трудах Н. Н. Семенова и его школы. Сущность этой теории заключается в следующем. Инициированная каким-либо образом химическая реакция приводит к образованию активных центров. В свою очередь, эти центры вызывают химические превращения, при которых вновь создаются активные центры, и в конечном итоге возникает цепная реакция.
Начавшийся процесс химических превращений будет продолжаться до тех пор, пока на одном из звеньев начальный центр не вступит в реакцию обрыва. Обрыв цепи может происходить либо в объеме реагирующей смеси при взаимодействии начальных центров реакции между собой или с какими-либо примесями, либо на поверхности стенок реакционного сосуда.
Процессом зарождения цепи всегда является эндотермическая реакция. Поглощение энергии необходимо для разрыва внутримолекулярных связей. Энергия активации, необходимая для элементарных актов продолжения цепи, обеспечивается тепловым эффектом одного из экзотермических процессов продолжения цепи.
Реакции,
протекающих по механизму прямых цепей, не могут привести сами по себе к
возникновению самовоспламенения поскольку длина прямой цепи всегда конечна и
скорость образования начальных центров цепей при начавшейся реакции убывает
(вследствие расходования компонентов). Самовоспламенение является
следствием протекания разветвленных цепных реакций, отличающихся
тем, что в них наряду с актами продолжения цепи возникают и такие реакции, в
которых взамен одного прореагировавшего активного центра возникают по крайней
мере два новых.
27. Температура самовоспламенения.
Температура самовоспламенения — наименьшая температура горючего вещества, при которой происходит резкое увеличение скорости экзотермической реакции с воздухом, заканчивающееся воспламенением. Определяют в условиях специальных испытаний, характеризующихся идентичностью параметров теплоотвода.
Температура самовоспламенения — минимальная температура, при которой в нагретой газовоздушной смеси начинается самопроизвольный (т. е. без внешнего подвода теплоты) процесс горения, за счет выделения теплоты горящими частицами газа.
Температура самовоспламенения не является фиксированной для данного газа и зависит от многих параметров: его содержания в газовоздушной смеси, степени однородности смеси, формы и размеров сосуда, в котором смесь нагревается, быстроты и способа ее нагрева, каталитического влияния стенок сосуда, давления, под которым находится смесь. Точный учет перечисленных факторов весьма сложен, поэтому на практике, например, при оценке взрывоопасности, пользуются экспериментальными данными.
Температуры самовоспламенения горючих газов в кислороде несколько ниже, чем в воздухе. Введение в состав газов балластных примесей (азота и диоксида углерода) приводит к увеличению температуры самовоспламенения. Присутствие в сложных газах компонентов с низкой температурой самовоспламенения приводит к снижению температуры самовоспламенения смеси.
29. Методы определения температуры самовоспламенения.
Температура самовоспламенения зависит от многих факторов:
от химического состава;
от его физических свойств (теплоемкость, теплопроводность);
от времени индукции ti;
от давления в сосуде Р;
от материала стенок сосуда;
от начальной температуры стенокTS;
от метода определения температуры самовоспламенения.
Существует целый ряд экспериментальных методов определения температуры самовоспламенения газовых смесей. Основными из них являются:
метод впуска заранее заготовленной холодной смеси в эвакуированный нагретый сосуд;
метод нагревания компонентов смеси раздельно и затем смешивание в потоке нагретого сосуда (метод концентрических трубок).
метод адиабатического сжатия заранее заготовленной смеси.
30. Методы экспериментального определения температуры самовоспламенения. Существует четыре основных метода определения температуры самовоспламенения, которые отличаются друг от друга главным образом способами нагрева, смешения газов или паров горючего с окислителем. Характерной особенностью метода является то, что здесь исключается возможность непосредственного участия стенок в реакциях воспламенения. 3. Метод «струй».
Два потока — горючего газа или пара и окислителя нагреваются раздельно. Самовоспламенение происходит при смешении этих потоков на выходе из нагревательных труб, без соприкосновения реагирующей смеси с горячими стенками, но при совершенно неопределенном составе смеси перед ее воспламенением. 4. Метод «капли».
Этот метод наиболее распространен в лабораторной практике для определения температуры самовоспламенения паров жидкостей. Испытуемая горючая жидкость подается каплями из бюретки в нагретый тигель. Через него пропускается с регистрируемой скоростью кислород, воздух или другой окислитель. Температуру тигля, при которой капля самовоспламеняется, принимают за температуру самовоспламенения. Здесь, как и в методе струй, неопределенным является состав смеси перед ее воспламенением.
31. Самовоспламенение - резкое увеличение скорости экзотермических объемных реакций, сопровождающееся пламенным горением и/или взрывом.
Температура самовоспламенения - наименьшая температура окружающей среды, при которой в условиях специальных испытаний наблюдается самовоспламенение вещества.
32. Принудительное воспламенение или зажигание.
Зажигание - принудительное воспламенение рабочей смеси в камере сгорания двигателя внутреннего сгорания. Имеют распространение две системы зажигание: батарейное и от магнето. При батарейном зажигании электрический ток низкого напряжения (6-12 в) от аккумуляторной батареи через выключатель поступает в первичную обмотку индукционной катушки зажигания. Индуктированный во вторичной обмотке катушки зажигания ток высокого напряжения (12 000-15 000 в) подводится к ротору распределителя зажигания. Ток с ротора поступает к контакту, от которого подается к свече того цилиндра, где должно произойти воспламенение рабочей смеси. Батарейное зажигание отличается простотой устройства, меньшей стоимостью и обеспечивает хороший пуск двигателя; применяется главным образом на автомобилях.
Зажигание принудительное – воспламенение горючей смеси, искусственно вызываемое путем воздействия на нее внешнего источника тепла (электрического разряда, раскаленного тела, внесенного извне пламени и т.п.).
Принудительное воспламенение горючей смеси возможно лишь в определенных пределах по концентрации. Горючая смесь может подаваться в зону горения в готовом виде. В этом случае скорость распространения фронта пламени определяется только кинетикой химических реакций. Такое горение называется кинетическим, а пламя - нормальным.
33. Индукционный период воспламенения. Границы зажигания.
С температурой самовоспламенения TSвсегда связана величина ti - индукционный период или задержка воспламенения, поскольку переход отTS к TB всегда связан с некоторым временем развития реакций и накопления тепла.
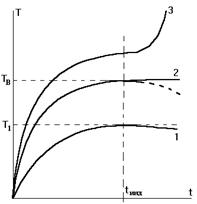
Три вида кривых изменения Т смеси от времени и определение времени индукции как времени, соответствующего точке перегиба. Нижняя кривая соответствует случаю стационарного разогрева до Т1. Пунктирная линия отражает более реальный случай, когда учитывается расход горючего. Верхняя кривая соответствует самовоспламенению.
Индукционный период наглядно показан на рис. 6.
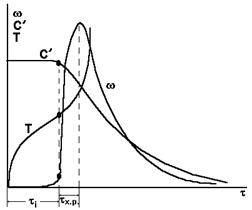
Рис.6.
Кривые зависимости с’=f(t), Т=f(t), =f(t) имеют характерный перегиб (рис.6.).
Характерные признаки самовоспламенения:
ti>>tх.р.
( tx.p. - время химической реакции; это время, соответствующее увеличению скорости химической реакции ве раз, или время от начала заметного хода химической реакции до момента, когда скорость химической реакции достигает максимального значения.)
время ti составляет порядка 85% от общего времени процесса воспламенения, при этом (ti) = 0,05 мах.
ti ~ Е.
При измерении температуры TB обязательно дается ti.
TS наиболее близка к TB при ti стремящейся к бесконечности .
Практически
ti ~ 10 с.
Концентрационные
границы зажигания газа – предельные концентрации горючего газа в смеси с воздухом,
при к-рых смесь воспламеняется и горит. Газовоздушная смесь способна гореть
только при определ. соотношении горючего газа и воздуха. Наименьшая
концентрация горючего газа в смеси, при к-рой газ зажигается (бедная смесь),
наз. нижним пределом воспламенения, а наибольшая, при к-рой газ может гореть
(богатая смесь), — верхним. Подогрев газовоздушной смеси раздвигает границы
зажигания. Наличие их в осн. объясняется снижением темп-ры горения для бедных и
богатых смесей. При потерях теплоты в окружающую среду темп-ра пламени так
сильно падает, что смесь не способна гореть. Для бедных смесей она падает
потому, что необходимо нагревать большое кол-во лишнего воздуха, не участвующего
в процессе горения. У богатых смесей лишнего воздуха нет, наоборот, значит,
часть газа не обеспечена им для горения и не может гореть. На нагрев этого газа
расходуется значит. кол-во теплоты, из-за чего темп-ра падает. Границы
зажигания для метана и природного газа — 5 и 15%, для пропана — 2,4 и 9,5%. Для
обнаружения утечек газа с запасом по отношению к нижнему пределу воспламенения
запах газа должен резко ощущаться при его концентрации в 1 % — для природного
газа и 0,5% — для сжиж.