Материал: Ответы экзамен горения и взрыва
Для протекания процесса горения необходимо горючее вещество, кислород (воздух) и источник воспламенения. Горючее вещество и кислород составляют горючую систему. Источник воспламенения вызывает в ней реакцию окисления. При установившемся горении источником воспламенения служит теплота зоны реакции.
Горючие системы могут быть однородными (однофазными, гомогенными) и неоднородными (многофазными, гетерогенными, гетерофазными). К гомогенным относятся газообразные системы, в которых горючее вещество и окислитель перемешаны друг с другом, например, смеси горючих газов с воздухом. К неоднородным относятся системы, в которых горючее вещество и окислитель находятся в разных фазах, отделены друг от друга поверхностью раздела, например твердые горючие материалы и жидкости, находящиеся в соприкосновении с воздухом, струи горючих газов, поступающие в воздух.
При горении гетерогенных горючих систем кислород, для того чтобы вступить в реакцию с горючим веществом, должен продиффундировать через область пространства, занятую смесью воздуха и продуктов горения.
При высоких температурах наблюдается диффузионное горение, при низких — кинетическое
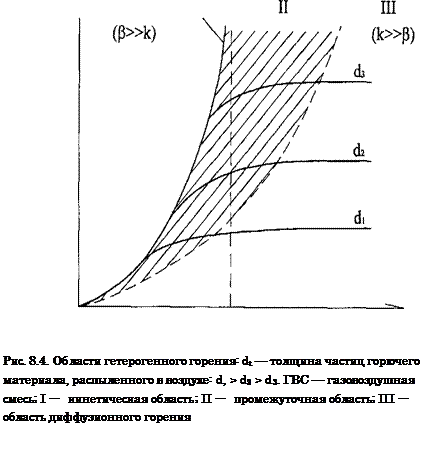 Горение
всех видов газов, жидкостей и твердых веществ на пожарах (за исключением
некоторых взрывчатых веществ и пиротехнических изделий) является диффузионным. Так как наблюдаемая скорость химической реакции в диффузионной
области определяется скоростью диффузии кислорода в зону реакции, то все
реакции горения в этой области имеют одинаковую скорость, не зависящую от
природы горючего. Температурная зависимость скорости реакции в этой области
сравнительно невелика и определяется изменением физических констант (коэффициента
диффузии, вязкости и т.д.) от температуры.
Горение
всех видов газов, жидкостей и твердых веществ на пожарах (за исключением
некоторых взрывчатых веществ и пиротехнических изделий) является диффузионным. Так как наблюдаемая скорость химической реакции в диффузионной
области определяется скоростью диффузии кислорода в зону реакции, то все
реакции горения в этой области имеют одинаковую скорость, не зависящую от
природы горючего. Температурная зависимость скорости реакции в этой области
сравнительно невелика и определяется изменением физических констант (коэффициента
диффузии, вязкости и т.д.) от температуры.
При горении гомогенных горючих систем, в которых окислитель и горючее вещество находятся в одной фазе, диффузионные явления обычно роли не играют.
Горение,
зависящее только от скорости химической реакции, называется кинетическим.
Скорость кинетического горения смесей значительно превышает скорость
диффузионного горения горючих веществ, находящихся в них. Горение таких смесей
в замкнутом объеме представляет взрыв. На практике кинетическое горение наблюдается
только в начальной фазе пожара. Так, пожар ЛВЖ в резервуарах часто возникает в
результате взрыва образовавшейся в них смеси паров жидкости с воздухом. При
взрыве смеси крыша резервуара сбрасывается и горение паров жидкости происходит
в диффузионной области.
14. Теплота сгорания горючих веществ
Горючее, имеющее в своем составе водород, при сгорании образует воду в газообразном состоянии, которая, охлаждаясь, будет конденсироваться. Так как в процессе конденсации паров тепло выделяется, то общее количество теплоты, полученное при сгорании вещества, будет больше на эту величину, при этом количество теплоты, выделяющееся при конденсации паров, равно количеству теплоты, затраченному на парообразование. Тогда Qв = Qн+r, где – Qв высшая теплота сгорания вещества, r – удельная теплота парообразования воды, а Qн – низшая теплота сгорания это количество теплоты, выделяющееся при полном сгорании единицы количества горючего вещества (моль, кг или м3).
Qн может быть рассчитана по закону Гесса, который говорит о том, что тепловой эффект химической реакции равен разности сумм теплоты образования продуктов реакции и теплоты образования исходных веществ, при этом надо учитывать, что теплота образования простого вещества (вещества, молекулы которого состоят из атомов одного элемента, например, N2, O2, H2, S, C...) принимается равной нулю. Удельная теплота сгорания (формулы Д. И. Менделеева).
Высшая:
![]()
Низшая:
![]()
где C,H,W,S – суммарное содержание веществ в % по массе, 25,1*(9Н+W )– теплота затраченная на испарение влаги W вещества и воды, образующейся при сгорании водорода Н горючего вещества (кДж/кг)
15. Стехиометрия горения. Удельный расход окислителя
на горение техногенного вещества.
Уравнение реакции горения вещества в воздухе составляется с учетом того, что в нем на 1 моль кислорода приходится 3,76 молей азота. Например, реакции горения водорода, метана, этана, пропана, ацитилена и спирта, и запишутся в виде следующих уравнений:
2Н2 +02 +3,76N2 = 2H2 0 + 3,76N2.
СН4 + 202 + 2 * 3,76N2 = С02 + 2Н20 + 2 • 3,76N2;
С2Н6 + 3,502 + 3,5* 3,76N2 = 2С02 + 3Н20 + 3,5 • 3,76N2;
С3Н8 + 502 + 5* 3,76N2 = 3С02 + 4Н20 + 5 • 3,76N2;
С2Н2 + 2,502 + 2,5* 3,76N2 = 2С02 + Н20 + 2,5 • 3,76N2;
С2Н50Н + 302 + 3 • 3/76N 2 = 2С02 + ЗН20 + 3 • 3,76N2;
Азот в уравнениях химических реакций горения учитывается потому, что он поглощает часть теплоты, выделяемой в результате реакций горения, и входит в состав продуктов сгорания — дымовых газов. При написании уравнения горения и составлении материального баланса, как правило, записывают только продукты полного окисления СО2 и Н2О. Если в составе горючего вещества есть сера (S), то при сгорании образуется SО2– также записывают. Азот (N), входящий в состав горючего вещества, при горении в воздухе не окисляется, а выделяется в виде свободного азота (N2). Объясняется это тем, что при горении в воздухе температура горения относительно невысокая (1500-2000 К) и при такой температуре окислы азота не образуются. По уравнениям химических реакций горения рассчитывается количество воздуха, необходимого для полного сгорания единицы массы или единицы объема горючего вещества, а также состав и количество продуктов сгорания.
Минимальное количество воздуха, необходимое для полного сгорания единицы массы (кг) или объёма (м3) горючего вещества, называется теоретически необходимым и обозначается Vв0.
Для горения индивидуального вещества(газа) потребуется удельный объём воздуха, рассчитываемый по формуле: Vв0 = 4,76*О/ Z (м3воздуха/м3газов), где О – количество молей кислорода, Z – количество молей горючего, 4,76 – количество молей воздуха, приходящихся на один моль кислорода.
Например: Определить удельный объём воздуха Vв0 для горения водорода, метана, этана, пропана и ацитилена. Решение: Из уравнений реакций горения ( см. уравнения выше, без записи азота):
для водорода: 2Н2 +02 = 2H2 0 4,76*1/2=2,38 м3воздуха/м3водорода
для метана: СН4 + 202 = С02 + 2Н20 4,76*2/1=9,52 м3воздуха/м3метана
для этана: С2Н6 + 3,502 = 2С02 + 3Н20 4,76*3,5/1=16,66 м3воздуха/м3этана
для пропана: С3Н8 + 502 = 3С02 + 4Н20 4,76*5/1= 23,8 м3воздуха/м3пропана
для ацителена: С2Н2 + 2,502 = 2С02 + Н20 4,76*2,5/1= 11,9 м3воздуха/м3ацитилена
Для горения смеси химических соединений (древесина, торф ,нефть, смесь газов и др.)
– для сгорания 1 кг жидких и твердых веществ потребуется:
Vв0 = 0,269*(С/3+Н+S/8 – О/8) м3воздуха/кг горючего, где С, Н, S, О – процентное содержание соответствующего элемента по массе.
Например: Определить объём воздуха, теоретически необходимого для горения для 5 кг торфа состава: С – 40%, Н – 4%, О – 13%, N – 20%, А (зола) – 10%, W – 13%. Решение: Так как азот, зола и влага топлива не принимают участие в горении, то на 1кг торфа потребуется
– для сгорания 1 м3 смеси газов потребуется: Vв0 =( ∑Ki*Гi )/21( м3воздуха/м3смеси газов),
где Ki – количество молей кислорода, расходуемых на 1 моль i-го газа, Гi – процентное содержание i-го газа в смеси газов (%).
Например: Определить объём воздуха, теоретически необходимого для горения 1м3 природного газа состава: СН4 – 86,5%, С2Н6 – 3%, С3Н8 – 1%, СО2 – 7,3%, N2 – 2,2%.
Решение. Из уравнений реакций горения соответствующих газов определяем коэффициенты Ki для метана, этана и пропана (СО2 и N2 не принимают участие в горении).
для метана: СН4 + 202 = С02 + 2Н20, откуда Кметана = 2;
для этана: С2Н6 + 3,502 = 2С02 + 3Н20 откуда Кэтена = 3,5;
для пропана: С3Н8 + 502 = 3С02 + 4Н20 откуда Кпропана = 5;
Для сгорания 1 м3 природного газа указанного состава потребуется:
Vв0 = (2*86,5+3,5*3+5*1) /21= 8,98 ( м3воздуха/м3 природного газа)
16. Состав атмосферного воздуха при расчётах параметров горения.
При большинстве пожаров в основе горения лежат реакции соединения горючих веществ с кислородом воздуха и только в отдельных случаях, когда горят взрывчатые вещества, пиротехнические изделия и другие материалы с положительным кислородным балансом, горение происходит за счет кислорода, содержащегося в молекуле горючего вещества или кислорода окислителя.
Поскольку воздух состоит из 21 % (об.) кислорода и 79 % (об.) азота, т.е. в нем на 1 моль кислорода приходится 79/21 = 3,76 молей азота, то уравнение реакции горения вещества в воздухе составляют с учетом того, что на каждый моль кислорода приходится по 3,76 моля азота.
Например, реакции горения водорода, метана, этана, пропана, ацитилена и спирта, и запишутся в виде следующих уравнений:
2Н2 +02 +3,76N2 = 2H2 0 + 3,76N2.
СН4 + 202 + 2 * 3,76N2 = С02 + 2Н20 + 2 • 3,76N2;
С2Н6 + 3,502 + 3,5* 3,76N2 = 2С02 + 3Н20 + 3,5 • 3,76N2;
С3Н8 + 502 + 5* 3,76N2 = 3С02 + 4Н20 + 5 • 3,76N2;
С2Н6 + 3,502 + 3,5* 3,76N2 = 2С02 + 3Н20 + 3,5 • 3,76N2;
С2Н50Н + 302 + 3 • 3/76N 2 = 2С02 + ЗН20 + 3 • 3,76N2;
Азот в уравнениях химических реакций горения учитывается потому, что он поглощает часть теплоты, выделяемой в результате реакций горения, и входит в состав продуктов сгорания — дымовых газов. При написании уравнения горения и составлении материального баланса, как правило, записывают только продукты полного окисления СО2 и Н2О. Если в составе горючего вещества есть сера (S), то при сгорании образуется SО2 – его также записывают. Азот (N), входящий в состав горючего вещества, при горении в воздухе не окисляется, а выделяется в виде свободного азота (N2). Объясняется это тем, что при горении в воздухе температура горения относительно невысокая (1500-2000 К) и при такой температуре окислы азота не образуются. По уравнениям химических реакций горения рассчитывается количество воздуха, необходимого для полного сгорания единицы массы или единицы объема горючего вещества, а также состав и количество продуктов сгорания.
17. Удельный теоретический расход воздуха на горение техногенного вещества.
Уравнение реакции горения вещества в воздухе составляется с учетом того, что в нем на 1 моль кислорода приходится 3,76 молей азота. Например, реакции горения водорода, метана, этана, пропана, ацитилена и спирта, и запишутся в виде следующих уравнений:
2Н2 +02 +3,76N2 = 2H2 0 + 3,76N2.
СН4 + 202 + 2 * 3,76N2 = С02 + 2Н20 + 2 • 3,76N2;
С2Н6 + 3,502 + 3,5* 3,76N2 = 2С02 + 3Н20 + 3,5 • 3,76N2;
С3Н8 + 502 + 5* 3,76N2 = 3С02 + 4Н20 + 5 • 3,76N2;
С2Н2 + 2,502 + 2,5* 3,76N2 = 2С02 + Н20 + 2,5 • 3,76N2;
С2Н50Н + 302 + 3 • 3/76N 2 = 2С02 + ЗН20 + 3 • 3,76N2;
Азот в уравнениях химических реакций горения учитывается потому, что он поглощает часть теплоты, выделяемой в результате реакций горения, и входит в состав продуктов сгорания — дымовых газов. При написании уравнения горения и составлении материального баланса, как правило, записывают только продукты полного окисления СО2 и Н2О. Если в составе горючего вещества есть сера (S), то при сгорании образуется SО2– также записывают. Азот (N), входящий в состав горючего вещества, при горении в воздухе не окисляется, а выделяется в виде свободного азота (N2). Объясняется это тем, что при горении в воздухе температура горения относительно невысокая (1500-2000 К) и при такой температуре окислы азота не образуются. По уравнениям химических реакций горения рассчитывается количество воздуха, необходимого для полного сгорания единицы массы или единицы объема горючего вещества, а также состав и количество продуктов сгорания.
Минимальное количество воздуха, необходимое для полного сгорания единицы массы (кг) или объёма (м3) горючего вещества, называется теоретически необходимым и обозначается Vв0.
Для горения индивидуального вещества(газа) потребуется удельный объём воздуха, рассчитываемый по формуле: Vв0 = 4,76*О/ Z (м3воздуха/м3газов), где О – количество молей кислорода, Z – количество молей горючего, 4,76 – количество молей воздуха, приходящихся на один моль кислорода. Например: Определить удельный объём воздуха Vв0 для горения водорода, метана, этана, пропана и ацитилена. Решение: Из уравнений реакций горения ( см. уравнения выше, без записи азота):
для водорода: 2Н2 +02 = 2H2 0 4,76*1/2=2,38 м3воздуха/м3водорода
для метана: СН4 + 202 = С02 + 2Н20 4,76*2/1=9,52 м3воздуха/м3метана
для этана: С2Н6 + 3,502 = 2С02 + 3Н20 4,76*3,5/1=16,66 м3воздуха/м3этана
для пропана: С3Н8 + 502 = 3С02 + 4Н20 4,76*5/1= 23,8 м3воздуха/м3пропана
для ацителена: С2Н2 + 2,502 = 2С02 + Н20 4,76*2,5/1= 11,9 м3воздуха/м3ацитилена
Для горения смеси химических соединений (древесина, торф ,нефть, смесь газов и др.)
– для сгорания 1 кг жидких и твердых веществ потребуется:
Vв0 = 0,269*(С/3+Н+S/8 – О/8) м3воздуха/кг горючего, где С, Н, S, О – процентное содержание соответствующего элемента по массе.