Материал: Ответы экзамен горения и взрыва
Например: Определить объём воздуха, теоретически необходимого для горения для 5 кг торфа состава: С – 40%, Н – 4%, О – 13%, N – 20%, А (зола) – 10%, W – 13%. Решение: Так как азот, зола и влага топлива не принимают участие в горении, то на 1кг торфа потребуется
Vв0 = 0,269*(40/3+4 – 13/8) = 4,23 м3/кг, а на 5кг – 4,23*5 = 21,15 м3воздуха.
– для сгорания 1 м3 смеси газов потребуется: Vв0 =( ∑Ki*Гi )/21( м3воздуха/м3смеси газов),
где Ki – количество молей кислорода, расходуемых на 1 моль i-го газа, Гi – процентное содержание i-го газа в смеси газов (%).
Например: Определить объём воздуха, теоретически необходимого для горения 1м3 природного газа состава: СН4 – 86,5%, С2Н6 – 3%, С3Н8 – 1%, СО2 – 7,3%, N2 – 2,2%.
Решение:. Из уравнений реакций горения соответствующих газов определяем коэффициенты Ki для метана, этана и пропана (СО2 и N2 не принимают участие в горении).
для метана: СН4 + 202 = С02 + 2Н20, откуда Кметана = 2;
для этана: С2Н6 + 3,502 = 2С02 + 3Н20 откуда Кэтена = 3,5;
для пропана: С3Н8 + 502 = 3С02 + 4Н20 откуда Кпропана = 5;
Для сгорания 1 м3 природного газа указанного состава потребуется:
Vв0 = (2*86,5+3,5*3+5*1) /21= 8,98 (
м3воздуха/м3 природного газа)
18. Коэффициент избытка воздуха.
 Практически при горении на пожарах расход
воздуха значительно больше. Разность между количеством воздуха, идущим на
горение, и теоретически необходимым, называется избытком воздуха. Отношение
количества воздуха, практически расходующегося при горении (Vв) к теоретически необходимому количеству
(Vв0), называется коэффициентом
избытка воздуха aв : aв
= Vв / Vв0
Практически при горении на пожарах расход
воздуха значительно больше. Разность между количеством воздуха, идущим на
горение, и теоретически необходимым, называется избытком воздуха. Отношение
количества воздуха, практически расходующегося при горении (Vв) к теоретически необходимому количеству
(Vв0), называется коэффициентом
избытка воздуха aв : aв
= Vв / Vв0
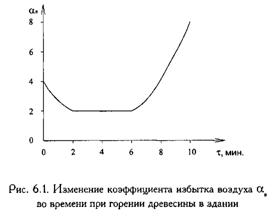
При пожарах внутри помещений коэффициент избытка воздуха непостоянен и
изменяется во времени даже при постоянной площади приточных проёмов. На
величину aв влияют вид и состояние
горючего вещества, величина площади пожара и условия диффузии воздуха к зоне
горения. С увеличением площади пожара коэффициент aв уменьшается и достигает минимума при максимальной
площади пожара ( вследствии увеличения Vв0 ). По мере выгорания вещества
на этой площади коэффициент aв снова увеличивается. (см. рис.
6.1.)
19. Определение количества и состава продуктов сгорания вещества
Состав и количество продуктов сгорания определяются по уравнениям химических реакций горения и рассчитывается количество воздуха, необходимого для полного сгорания единицы массы или единицы объема горючего вещества.
При большинстве пожаров в основе горения лежат реакции соединения горючих веществ с кислородом воздуха и только в отдельных случаях, когда горят взрывчатые вещества, пиротехнические изделия и другие материалы с положительным кислородным балансом, горение происходит за счет кислорода, содержащегося в молекуле горючего вещества или кислорода окислителя.
Поскольку воздух состоит из 21 % (об.) кислорода и 79 % (об.) азота, т.е. в нем на 1 моль кислорода приходится 79/21 = 3,76 молей азота, то уравнение реакции горения вещества в воздухе составляют с учетом того, что на каждый моль кислорода приходится по 3,76 моля азота.
Например, реакции горения водорода, метана, этана, пропана, ацитилена и спирта, и запишутся в виде следующих уравнений:
2Н2 +02 +3,76N2 = 2H2 0 + 3,76N2.
СН4 + 202 + 2 * 3,76N2 = С02 + 2Н20 + 2 • 3,76N2;
С2Н6 + 3,502 + 3,5* 3,76N2 = 2С02 + 3Н20 + 3,5 • 3,76N2;
С3Н8 + 502 + 5* 3,76N2 = 3С02 + 4Н20 + 5 • 3,76N2;
С2Н6 + 3,502 + 3,5* 3,76N2 = 2С02 + 3Н20 + 3,5 • 3,76N2;
С2Н50Н + 302 + 3 • 3/76N 2 = 2С02 + ЗН20 + 3 • 3,76N2;
Азот в уравнениях химических реакций горения учитывается потому, что он поглощает часть теплоты, выделяемой в результате реакций горения, и входит в состав продуктов сгорания — дымовых газов. При написании уравнения горения и составлении материального баланса, как правило, записывают только продукты полного окисления СО2 и Н2О. Если в составе горючего вещества есть сера (S), то при сгорании образуется SО2 – его также записывают. Азот (N), входящий в состав горючего вещества, при горении в воздухе не окисляется, а выделяется в виде свободного азота (N2). Объясняется это тем, что при горении в воздухе температура горения относительно невысокая (1500-2000 К) и при такой температуре окислы азота не образуются.
Теоретический объём продуктов сгорания (aв=1) твердых и жидких горючих веществ определяется по формуле: Vпс0=( С02+ Н20+ N2+ SО2)*22,4/М (м3/кг), где С02, Н20, N2, SО2 – число киломолей соответствующего вещества в уравнении реакции горения одного киломоля горючего вещества. М– молекулярная масса горючего вещества, кг/кмоль.
Например Определить объем и состав (в объемных процентах) продуктов сгорания 1 кг этилацетата (СН3СООС2Н.) при 273 К и давлении 101,3 кПа. ( т.е. при нормальных условиях).
Решение. Составляем уравнение горения этилацетата в воздухе:
CH3COOC2H5+502+5*3,76N2=4C02+4H20+18,8N2.
Определяем состав продуктов сгорания в объемных процентах:
C02=4*100/26,8=15,92%; H20=4*100/26,8=15,92%; N2=100 – 2*15,92=68,16% .
Если горение протекает при избытке воздуха ∆Vв, то находим его по формуле: ∆Vв=(aв -1)* Vв0
Полное количество азота в продуктах сгорания составит:
VN2= VN20+0,79(aв -l)* Vв0, а количество избыточного кислорода: ∆VO2=0,21.( aв -l)* Vв0
Полное
количество продуктов сгорания: Vпс = Vпс0 + ∆Vв
20. Энтальпия и энтропия
Энтальпия, или общее теплосодержание насыщенного пара, это количество теплоты, необходимое для повышения температуры 1кг вещества от абсолютного нуля до пара заданной температуры.
Энтальпия в общем случае является функцией температуры и давления. Увеличение энтальпии с приращением температуры: Δi = Срср (Т2 – Т1) = Срср (t2 – t1), Дж/кг, т.е. изменение энтальпии идеального газа равно произведению средней теплоёмкости при постоянном давлении на разность температур газа.
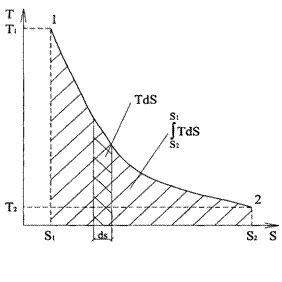
Энтропия – функция состояния рабочего тела, выражается соотношением:
ds = dq / T = (du + dl) / T, Дж/(кг∙К), где: ds – приращение энтропии, Дж/(кг∙К).
 dq–изменение тепловой энергии
рабочего тела, Дж/кг. du–приращение внутренней энергии, Дж/кг.
dl – внешняя работа, Дж/кг.
Т – абсолютная температура, К
dq–изменение тепловой энергии
рабочего тела, Дж/кг. du–приращение внутренней энергии, Дж/кг.
dl – внешняя работа, Дж/кг.
Т – абсолютная температура, К
Таким образом, энтропия – это параметр, который изменяется только от количества переданной или отведённой теплоты. При ds > 0 теплота к системе подводится, при ds < 0 – отводится. В термодинамике широко используются не только координаты p – v, но и s – T, а также термодинамическое состояние вещества представляют диаграммой i – s.
![]() Энтропия не может быть измерена
каким-либо образом, как например, объем и определяется только расчетным путем.
Количество теплоты: q = Т • ds или dq=Tds .
Энтропия не может быть измерена
каким-либо образом, как например, объем и определяется только расчетным путем.
Количество теплоты: q = Т • ds или dq=Tds .
Функциональные
зависимости T=T(s) и р = р (v) определяют термодинамические
процессы, поэтому в термодинамике широко используются не только координаты « р
-v», но и «s-Т» — координаты, характеризующие теплообмен с
внешней средой
21. Энтальпия окислителя и воздуха, участвующего в горении
Энтальпия — это полная энергия рабочего тела в потоке, зависящая от термодинамического состояния тела и представляющая собой сумму внутренней энергии u и потенциальной энергии pv,
т.е.: i=u+pv. В случае пожара это энергия горючих веществ, окислителя и воздуха, поступающих в зону горения или уходящих из неё.
Тепловой баланс внутреннего пожара на любой стадии развития, отнесённый к единице площади пожара: Qнр * Wм + QФ = Q1 + Q2+Q3+Q4 + Q5+Q6, кДж/(м2*с),
где Qнр — низшая удельная теплота сгорания вещества, кДж/кг;
Qф — энтальпия горючих веществ и воздуха, поступающих на горение в единицу времени на 1 м2 площади пожара, кДж/(м2*с);
Wм — массовая скорость выгорания горючего вещества с 1 м2 горящей поверхности, кг/(м2*с);
Q1 — энтальпия продуктов сгорания, уходящих из зоны горения с единицы площади пожара в единицу времени, кДж/(м2*с);
Q2 — энтальпия избытка воздуха, поступающего на горение, кДж/(м2*с);
Q3— количество теплоты, излучаемой пламенем, кДж/(м2*с);
Q4 — количество теплоты, затрачиваемой на нагрев реагирующих веществ, кДж/(м2*с);
Q5 — количество теплоты, затрачиваемой на нагрев строительных конструкций, кДж/(м2*с);
Q6 — потери теплоты вследствие неполноты химического сгорания, кДж/(м2*с).
Количество теплоты, излучаемой пламенем факела в единицу времени с единицы поверхности, может быть определено по формуле Стефана-Больцмана: Q3=ε0*σ*Т4 пл , кДж/(м2-с),
где ε0 — степень черноты пламени;
σ — постоянная Стефана-Больцмана, σ = 5,67*10-11 кВт/(м2*К4); Тпл — температура пламени, К.
При горении нефтепродуктов степень черноты пламени близка к единице.

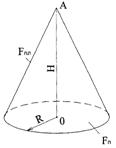 Если форму пламени принять конической, то отношение
поверхности пламени Fпл к площади пожара Fп для случая горения нефтепродуктов
в резервуарах примерно составит:
Если форму пламени принять конической, то отношение
поверхности пламени Fпл к площади пожара Fп для случая горения нефтепродуктов
в резервуарах примерно составит:
![]()
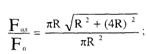
![]()
Таким образом, на внутренних пожарах доля теплоты, теряемой излучением, меньше половины теплоты, выделяющейся в результате горения.
Тепловой
баланс открытого пожара отличается от внутреннего тем, что в правой части
уравнения отсутствует величина Q5. На открытом пожаре наибольшее
значение имеет теплота, уносимая с продуктами сгорания и излучаемая зоной
горения. Последнее обстоятельство способствует распространению пожара и затрудняет
действия пожарных.
22. Уравнение теплового баланса процесса горения
при адиабатических условиях.
Выделившееся в результате сгорания тепло нагревает продукты горения (CO2, H2O, N2...) от начальной температуры T0 до температуры Tг, увеличивая их теплосодержание и уравнение теплового баланса будет: Qн*(1 – h) = ∑ { Hпгi(Tг) – Hпгi(T0)}* Vпгi где: Qн – низшая теплота сгорания вещества; h – коэффициент теплопотерь (доля потерь тепла на излучение); Hпгi(Tг) и Hпгi(T0) – значения теплосодержания (энтальпии) i-го продукта горения при температуре горения и начальной температуре; Vпгi – объем i-го продукта горения. Если теплосодержание продуктов горения при Т = 273 К принять равным нулю, то уравнение теплового баланса будет: Qн*(1 – h) = ∑Hпгi(Tг) * Vпгi
При горении в адиабатических условиях, т. е. горении с теоретическим количеством воздуха (aв=1) без потерь теплоты (h = 0) и без теплообмена с окружающей средой уравнение теплового баланса будет: Qн =∑ Hпгi(Tг) * Vпгi ,
или в случае общего теплового баланса внутреннего пожара (см. 21) Qнр * Wм = Q1
где Qнр — низшая удельная теплота сгорания вещества, кДж/кг;
Wм — массовая скорость выгорания горючего вещества с 1 м2 горящей поверхности, кг/(м2*с);
Q1 — энтальпия продуктов сгорания, уходящих из зоны горения с единицы площади пожара в единицу времени, кДж/(м2*с);
23. Калориметрическая (адиабатическая) температура горения.
Реальная температура горения.
Выделяющаяся в зоне горения теплота воспринимается продуктами сгорания, вследствие чего они нагреваются до высокой температуры. Различают калориметрическую, теоретическую и действительную температуры горения.
Действительной температурой горения называется температура реально устанавливающаяся в условиях пожара.
Под калориметрической температурой понимается температура, которую приобретают продукты полного сгорания, когда вся теплота расходуется на их нагревание.
При вычислении теоретической температуры пренебрегают потерями теплоты в окружающую среду, но учитывают расход теплоты на диссоциацию продуктов реакции (что происходит при температурах выше 1973 К).
Калориметрическую температуру горения вычисляют для следующих постоянных условий:
–воздух и горючее вещество находятся при нормальных условиях (273 К);
–коэффициент избытка воздуха равен единице;