Материал: Оптимизация методик определения концентрации железа (III) в полиэлектролитных микрокапсулах и магнитоуправляемых липосомах
Из данных таблицы видим, что концентрация железа
(III) в исследуемых
образцах различна и составляет 643мг/л; 953мг/л; 1134мг/л в капсулах и
1651мг/л; 1191мг/л; 305мг/л в липосомах. Относительная погрешность определения
концентраций железа в капсулах и липосомах метода комплексонометрического
титрования составила 4-7% и соответственно 1-21% для липосом.
3.3 Результаты
определения концентрации железа (III) в полиэлектролитных микрокапсулах и
магнитоуправляемых липосомах методом фотоколориметрии
Также как и в случае комплексонометрического титрования на первом этапе была произведена оценка специфичности метода. С целью проверки были исследованы холостые образцы полиэлектролитных микрокапсул и липосом, не содержащих магнетит (холостая проба) и образцы с содержанием наночастиц магнетита (опытный). На рисунке 3.3.1. приведены спектры поглощения растворенных холостых образцов и образцов с содержанием наночастиц магнетита.
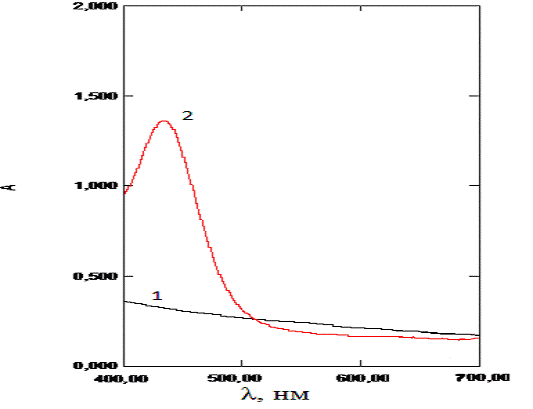
Рис.3.3.1. Спектры поглощения растворенных
пустых капсул (1) линия и растворенных микрокапсул с магнетитом (2)
Отметим, что растворенные липосомы дают такой же спектр поглощения как и микрокапсулы, при условии что концентрация магнетита в липосомах равняется концентрации магнетита в капсулах.
На спектрах поглощения растворенных магнетит содержащих образцов имеется пик поглощения с максимумом в области 430 нм, на спектрограммах холостых образцов этот пик отсутствует, поэтому в качестве длинны волны, для определения железа, была выбрана длина волны (λ)=430нм.
В качестве нижнего предела измерений принималась концентрация железа (III) в растворе, при определении оптической плотности которого отношение шум/сигнал равнялось 5. Для оценки НПКО исследовали стандартные растворы квасцов с известными концентрациями железа 0,01мг/л; 0,1мг/л; 1,0мг/л. Результаты измерений представлены в таблице 4.
Таблица 4 Нижний предел количественного определения метода фотоколориметрии
|
Взятая концентрация, мг/л |
№ Определения |
Отношение шум/сигнал |
|
0,01 |
1 |
3,4 |
|
|
2 |
3,8 |
|
|
3 |
2,6 |
|
0,1 |
1 |
5,7 |
|
|
2 |
6,3 |
|
|
3 |
|
|
1,0 |
1 |
12,4 |
|
|
2 |
15,8 |
|
|
3 |
17,2 |
Как видно из таблицы 4 наименьшее концентрация, при которой отношение шум/сигнал было больше 5, равна 0,1мг/л. Эта концентрация принималась за нижний предел количественного определения железа (III). Таким образом чувствительность спектрофотометрического метода была практически в 1000 раз выше чем у метода комплексонометрического титрования.
Проверка гипотезы о линейной зависимости
оптической плотностью (А) и концентрации железа в образце. Было проведено
определение железа (III)
в растворах с его известной концентрацией. Зависимость оптической плотности (А)
от концентрации железа (III)
в исследуемых образцах на длине волны 430нм показана на рисунке 9.
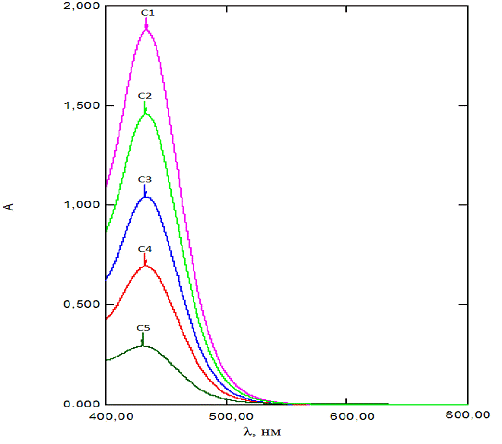
Рис. 3.3.2 Спектры поглощения растворенного
магнетита с различными концентрация ми (С)
Из рисунка 3.3.2. видно, что оптическая плотность увеличивается при увеличении концентрации.
Построение калибровочной кривой для фотоколориметрии было описано в параграфе 2.2. В данном разделе приведены значения оптической плотности калибровочных растворов и метрологические характеристики для каждой точки. Следует заметить, что определения оптической плотности для каждого образца производилось не менее трех раз. Далее рассматривалась средняя оптическая плотность, погрешность эксперимента определялась как стандартное отклонение. Относительную погрешность определялась как отношение стандартного отклонения к среднему значению. Результаты измерений представлены в таблице 5.
Таблица 5 Калибровка для фотоколориметрического метода
|
Взятая концентрация, мг/л |
№ Определения |
Значение A |
Средняя А |
Погрешность |
Относительная погрешность, % |
|
0,1 |
1 |
0,0095 |
0,009 |
0,0004 |
4,87 |
|
|
2 |
0,0110 |
|
|
|
|
|
3 |
0,0075 |
|
|
|
|
0,2 |
1 |
0,0165 |
0,017 |
0,0008 |
4,69 |
|
|
2 |
0,0171 |
|
|
|
|
|
3 |
0,0181 |
|
|
|
|
0,5 |
1 |
0,0471 |
0,045 |
0,0025 |
5,56 |
|
|
2 |
0,0455 |
|
|
|
|
|
3 |
0,0422 |
|
|
|
|
1,0 |
1 |
0,0976 |
0,095 |
0,0780 |
8,24 |
|
|
2 |
0,1012 |
|
|
|
|
|
3 |
0,0862 |
|
|
|
|
1,5 |
1 |
0,1511 |
0,148 |
0,0030 |
2,02 |
|
|
2 |
0,1452 |
|
|
|
|
|
3 |
0,1491 |
|
|
|
|
2,0 |
1 |
0,2038 |
0,196 |
0,0085 |
4,34 |
|
|
2 |
0,1971 |
|
|
|
|
|
3 |
0,1869 |
|
|
|
|
2,5 |
1 |
0,2471 |
0,238 |
0,0081 |
3,40 |
|
|
2 |
0,2363 |
|
|
|
|
|
3 |
0,2312 |
|
|
|
|
3,0 |
1 |
0,3212 |
0,298 |
0,0229 |
7,67 |
|
|
2 |
0,2754 |
|
|
|
|
|
3 |
0,2985 |
|
|
|
|
3,5 |
1 |
0,3511 |
0,343 |
0,0070 |
2,06 |
|
|
2 |
0,3371 |
|
|
|
|
|
3 |
0,3422 |
|
|
|
По результатам измерений была построена калибровочная кривая (рисунок 3.3.3.), по которой в последующем производилось определение концентрации железа (III) в исследуемых образцах, уравнение калибровочной кривой имело вид y=0,11x-0,002 коэффициент корреляции R2 = 0,999
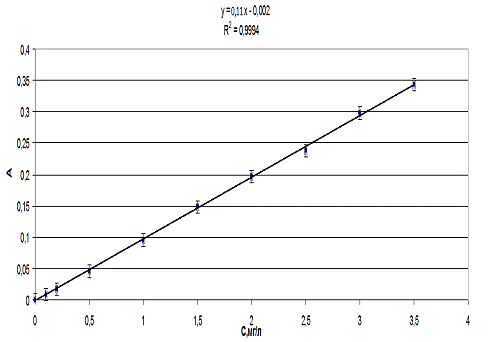
Рис. 3.3.3 Калибровочный график для определения
концентрации железа (III)
фотоколориметрическим методом
На рисунке 3.3.3. представлена корреляционная зависимость оптической плотности от концентрации железа (III) относительная ошибка в области НПКО составляет 5%.
Таким образом метод, фотоколориметрии для определения концентрации железа (III) оказался более чувствительным и имел меньшую погрешность измерения по сравнению с методом комплексонометрического титрования. В связи с этим данному методу было отдано предпочтение при исследовании концентрации железа (III) в образцах полиэлектролитных микрокапсул и магнитоуправляемых липосом.
Выше описанные методы были использованы для определения концентрации железа (III) в образцах полиэлектролитных микрокапсул и магнитоуправляемых липосом, для исследования были предоставлены по три образца полиэлектролитных микрокапсул (в дальнейшем МК1, МК2, МК3) и три образца магнитоуправляемых липосом(в дальнейшем Л1, Л2, Л3) синтезированных в разное время. Пробоподготовка взвеси полиэлектролитных микрокапсул и магнитоуправляемых липосом по методике, описанной ниже [26] следующим образом:
Для выделения железа из полиэлектролитных микрокапсул и магнитоуправляемых липосом использовали концентрированную соляную кислоту. Суспензию полиэлектролитных микрокапсул и магнитоуправляемых липосом 0,1 мл растворяли 0,1 мл 37% HCl. Многослойные микрокапсулы формируются слабыми полиэлектролитами чувствительными к pH среды, они становятся незаряженными, что приводит к разрушению капсулы [27]. В результате этого капсулы подвергаются деструкции, а освободившийся магнетит растворяется кислотой с образованием соответствующих солей железа (II, III). Липосомы под действием концентрированной соляной кислоты раскрываются, содержащийся в них магнетит высвобождается, под действием кислоты превращается в. соли железа (II, III). Образцы растворенные в кислоте необходимо нагреть на водяной бане при температуре 80-900С с добавлением 1мл H2O2 6% для того чтобы все железо перешло в степень окисления (III) довести объем до 50 мл.
Результаты определения концентраций железа (III)
в образцах фотоколориметрическим методом приведены в таблице 6.
Таблица 6 Результаты определения концентрации железа (III) в образцах фотоколориметрическим методом
|
№ |
А |
<A> |
Сx(Fe3+), мг/л |
C(Fе3+),мг/л |
Погрешность |
Относительная погрешность, % |
|
Мк1 |
0,1021 |
0,10 |
1,20 |
600 |
0,01 |
5,81 |
|
|
0,0947 |
|
|
|
|
|
|
|
0,1063 |
|
|
|
|
|
|
МК2 |
0,1461 |
0,14 |
1,62 |
810 |
0,01 |
2,45 |
|
|
0,1393 |
|
|
|
|
|
|
|
0,1442 |
|
|
|
|
|
|
Мк3 |
0,2057 |
0,20 |
2,10 |
1050 |
0,01 |
5,12 |
|
|
0,1976 |
|
|
|
|
|
|
|
0,1857 |
|
|
|
|
|
|
Л1 |
0,3102 |
0,30 |
3,17 |
1585 |
0,01 |
2,24 |
|
|
0,2966 |
|
|
|
|
|
|
|
0,3027 |
|
|
|
|
|
|
Л2 |
0,219 |
0,22 |
2,30 |
1150 |
0,016 |
7,40 |
|
|
0,220 |
|
|
|
|
|
|
|
0,221 |
|
|
|
|
|
|
Л3 |
0,048 |
0,05 |
0,53 |
210 |
0,01 |
5,57 |
|
|
0,049 |
|
|
|
|
|
|
|
0,500 |
|
|
|
|
|
Из данных таблицы видим, что концентрация железа
(III) в исследуемых
образцах различна и составляет 600мг/л; 810мг/л; 1050мг/л в капсулах и
1585мг/л; 1150мг/л; 210мг/мл в липосомах. Относительная погрешность определения
концентраций железа (III)
в капсулах для фотоколориметрического метода 2-5% в липосомах 2-7%
соответственно.
3.4 Результаты
определения концентрации железа (III) в полиэлектролитных микрокапсулах и
магнитоуправляемых липосомах методом ЭПР-спектроскопии
Химические методы определения концентрации железа (III) обладают достаточной точностью и специфичностью в синтетических (искусственных) объектах. При биомедицинском применении полиэлектролитных микрокапсул и липосом возникает задача, по изучению их биокинетики и тканевого распределения. Химические методы в данном случае не пригодны для определения концентрации железа (III), так как они не позволяют идентифицировать железо введенное в организм в капсулах, липосомах и собственное железо присутствующее в организме. Для этой цели необходим метод с помощью которого можно идентифицировать железо (III), входящее в состав магнитных наночастиц и ионизированное железо (III) организма (входящее в состав гемоглобина и миоглобина). В качестве такого метода был выбран метод электронного парамагнитного резонанса (ЭПР).
Специфичность основана на возможности достоверно определять магнетит в образцах и достигается путем использования проб сравнения. В качестве образца сравнения были взяты образцы донорской крови, в которых была определена концентрация железа методом фотоколориметрии.
Проводили анализ образцов крови
(холостая проба) и образцов крови с добавлением магнитоуправляемых липосом и
полиэлектролитных микрокапсул (опытный образец). При ЭПР-спектроскопии холостых
образцов крови сигналов характерных для магнетита обнаружено не было. Данные
представлены на рисунке 3.4.1.
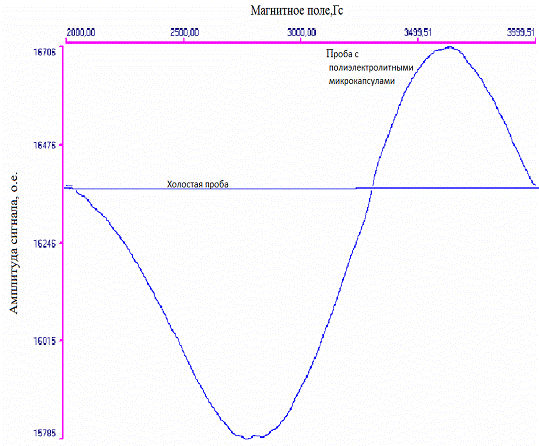
Рис. 3.4.1.ЭПР-спектр поглощения холостой пробы
и пробы с добавлением полиэлектролитных микрокапсул. Спектр поглощения для
холостой пробы не был зарегистрирован
Для нахождения нижнего предела
количественного определения магнетита проводили анализ проб, приготовленных из
растворов коллоидного магнетита с концентрациями в диапазоне от 4,6 до 277,8 мг/л (4,6; 46,3;
185,2; 277,8 мг/л). Каждая проба содержала после высушивания то же количество
магнетита, что и 10 мкл раствора, использовавшегося при ее приготовлении (0,05;
0,46; 1,85; 2,78 мкг). Выбор концентраций обусловлен литературными данными и
результатами предварительных собственных исследований отношения сигнал/шум.
Эксперименты по ЭПР-спектрометрии для каждого из проб проводили не менее 6 раз
и определяли отношение сигнал/шум. Уровень шума определялся по ЭПР-сигналу
контрольного образца, приготовленного из воды Milli-Q. Результаты исследований
приведены в таблице 7.
Таблица 7 Нижний предел количественного определения магнетита методом ЭПР-спектроскопии
|
№ серии |
Масса вещества в образце, мкг |
№ анализа |
Отношение сигнал/шум |
Среднее |
Погрешность |
Относительная погрешность, % |
|
1 |
0,05 |
1 |
2,0 |
1,7 |
0,2 |
14,4 |
|
|
|
2 |
1,6 |
|
|
|
|
|
|
3 |
1,7 |
|
|
|
|
|
|
4 |
1,9 |
|
|
|
|
|
|
5 |
1,3 |
|
|
|
|
|
|
6 |
1,7 |
|
|
|
|
2 |
0,46 |
1 |
4,8 |
4,9 |
0,3 |
8,2 |
|
|
|
2 |
4,7 |
|
|
|
|
|
|
3 |
4,8 |
|
|
|
|
|
|
4 |
5,1 |
|
|
|
|
|
|
5 |
4,6 |
|
|
|
|
|
|
6 |
5,4 |
|
|
|
|
3 |
1,85 |
1 |
7,3 |
6,9 |
0,3 |
4,9 |
|
|
|
2 |
6,3 |
|
|
|
|
|
|
3 |
6,8 |
|
|
|
|
|
|
4 |
7,0 |
|
|
|
|
|
|
5 |
6,9 |
|
|
|
|
|
|
6 |
7,1 |
|
|
|
|
4 |
2,78 |
1 |
9,9 |
9,7 |
0,3 |
3,1 |
|
|
|
2 |
9,7 |
|
|
|
|
|
|
3 |
9,8 |
|
|
|
|
|
|
4 |
9,6 |
|
|
|
|
|
|
5 |
9,1 |
|
|
|
|
|
|
6 |
10,1 |
|
|
|