Материал: Оптимизация методик определения концентрации железа (III) в полиэлектролитных микрокапсулах и магнитоуправляемых липосомах
Оптимизация методик определения концентрации железа (III) в полиэлектролитных микрокапсулах и магнитоуправляемых липосомах
Федеральное государственное бюджетное образовательное
учреждение высшего профессионального образования
«МОРДОВСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ им. Н. П. ОГАРЁВА»
Институт физики и химии
Кафедра общей физики
БАКАЛАВРСКАЯ РАБОТА
ОПТИМИЗАЦИЯ
МЕТОДИК ОПРЕДЕЛЕНИЯ КОНЦЕНТРАЦИИ ЖЕЛЕЗА (III)
В ПОЛИЭЛЕКТРОЛИТНЫХ МИКРОКАПСУЛАХ И МАГНИТОУПРАВЛЯЕМЫХ ЛИПОСОМАХ
Саранск 2015
Реферат
Объекты исследования: полиэлектролитные микрокапсулы, магнитоуправляемые липосомы
Цель работы: подбор оптимального метода количественного определения железа (III) в магнетитсодержащих контейнерах для направленной доставки лекарств (полиэлектролитных микрокапсулах и магнитоуправляемых липосомах).
Методы исследования: метод комплексонометрического титрования, метод фотоколориметрии, метод ЭПР-спектроскопии.
Полученные результаты: показано, что
фотоколориметрический метод может считаться оптимальным для определения
концентрации железа (III)
в синтетических образцах полиэлектролитных микрокапсул и липосом. Так же
показано, что фотоколориметрический метод может использоваться в качестве
эталонного метода, для калибровки ЭПР-спектрометра по определению концентрации
магнетита. В процессе выполнения настоящей работы предложен метод, дающий
возможность определения концентрации магнетита в биообразцах, содержащих
ионизированное железо, этим методом является ЭПР-спектроскопия.
ВВЕДЕНИЕ
Актуальность проблемы. В настоящее время ведутся активные поиски путей снижения токсичности и повышения избирательности лекарственной терапии. Одним из таких путей является создание таргетных форм лекарств, управляемых с помощью внешних воздействий (постоянное и переменное электромагнитное поле, ультразвук и др.). Примером данного подхода может служить магнитоуправляемые лекарственные препараты. Они были предложены в 70-е годы ХХ века и представляют собой комплекс ферромагнетика и лекарственного препарата [1]. Такое сочетание может позволить концентрировать лекарство в зоне патологического очага с помощью постоянного магнита или значимо повышать локальную температуру путем воздействия СВЧ-излучением. В ранних работах по магнитоуправляемому транспорту лекарств сообщалось о создании конъюгатов наночастиц магнетита с лекарственными препаратами. Недостатками таких конструкций были невысокая «лекарственная емкость» и сложность получения обратимо диссоциирующих комплексов лекарства и ферромагнетика. В связи с этим, современные исследования направлены на создание магнитоуправляемых микро- и наноконтейнеров, в которые инкапсулируется лекарственный препарат. В начале XXI века были предложены полиэлектролитные микрокапсулы, получаемые по технологии Layer-by-layer, с инкорпорированными между слоями полимеров наночастицами магнетита [2]. До настоящего времени для определения концентрации железа в микрокапсулах и других экспериментальных магнитоуправляемых системах использовались простые, но не обладающие достаточной точностью методы - гравиметрия и косвенный расчетный метод [3] и др. Применение микрокапсул in vivo требует более точной их стандартизации по качественному и количественному составу, в частности - по массовой концентрации магнетита и/или железа (III). В связи с этим необходим подбор оптимального метода, позволяющего с достаточной точностью определять содержание железа (III) в микрокапсулах. Еще одной важной задачей, возникающей при применении магнитных микрокапсул in vivo, является необходимость их идентификации в биосредах, имеющих в своем составе ионизированное железо (III). Химические методы в данном случае неприменимы, так как не позволяют дифференцировать эндогенное и экзогенное железо (III). Одним из методов, позволяющих идентифицировать магнетит в различных объектах, является ЭПР-спектроскопия. Однако сообщений о применении этого метода для количественного определения железа (III) в биосредах мы не встретили. Данные обстоятельства и послужили основанием для проведения настоящего исследования.
Цель работы: подбор оптимального метода количественного определения железа (III) в магнетитсодержащих контейнерах для направленной доставки лекарств (полиэлектролитных микрокапсулах и магнитоуправляемых липосомах).
Задачи исследования:
. Проанализировать применимость комплексонометрического титрования для определения концентрации железа (III) в полиэлектролитных микрокапсулах и магнитоуправляемых липосомах
. Проанализировать применимость фотоколориметрии для определения концентрации железа (III) в полиэлектролитных микрокапсулах и магнитоуправляемых липосомах.
. Проанализировать возможность применения метода ЭПР-спектроскопии для определения концентрации магнетита в синтетических объектах и биологических средах.
. Провести сравнительный анализ результатов по
определению концентраций железа (III)
в полиэлектролитных микрокапсулах и магнитоуправляемых липосомах данных методов
1. Литературный обзор.
Характеристика методов определения концентрации химических элементов в сложных
соединениях
В последнее время широко применяются лекарства в
виде коллоидов микроскопических капсул и липосом [4,5], которые применяются для
лечения определенных заболеваний. В качестве защиты лекарственных средств от
нежелательного воздействия среды организма применяется полимерное покрытие а
также бислой фосфолипидов, в которых включен магнетит или его аналоги для того,
чтобы можно было доставлять и концентрировать защищенное лекарство в нужной
области. Определение концентрации железа (III),
магнетита в полиэлектролитных микрокапсулах и магнитоуправляемых липосомах
является важнейшей задачей для характеристики препаратов содержащих магнитные
вещества, в качестве агента по доставке и концентрированию лекарственных
средств внутри пораженных, различными заболеваниями, частях тела. Для
определения концентрации железа в препаратах, автором работы был выполнен обзор
соответствующей литературы, выбраны наиболее доступные и простые в плане
подготовки и аппаратуры методы которые будут рассмотрены ниже.
1.1 Метод
комплексонометрического титрования
Метод комплексонометрии основан на реакциях, которые сопровождаются образованием комплексных соединений катионов с органическими реактивами - комплексонами. При этом образуются комплексные соединения, которые называют внутрикомплексными или хелатными комплексными соединениями. Комплексонами называют органические соединения, представляющие собой производные аминополикарбоновых кислот [6,7]. к таким кислотам относится этилендиаминтетрауксусная кислота (ЭДТА).
ЭДТА (ТРИЛОН Б) образует со многими катионами
металлов устойчивые мало диссоциируемые растворимые в воде внутрикомплексные
соли. В комплексах часть связей носит ионный характер, часть -
донорно-акцепторный. ЭДТА с ионами металлов любого заряда образует
четырех-пяти- или шести координационный комплекс с пятичленными циклами. Атом
металла находится в окружении атомов кислорода и атомов азота, находящихся в
цис-положении.
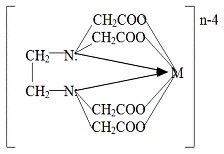
Рис.1.1.1 Структурная формула ЭДТА
В реакциях комплексообразования
реакции между ТРИЛОНОМ Б и ионами металлов протекают стехиометрически в
соотношении 1 : 1. Следовательно, молярная масса эквивалента ЭДТА и
определяемого иона металла равны их молярным массам. При титровании ЭДТА солей
металлов комплексообразователей протекают следующие реакции:
Ме2+ + Н2Y 2- → МеY2- + 2 Н+
Ме3+ + Н2Y 2- → МеY- + 2 Н+
Из приведенных реакций следует, что на 1 моль ионов металла, независимо от степени окисления металла, идет 1 моль ТРИЛОНА Б и освобождается 2 моль ионов водорода. Образующиеся комплексные соединения различаются лишь по заряду. Ионы водорода понижают рН раствора, в результате повышения кислотности среды требуемого комплексного соединения может не получиться [8,9].
Поэтому титрование проводят в
буферном растворе, поддерживающем определенное значение рН. Все это позволяет
использовать ЭДТА для титриметрического определения солей металлов.
1.2 Метод
фотоколориметрии
По сравнению с другими методами фотоколориметрический метод является наиболее объективным и дает более точные данные. Принцип работы фотоколориметра заключается в следующем, световой поток, проходя через окрашенный раствор, поглощается не полностью. Часть светового потока, прошедшего через раствор, попадает на фотоэлемент, который преобразует световую энергию в электрический ток. Возникающий в фотоэлементе ток регистрируется с помощью микроамперметра [10].
Фотоколориметры предназначены для измерения оптической плотности растворов в диапазоне 200-900 нм.
Оптическую плотность стандартного и анализируемого растворов всегда измеряют по отношению к раствору сравнения, или нулевому раствору. В качестве такого раствора можно использовать раствор, содержащий все добавляемые реактивы, кроме определяемого вещества. Если же все компоненты раствора сравнения и добавляемый реагент бесцветны и, следовательно, не поглощают оптического излучения в видимой части спектра, то в качестве раствора сравнения можно использовать дистиллированную воду.
Определение концентрации растворов
на фотоколориметрах проводят обычно с помощью градуировочного графика
(рис.1.2.1.).
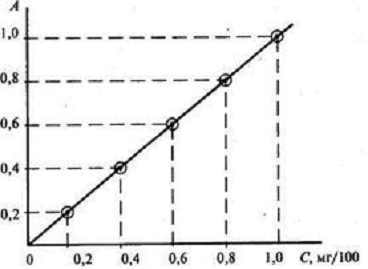
Рис.1.2.1. Пример градуировочного
графика для определения концентрации фотоколориметрическим методом
Градуировочный график отражает связь между оптической плотностью А и концентрацией С. Оптическую плотность называют также абсорбцией (А). Для построения градуировочного графика готовят стандартный раствор, содержащий строго определенное количество исследуемого вещества. С этой целью точно измеренные объемы исходного стандартного раствора, содержащего определенную концентрацию исследуемого вещества, переносят в мерные колбы вместимостью 100 или 50 мл и добавляют соответствующие реактивы, вызывающие окраску анализируемого раствора. Затем содержимое каждой колбы доводят дистиллированной водой до метки. Определение оптической плотности приготовленных стандартных растворов начинают с раствора, окрашенного слабее других, соответственно этот раствор обладает меньшей концентрацией по сравнению с другими растворами. По полученным данным строят градуировочный график.
В дальнейшем по градуировочному
графику определяют концентрацию вещества в анализируемом растворе, зная его
оптическую плотность [10].
1.3 Метод
электронного парамагнитного резонанса
Метод ЭПР является основным методом для изучения парамагнитных частиц присутствующих в биологических системах. К парамагнитным частицам имеющим важное биологическое значение относятся два главных типа соединений - это свободные радикалы и металлы переменной валентности (такие как Fe, Cu, Co, Ni, Mn) или их комплексы. Кроме свободнорадикальных состояний методом ЭПР исследуют триплетные состояния, возникающие в ходе фотобиологических процессов [11].
Орбитальное и спиновое движение
электронов лежат в основе существовании у них орбитального и спинового
механических моментов. Магнитный момент электрона складывается в общем случае
из спинового и орбитального магнитных моментов. Однако, в большинстве случаев,
орбитальный магнитный момент равен нулю. Поэтому при обсуждении принципа метода
ЭПР будет рассматриваться только спиновый магнитный момент. В отсутствие
внешнего магнитного поля магнитные моменты электронов ориентированы случайным
образом (рис. 1.3.1. А), и их энергия практически не отличается друг от друга
(Е0). При наложении внешнего магнитного поля магнитные моменты электронов
ориентируются в поле в зависимости от величины спинового магнитного момента
(рис. 1.3.1. Б), и их энергетический уровень расщепляется на два (рис. 1.3.2.).
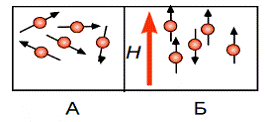
Рис.1.3.1. Ориентация магнитных моментов электронов А) в отсутствии внешнего магнитного поля Б) во внешнем магнитном поле Н
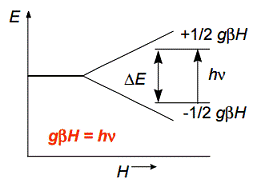
Рис.1.3.2. расщепление
энергетических уровней одиночных электронов в магнитном поле (эффект Зеемана),
где H напряжение
магнитного поля, g коэффициент пропорциональности
Уравнение
![]() (1)
(1)
описывает эффект Зеемана, который заключается в следующем: энергетические уровни электронов, помещенных в магнитное поле, расщепляются в этом поле в зависимости от величины спинового магнитного момента и интенсивности магнитного поля.
Основное уравнение резонанса.
Количество электронов, имеющих ту или иную энергию, будет определяться в
соответствии с распределением Больцмана, а именно
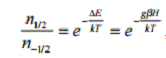 (2)
(2)
где n1 и n2 количество электронов на более высоком или более низком энергетическом уровне, соответствующем магнитному моменту электрона со спином +1/2 или -1/2
Если теперь на систему электронов, находящуюся в магнитном поле, подать электромагнитную энергию, то при определенных значениях величины энергии падающего кванта будут происходить переходы электронов между энергетическими уровнями. Необходимым условием переходов является равенство энергии падающего кванта (hν) разности энергий между уровнями электронов с различными спинами (gβH).
Уравнение ΔE=hν=gβH выражает основное условие поглощения энергии электронами. Под влиянием излучения электроны, находящиеся на более высоком энергетическом уровне, будут испускать энергию и возвращаться на нижний уровень. Электроны же, находящиеся на нижнем уровне, будут поглощать энергию и переходить на более высокий энергетический уровень, это явление называется резонансным поглощением. Поскольку вероятности одиночных переходов между энергетическими уровнями равны, а общая вероятность переходов пропорциональна количеству электронов, находящихся на данном энергетическом уровне, то поглощение энергии будет преобладать над ее излучением.
Необходимо отметить особое положение свободных радикалов, то есть молекул, имеющих не спаренные электроны на внешней электронной, в распределении электронов по уровням энергии. Если на орбитали имеется парное количество электронов, то заселенность энергетических уровней будет одинакова и количество поглощенной энергии электронами будет равно количеству излученной энергии [12].
Площадь под линией поглощения образца пропорциональна концентрации парамагнитных частиц в нем. Таким образом, концентрация парамагнитных центров пропорциональна первому интегралу под линией поглощения или второму интегралу от спектра ЭПР.
железо полиэлектролитный микрокапсула магнитоуправляемый
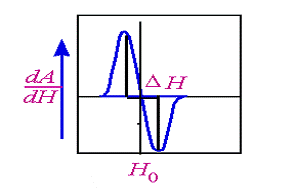
Рис.1.3.3. ЭПР-спектр, первая производная
поглощения амплитуды (А) по магнитному полю (Н)
Для определения концентрации измеряют площади
под кривой поглощения у эталона с известной концентрацией парамагнитных центров
[13] и у измеряемого образца и неизвестную концентрацию находят из пропорции,
при условии, что оба образца имеют одинаковую форму и объем:
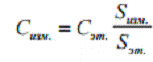 (3)
(3)
2. Описание
экспериментальных методик определения концентрации железа (III) в
магнитоуправляемых липосомах и полиэлектролитных микрокапсулах
В данной работе нами были применены и апробированы различные методы определения концентрации железа (III) [14,15,16] в выбранных нами объектах. Методы отличаются друг от друга сложностью выполнения, а также аппаратной частью.
Фотоколориметрический метод заключается в
анализе оптической плотности окрашенного раствора, содержащего неизвестную
концентрацию определяемого вещества. Комплексонометрическое титрование
позволяет определять концентрацию вещества по объему титранта при котором
окраска раствора полностью исчезает, ЭПР-спектроскопия позволяет определять
концентрацию по средством определения площади под кривой спектра поглощения.
следует заметить, что каждый из перечисленных методов имеет определенные
достоинства и недостатки которые будут перечислены ниже.
2.1 Методика
определения концентрации железа (III) в магнитоуправляемых липосомах и полиэлектролитных
микрокапсулах методом комплексонометрического титрования