Материал: Оптимизация методик определения концентрации железа (III) в полиэлектролитных микрокапсулах и магнитоуправляемых липосомах
Для определения концентрации железа (III) использовали метод комплексонометрического титрования, описанный в [17].
Принцип метода. Метод основан на обесцвечивании фиолетового раствора сульфосалицилата железа при взаимодействии с ТРИЛОНОМ Б (ЭДТА). Реактивы
Сульфосалициловая кислота (C7H6O6Sx2H2O)
ТРИЛОН Б(C10H14O8N2Na2*2H2O)
Вода дистиллированная
Оборудование
Штатив
Бюретка 20мл
дозатор автоматический biohit 1мл
Коническая колба 250мл
Весы аналитические
Методика титрования
Перед анализом необходимо подготовить раствор
ТРИЛОНА Б нужной концентрации и соответственно пробу в которой будет
определяться железо. Раствор ТРИЛОНА Б готовится по формуле
Сэ(эдта)=m(навески)/(Мэ(ЭДТА)*Vколбы)
Подробное описание пробоподготовки приведено в [18].
Подготовленную пробу известного объема титруют до полного обесцвечивания, при этом по каплям приливал из бюретки раствор ТРИЛОНА Б, энергично перемешивая колбу с образцом. После того как образец практически полностью обесцветился, определяется объем титранта использованного для анализа. Затем добавляется еще несколько капель для проверки правильности анализа. Если образец не изменяет окраску, значит определенный объем титранта был правильный. Если происходит изменение окраски, значит процедуру нужно было повторять до того момента, когда изменение цвета образца прекратилось.
Обработка результатов
Расчет концентрации железа (III) производилось по формулам:
(Fe(III)) = ((Cэ ∙ Vср)(ТРИЛОНА Б) ∙ Mэ(Fe) ∙ V(всего исследуемого раствора)) / (1000 ∙ V(пробы))
C(Fe в коллоиде магнетита) = m(Fe(III)) / V(маг. жидкости)
2.2 Методика
определения концентрации железа (III) в магнитоуправляемых липосомах и полиэлектролитных
микрокапсулах методом фотоколориметрии
Метод основан на взаимодействии ионов железа в щелочной среде с сульфосалициловой кислотой при этом происходит образование окрашенного в желтый цвет комплексного соединения [19,20]. Интенсивность окраски, пропорциональна массовой концентрации железа (III).
Измерения проводили при длине волны 430 нм, так как на этой длине волны наблюдается максимальное поглощение раствора железа (III), подготовленного из полиэлектролитных микрокапсул и магнитоуправляемых липосом.
Следует заметить, что на длине волны 430 нм не наблюдается поглощения самими капсулами и липосомами что свидетельствует о корректном выборе этой длины волны, для проведения измерений
Реактивы, использованные для реализации фотоколориметрических измерений
железоаммонийные квасцы 12-водные кристаллогидраты (FeNH4(SO4)2 x12H2O)
соляная кислота 37% (HCl)
сульфосалициловая кислота (кристаллы (C7H6O6Sx2H2O))
хлорид аммония (кристаллы (NH4Cl))
пероксид водорода 6% (H2O2)
аммиак раствор 1:1 (NH4OH)
вода дистиллированная
Оборудование, использованное для осуществления спектрофотометрических измерений
спектрофотометр марки shimadzu uv2600
весы аналитические axis
дозатор автоматический biohit 1мл
колбы 50мл
колба 1000мл
колба 25мл
Описание методики пробоподготовки образцов и проведения спектрофотометрических измерений
1. Приготовление основного
стандартного раствора железоаммонийных квасцов: 0,8636 г железоаммонийных
квасцов (FeNH4(SO4)2×12H 2O)
взвешивали с точностью до 0,0002 г по шкале
<#"868167.files/image009.gif">а) б)
б)
Рис.3.1.1 а) Фотографии взвеси
микрокапсул до обработки концентрированной соляной кислотой рис.3.1.1. б)
фотография капсул после обработки концентрированной соляной кислотой
При добавлении концентрированной соляной кислоты в суспензию магнитоуправляемых липосом эмульсия расслаивалась на раствор хлоридов железа и жиры, поскольку липосомы имеют наноразмеры, в следствии этого не возможно визуально наблюдать их в оптический микроскоп, для решения этой проблемы был использован метод атомно-силовой микроскопии (АСМ) рисунок 3.1.2.
 а)
а) 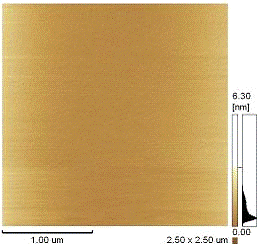 б)
б)
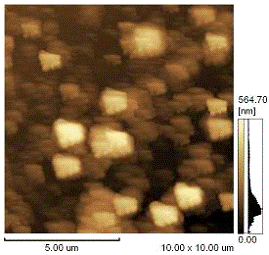
Рис.3.1.2. а) АСМ фотография
образцов липосом до обработки концентрированной соляной кислотой рис.3.1.2. б)
липосомы после добавления концентрированной соляной кислоты
На рисунке 3.1.2 представлены АСМ-изображения образцов магнитоуправляемых липосом до и после обработки. До обработки наблюдаются сферические структуры, после обработки концентрированной соляной кислотой каких либо структур не обнаружено.
Таким образом было установлено, что
обработка концентрированной соляной кислотой позволяет, полностью перевести
наночастицы магнетита в ионизированную форму, концентрация которых в дальнейшем
может быть определенна физико-химическими методами.
3.2
Результаты определения концентрации железа (III) в полиэлектролитных микрокапсулах и
магнитоуправляемых липосомах методом комплексонометрического титрования
Специфичность метода характеризуется точностью определения требуемого аналита в исследуемом объекте. В нашем случае в исследуемом объекте присутствуют различные компоненты: в частности в полиэлектролитных микрокапсулах это смесь растворов полимеров, а в магнитоуправляемых липосомах смесь фосфолипидов. Для определения специфичности метода, нами был выполнен анализ влияния указанных выше компонентов на результаты определения железа в исследуемых образцах. Для этой проверки выполнялись следующие эксперименты. Для полиэлектролитных микрокапсул и липосом не содержащих наночастицы магнетита (холостая проба), а также полиэлектролитных микрокапсул, магнитоуправляемых липосом содержащих наночастицы магнетита (опытный). В холостых пробах при добавлении сульфосалициловой кислоты не замечено наличие фиолетовой окраски, которая характерна для комплекса сульфосалицилата железа. В опытных пробах при добавлении к лизату полиэлектролитных капсул и магнитоуправляемых липосом наблюдалась фиолетовая окраска. Данный факт специфичен для комплекса железа с сульфосалициловой кислотой. На основе этого следует вывод о том, что в лизатах образцов отсутствуют вещества, которые могут вносить погрешность при определении железа (III).
Так как суспензии полиэлектролитных
микрокапсул и магнитоуправляемых липосом изготавливаются в малых объемах и их
синтез имеет высокую себестоимость, объем исследуемого образца был ограничен и
составлял 0,1мл с синтеза. Оценка нижнего предела количественного определения
железа (III) методом
комплексонометрического титрования проводилась следующим образом: исследовали
стандартные растворы железоаммонийных квасцов (FeNH4(SO4)2 ) в концентрациях
равных 10мг/л; 100мг/л; 200мг/л. Возможность проведения титрования оценивали по
образованию визуально различимой фиолетовой окраски результаты исследования представлены
в таблице 1.
Таблица 1 Нижний предел количественного определения титрования
|
Взятая концентрация, мг/л |
№ Определения |
Наличие визуально различимой окраски железа с сульфосалициловой кислотой |
Объем титранта, мл |
Средний объем, мл |
Погрешность |
Относительная погрешность, % |
|
10 |
1 |
- |
- |
- |
- |
- |
|
|
2 |
- |
- |
|
|
|
|
|
3 |
- |
- |
|
|
|
|
100 |
1 |
Фиолетовая окраска |
1,5 |
1,70 |
0,20 |
11,76 |
|
|
2 |
Фиолетовая окраска |
1,7 |
|
|
|
|
|
3 |
Фиолетовая окраска |
1,9 |
|
|
|
|
200 |
1 |
Фиолетовая окраска |
2,6 |
2,57 |
0,15 |
5,95 |
|
|
2 |
Фиолетовая окраска |
2,7 |
|
|
|
|
|
3 |
Фиолетовая окраска |
2,4 |
|
|
|
Как видно из таблицы образование визуально различимой окраски происходило при концентрации железоаммонийных квасцов (FeNH4(SO4)2 ) начиная с 100мг/л, эта концентрация была принята за нижний предел количественного определения. Следует отметить, что относительная погрешность определения концентрации железа (III) в области НПКО была выше чем в области других концентраций.
Для проверки гипотезы о линейной зависимости между объемом титранта и концентрацией железа (III) в образце было проведено определение железа (III) в растворах с его известной концентрацией 1)100 мг/л; 2) 200 мг/л; 3) 400 мг/л; 4) 600 мг/л; 5) 800 мг/л; 6)1600 мг/л.
Эксперимент по определению концентрации железа (III)
проводили не менее 3 раз. Рассчитывали среднее значение объема титранта.
Погрешность эксперимента определялась, как стандартное отклонение,
относительную погрешность определяли как отношение стандартного отклонения к
средней величине. Результаты исследования и соответствующие значения
погрешностей представлены в таблице 2.
Таблица 2 Калибровка комплексонометрического титрования
|
Взятая концентрация, мг/л |
№ Определения |
Объем титранта, мл |
Средний объем, мл |
Погрешность |
Относительная погрешность, % |
|
100 |
1 |
1,7 |
2,1 |
0,20 |
18,94 |
|
|
2 |
2,2 |
|
|
|
|
|
3 |
2,5 |
|
|
|
|
200 |
1 |
4,5 |
4,2 |
0,17 |
4,12 |
|
|
2 |
4,5 |
|
|
|
|
|
3 |
4,2 |
|
|
|
|
400 |
1 |
8,3 |
8,3 |
0,20 |
2,40 |
|
|
2 |
8,5 |
|
|
|
|
|
3 |
8,1 |
|
|
|
|
600 |
1 |
7,6 |
12,5 |
0,15 |
1,22 |
|
|
2 |
7,8 |
|
|
|
|
|
3 |
7,5 |
|
|
|
|
800 |
1 |
16,5 |
16,5 |
0,06 |
0,34 |
|
|
2 |
16,5 |
|
|
|
|
|
3 |
16,6 |
|
|
|
|
1600 |
1 |
31,5 |
31,5 |
0,06 |
0,18 |
|
|
2 |
31,5 |
|
|
|
|
|
3 |
31,4 |
|
|
|
На рисунке 3.2.1. представлена корреляционная
зависимость объема титранта от концентрации железа (III).
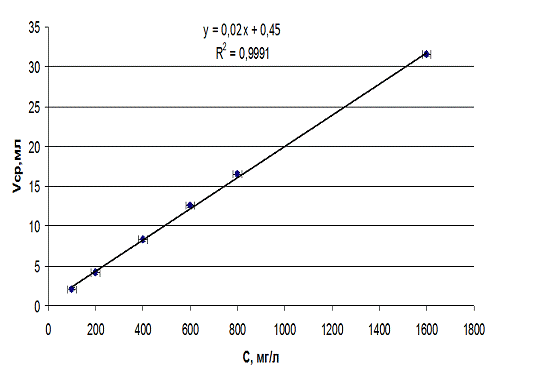
Рис.3.2.1 Калибровочный график для определения
концентрации железа (III)
методом комплексонометрического титрования
Из приведенного на рисунке 7 графика видно, что в исследуемом диапазоне концентраций эта зависимость линейна. Уравнение линейной регрессии имеет вид y=0,02x+0,45 коэффициент корреляции R2 = 0,999
Относительная ошибка составляет 0,18-19% в зависимости от диапазона измеряемых концентраций, она увеличивается в области малых концентраций. Таким образом метод комплексонометрического титрования позволяет с достаточной точностью определить железо (III) в образцах полиэлектролитных микрокапсул и магнитоуправляемых липосом, при условии если концентрация железа в них превышает 10мг/л.
Выше описанный метод были использованы для определения концентрации железа (III) в образцах полиэлектролитных микрокапсул и магнитоуправляемых липосом, для исследования были предоставлены по три образца полиэлектролитных микрокапсул (в дальнейшем МК1, МК2, МК3) и три образца магнитоуправляемых липосом(в дальнейшем Л1, Л2, Л3) синтезированных в разное время.
Пробоподготовка взвеси полиэлектролитных микрокапсул и магнитоуправляемых липосом проводилось по методике описанной ниже [24] производили следующим образом:
Для выделения железа из полиэлектролитных микрокапсул и магнитоуправляемых липосом использовали концентрированную соляную кислоту. Суспензию полиэлектролитных микрокапсул и магнитоуправляемых липосом 1 мл растворяли 1мл 37% HCl. Многослойные микрокапсулы формируются слабыми полиэлектролитами чувствительными к pH среды, они становятся незаряженными, что приводит к разрушению капсулы [25]. В результате этого капсулы подвергаются деструкции, а освободившийся магнетит растворяется кислотой с образованием соответствующих солей железа (II, III). Липосомы под действием концентрированной соляной кислоты раскрываются, содержащийся в них магнетит высвобождается, под действием кислоты превращается в. соли железа (II, III).Образцы, растворенные в кислоте, необходимо нагреть на водяной бане при температуре 80-900С с добавлением 1мл H2O2 6% для того чтобы все железо перешло в степень окисления (III) и довести объем до 50 мл.
Результаты определения концентраций железа (III)
в образцах комплексонометрическим титрованием представлены в таблице 3.
Таблица 3 Результаты определения концентрации железа (III) в образцах комплексонометрическим титрованием
|
№ |
Vпроб.,мл |
Vтитр.,мл |
<V>, мл |
Погрешность |
Относительная погрешность, % |
mх, мг |
С(Fe3+), мг/л |
|
Мк1 |
10 |
1,6 |
1,53 |
0,06 |
3,76 |
0,13 |
643 |
|
|
10 |
1,5 |
|
|
|
|
|
|
|
10 |
1,5 |
|
|
|
|
|
|
Мк2 |
10 |
2,0 |
2,27 |
0,25 |
11,10 |
0,19 |
953 |
|
|
10 |
2,5 |
|
|
|
|
|
|
|
10 |
2,3 |
|
|
|
|
|
|
Мк3 |
10 |
2,7 |
2,70 |
0,20 |
7,41 |
0,23 |
1134 |
|
|
10 |
2,9 |
|
|
|
|
|
|
|
10 |
2,5 |
|
|
|
|
|
|
Л1 |
10 |
3,9 |
3,93 |
0,06 |
1,46 |
0,33 |
1651 |
|
|
10 |
3,9 |
|
|
|
|
|
|
|
10 |
4,0 |
|
|
|
|
|
|
Л2 |
10 |
2,9 |
2,83 |
0,06 |
2,04 |
0,24 |
1191 |
|
|
10 |
2,8 |
|
|
|
|
|
|
|
10 |
2,8 |
|
|
|
|
|
|
Л3 |
10 |
0,6 |
0,73 |
0,15 |
20,83 |
0,06 |
305 |
|
|
10 |
0,9 |
|
|
|
|
|
|
|
10 |
0,7 |
|
|
|
|
|