Материал: Оптимизация керамической технологии
Для практического применения важно также обеспечить минимальный уровень магнитных потерь, что достигается еще более медленным охлаждением образцов, чем в описанных выше экспериментах. К сожалению, при этом радикально изменяется распределение катионов, установившееся при высокотемпературном равновесии, возрастает вероятность изменения содержания кислорода и появляются градиенты свойств по объему [6].
Влияние условий обжига в
вакууме на свойства ферритов изучено достаточно подробно, а газотермических
режимов - не столь детально. Наиболее приближен к равновесию (при ![]()
![]() = 20
= 20![]()
![]() 10-3) V
режим, который является самым окислительным. Его маршрут пересекает
высококислородную границу шпинельного поля при наиболее высокой (~1100°С)
температуре, что связано с повышенной опасностью распада шпинельной фазы при
охлаждении [6].
10-3) V
режим, который является самым окислительным. Его маршрут пересекает
высококислородную границу шпинельного поля при наиболее высокой (~1100°С)
температуре, что связано с повышенной опасностью распада шпинельной фазы при
охлаждении [6].
При охлаждении по I-IV режимам от 1330 до 1200°С феррит окисляется в среде воздуха при атмосферном давлении. При температурах ниже 1200°С феррит сначала восстанавливается, а затем, при еще более низких температурах, окисляется. Интенсивность восстановления и окисления усиливается от IV к I режиму[6].
Охлаждение по ступенчатым программам приводит к окислению феррита в интервале температур 1330-1300 °С, затем - к восстановлению при 1300 °С и окислению во время дальнейшего охлаждения [6].
Таблица 4.1. Электромагнитные свойства Mn-Zn-ферритов
марки 2500НМС-2 в зависимости от содержания кислорода
Содержание кислорода Руд, Вт/м3 100°С
25°С
25°С
100°С
15
5,9
8,1
0,343
5890
6010
10
5,6
7,8
0,350
6000
5970
5
7,1
7,7
0,338
5490
5100
1
9,8
7,9
0,318
4480
3520
5. Особенности строения Твердые растворы системы MnFe2О4
- ZnFe2О4
обладают наибольшим значением магнитной проницаемости по сравнению со всеми
другими феррит-шпинелями и их твердыми растворами. Промышленность выпускает
марганеццинковые ферриты с проницаемостью до 6000; в лаборатории получены
ферриты с проницаемостью до 20000. Несмотря на это, промышленное производство
ферритов рассматриваемой системы началось значительно позднее, чем производство
никельцинковых ферритов. Причины этого кроются в серьезных технологических
трудностях, связанных с получением марганцевых ферритов [9].
Марганцевая шпинель MnFe2О4
устойчива выше 1200°С, при охлаждении происходит окисление марганца по схеме:
Mn2+-е
Марганцевая шпинель при этом
распадается на Мn2О3
и Fe2О3,
которые образуют между собой твердые растворы [9].
Таким образом, получить MnFe2О4
обжигом на воздухе практически невозможно - неизбежно появление ионов Мn3+, а это
ведет к ухудшению свойств ферритов [9].
Быстрое охлаждение марганцевых
ферритов в интервале 1100-250°С позволяет в известной мере избежать окисления Мn2+ в Мn3+ и, тем самым,
сохранить магнитные свойства, однако механические свойства таких ферритов
весьма низки.
Фактически промышленное производство
марганеццинковых ферритов началось после разработки режимов охлаждения в
вакууме и в инертных средах. В таком случае удается избежать окисления Мn2+ и получать
ферриты со стабильными свойствами.
В производстве марганцевых ферритов
давление кислорода оказывает влияние не только на разупорядоченность феррита,
как полупроводника, но и на валентное состояние ионов марганца. Отсюда вытекает
важность учета такого фактора, как давление кислорода, для технологии
марганцевых ферритов и построения диаграмм состояния с участием окислов
марганца[9].
В системе MnFe2O4 - ZnFe2O4 существует
непрерывный ряд твердых растворов, однако линии ликвидуса и солидуса не
определены. Построение этих линий затруднено из-за летучести ZnFe2O4 и
нестабильности валентных состояний ионов марганца. Чистый MnFe2O4 плавится
при 1580 °С, однако состав феррита, возможно, отличается от стехиометрического.
Твердые растворы ферритов марганца и
цинка образуются во всем интервале концентраций нагреванием при 1200 °С [9].
Определение области
шпинелеобразования в системе Mn-Zn-Fe-О не
проведено; весьма малочисленны также исследования в области псевдотройной
диаграммы MnO-ZnO-Fe2O3. Последняя
диаграмма имеет наибольшее значение для технологии, так как сырьем являются
именно эти окислы [9].
Система MnO- Fe2O3 может быть
построена в атмосферных условиях только для температур выше 1000° С, так как
при более низких температурах устойчива Мn2O3. Диаграмма
равновесия Мn2O3-Fe2O3 была
определена на воздухе. Фактически эта диаграмма до 1000 °С соответствует
равновесию в системе Мn2O3-Fe2O3, а выше
1000 °С в системе MnO-Fe2O3 [9].
Диссоциация Мn2O3 происходит
примерно при 900°С и с увеличением содержания Fe2O3 повышается
до 1000° С. Выше 1000°С появляется фаза
шпинели MnFe2O3, которая
устойчива до 1600°С. Из диаграммы состояния так же следует, что при обжиге
марганцевых ферритов температура спекания (1300- 1400 °С) совпадает с
температурой области устойчивости шпинели, однако при охлаждении в интервале
900-1000 °С происходит валентное превращение марганца, которое приводит к
распаду шпинели[9].
Предотвращение этого распада и
является основной задачей технологии марганцевых ферритов[9].
В области составов, соответствующих
стехиометрической шпинели (х Mn2++Fe2+ Получение
стехиометрической шпинели с Mn2++Fe2+ Третья двойная диаграмма
- МnО-ZnO ограничивающая
треугольник МnО-ZnO-Fe2O3,
не исследована, отсутствуют также данные о растворимости этих соединений друг в
друге. Учитывая, что МnО
имеет кубическую структуру типа NaCl,
a ZnO гексагональную, большой растворимости этих соединений друг в
друге вряд ли можно ожидать [9].
Поэтому трудно сказать, соответствует ли
представленный разрез составу при 1370 °С, или же в процессе охлаждения произошло
его изменение. На диаграмме можно выделить несколько полей сосуществования
равновесных фаз. Наиболее важна область I, где имеется одна фаза со структурой
шпинели. В этой области фактически лежат все составы промышленных ферритов [9].
Область II
соответствует двухфазному равновесию шпинели с Fe2O3,
область III - также двухфазному равновесию шпинели с ZnO.
О равновесии фаз в области IV нет сведений, однако, исходя из общих правил, в
данной области равновесия возможны три фазы: шпинель - ZnO-МnО
в области составов со структурой шпинели линии ОМ и О'М' фиксируют границы
тетрагонального искажения кубической решетки шпинели при введении избытка МnО
(ОМ-по данным рентгенографии, О'М' - по данным микроскопии) [7].
Тетрагональное искажение кубической решетки
шпинели с введением избытка МnО
указывает на появление в системе гаусманита Мn3O4,
т.е.
точки составов начинают выпадать из поля данной тройной диаграммы. Связано это,
как указывалось, с отсутствием контроля за давлением кислорода при построении
изотермического разреза. Твердые растворы шпинели с Fe2O3
в данном случае, как и в системе NiO-ZnO-Fe2O3,
являются метастабильными.
Для марганцевых ферритов диаграммы состав -
свойство, полученные различными авторами, имеют значительные расхождения
численных величин. Причины понятны из изложенного выше. Зависимость свойств
марганцевых ферритов от давления кислорода приводит к большому их разбросу, так
как стабильно выдержать этот параметр в технологии трудно.
Значения магнитной проницаемости,
значительно отличаются, а если учесть, что были получены ферриты с
проницаемостью 20000, то можно оценить роль технологических факторов в
получении марганцевых ферритов. Несмотря на различие в численных величинах,
максимум свойств наблюдается при х а) tg При спекании марганеццинковых ферритов не
следует забывать, что возможно испарение цинка, так как температура спекания
лежит в интервале 1300-1400 °С, а диссоциация ZnFe2O4
при этих температурах велика [7].
По виду диаграммы, состав - свойство можно
судить о влиянии неточностей при изготовлении шихты. Даже при значительных
отклонениях от стехиометрических составов образцы Mn1xZnxFe2O4
будут однофазными и со структурой шпинели [7].
Значения магнитной проницаемости для образцов
рассматриваемой системы (Зависимость некоторых свойств ферритов Mn1-xZnxFe2O4 от состава) значительно различаются
и весьма существенно зависят от режима охлаждения, вернее от характера газовой
среды при охлаждении.
Несмотря на то, что введение избыточных МnО
и ZnO не приводит к
образованию второй фазы, магнитная проницаемость уменьшается [7].
Очевидно, что растворение в шпинели МnО,
имеющей решетку типа NaCl,
приводит к напряжениям в решетке, а это и ведет к снижению начальной магнитной
проницаемости. Если считать, что фактически в твердый раствор вступает не МnО,
а гаусманит Мn3O4,
то все равно последний имеет тетрагональную решетку, которая также будет
вызывать напряжение в структуре шпинели [7].
Наличие тетрагонального искажения решетки
шпинели при большом избытке МnО
говорит о частичном окислении МnО
в Мn3О4,
который, по всей вероятности, и образует твердые растворы со шпинелью.
Из сказанного следует, что диаграмму
(Зависимость начальной магнитной проницаемости ферритов Mn1-xZnxFe2O4 от избытка оксилов) вряд ли можно
считать равновесной, хотя ценность ее для технологии несомненна.
Влияние избытка Fe2O3
на магнитную проницаемость марганеццинковых ферритов аналогично таковому в
системе NiO-ZnO-Fe2O3.
При небольшом избытке Fe2O3
магнитная проницаемость увеличивается, проходит через максимум и затем резко
падает. Обычно промышленные составы марганеццинковых ферритов имеют небольшой
избыток Fe2O3
(2-3 мол. %), что связано с указанным повышением магнитной проницаемости при
избытке Fe2O3.
Влияние избытков окислов MnO,
ZnO, Fe2O3
на другие свойства аналогично их влиянию на магнитную проницаемость. Например,
в случае удельной намагниченности насыщения (Зависимость некоторых свойств
ферритов системы MnO-ZnO-Fe2O3
от
избытка оксилов ), несмотря на
распад твердого раствора шпинели с Fe2O3
при содержании Fe2O3
более 50 мол. %, резкого уменьшения величины а до
значений, присущих исходным стехиометрическим ферритам, не наблюдается, как это
характерно для системы NiO-ZnO-Fe2O3[7].
Очевидно, в данном случае часть Fe2O3
при термической обработке переходит в Fe3O4
и при распаде метастабильных твердых растворов шпинели Fe2O3
магнетит, образующий стабильные твердые растворы с марганеццинковой шпинелью,
из раствора не выпадает. Таким образом, образующаяся при распаде твердого
раствора шпинель представляет собой не исходную марганеццинковую шпинель, а ее
раствор с Fe3O4,
что подтверждается также изменением параметра решетки. С увеличением избытка Fe2O3
в составах параметр решетки шпинели стремится к 8,39 А0 -величине
параметра решетки магнетита [7].
Некоторые свойства марганеццинковых ферритов
можно улучшить введением малых добавок, при этом, как правило, уменьшается
магнитная проницаемость.
Таким образом, ферриты системы MnO-ZnO-Fe2O3
обладают хорошими электромагнитными свойствами, однако получить стабильные
свойства в данной системе труднее, чем в системе NiO-ZnO-
Fe2O3.
Тем не менее, марганеццинковые ферриты производятся все в большем количестве.
6. Задача Решение
PbO=232,2 SrO=103,6 ZrO2=123,22 TiO2=79,90 Nb2O5=319,6474 PbO=326,0403 Процентный состав
PbO - 65,6531%65,6531%- 1,5610%
1,5610%
ZrO2 - 19,3848% + 5%=24,3048%
TiO2 - 11,5550% 11,5550%2O5
- 1,9261%1,9261%
Расчет навесок с учетом погрешности
PbO SrO ZrO2 TiO2 Nb2O5 Корректировка состава
Пересчет компонентов по ZrO2.
(PbO) 65,6531 -
19,3048
X - 24,3048 X PbO необходимо
добавить 82,6574 (SrO) 1,5610 -
19,3048
X - 24,3048 X SrO необходимо
добавить 1,9653 - 1,5610=0,4043%
(TiO2) 11,5550 -
19,3048
X - 24,3048 X TiO2 необходимо
добавить 14,5478 - 11,5550=2,9928%
(Nb2O5) 1,9261 -
19,3048
X - 24,3048 X Nb2O5 необходимо
добавить 2,4250 - 1,9261=0,4989%
В усреднитель необходимо добавить
следующее количество компонентов для корректировки:
PbO SrO TiO2 Nb2O5 Таким образом, в усреднителе:
PbO =0,5291
(кг)
SrO =0,0221
(кг)
ZrO2=0,1519 (кг)
TiO2=0,1631 (кг)
Nb2O5=0,021 (кг)
монокристалл плавка феррит
нестехиометрия
Выводы
По данной работе можно сделать следующие выводы:
. Основными способами выращивания
монокристаллов являются: выращивание монокристаллов из раствора в расплаве;
метод Вернейля, метод Чохральского; метод Бриджмена; метод зонной плавки;
гидротермальное выращивание; выращивание из паровой фазы. Различия между
методами в технологических установках, схемы которых приведены в работе.
. Описаны процессы кристаллизации и
рекристаллизации. Кристаллизация подразделяется на изотермическу,
изогидрическую, кристаллизацию высаливанием и кристаллизацию в ходе химической
реакции. Процесс рекристаллизации проходит в две стадии: первичная
рекристаллизация, а затем собирательная рекристаллизация.
. Рассмотрен метод совместного
осаждения, сущность которого заключается во взаимодействии щелочных агентов с
водными растворами солей, содержащих катионы разных металлов в том соотношении,
которое необходимо получить в готовом материале. Преимуществами метода
являются: возможность получения смеси исходных компонентов на молекулярном
уровне, снижение температуры синтеза порошков и спекание керамики при
температуре 50-100 оC
за счет высокой дисперсности порошков, выигрыш в электрофизических свойствах
при получении простых составов. Недостатками метода являются: громоздкость
технологических схем, трудность перехода от одного к другому, отсутствие
возможности получения многокомпонентных составов из-за различных условий
осаждения входящих элементов.
. Рассмотрены ферриты, как фазы
переменного состава, что связано с различными видами их нестехиометрии и
дефектности. Приведены структуры ферритов (структура граната, структура
шпинели, структура магнеплюмбита), а также описаны их особенности.
5. Подробно описаны . Решена задача по расчету
исходной смеси и корректировку ее состава по методу растворной химии.
Список источников
1. Нашельский, А.Я.
Производство полупроводниковых материалов/ А.Я. Нашельский. - М.: Металлургия,
1989. - 272с.
. Арзамасов, Б.Н.
Материаловедение/ Б.Н. Арзамасов. - М.: Машиностроение, 1986. - 384с.
. Нагаенко, А.В. Изучение
методов получения нанопорошков системы ЦТС/ А.В. Нагаенко. - Ростов-н/Д.: ЮФУ,
2009. - 40с.
. Журавлев, Г.И. Химия и
технология ферритов/ Г.И. Журавлев. - Л.: Химия, 1970. - 192с.
. Смит,
Я.
Ферриты/
Я.Смит.
-
М.: Philips
Technical Library, 1959. -
504с.
6. Прилипко, Ю.С.
Функциональная керамика. Оптимизация технологии/ Ю.С. Прилипко. - Донецк: Норд
Пресс, 2009. - 368с. . Матусевич, Л.Н.
Закономерности кристаллизации из растворов/ Л.Н. Матусевич. - М.: Химия,
1986.-304с.
. Левин, Б.Е. Физико-химические
основы получения, свойства и применение ферритов/ Б.Е. Левин. - М.:
Металлургия, 1979.-471с.
. Шольц, Н.Н. Ферриты для
радиочастот/ Н.Н. Шольц. - М.Л.: Энергия, 1966,-258с.
. Окадзаки, К.Т. Технология
керамических диэлектриков/ К.Т. Окадзаки. - М.: Энергия, 1976.-336с.
. Третьяков, Ю.Д. Точечные
дефекты и свойства неорганических материалов/ Ю.Д. Третьяков. - М.:Знание,
1974.-64с.
. Епифанов, Г.И. Физика
твердого тела/ Г.И. Епифанов/ Г.И. Епифанов. - М.: Высшая школа, 1978.-200с.
![]()
![]() , 10-3Электромагнитные
параметры
, 10-3Электромагнитные
параметры
![]()
![]() ГцB100mах Т
ГцB100mах Т![]()
![]() н
н
![]()
![]() - фазовых диаграмм на примере
марганец-цинковых ферритов
- фазовых диаграмм на примере
марганец-цинковых ферритов
![]()
![]() MnЗ+
MnЗ+
![]()
![]() 1), наблюдается аномальное изменение
хода зависимостей, что связывают с равновесием:
1), наблюдается аномальное изменение
хода зависимостей, что связывают с равновесием:
![]()
![]() Mn3++Fe3+
Mn3++Fe3+
![]()
![]() =0 даже при весьма малых
давлениях кислорода невозможно. Видно также, что величина
=0 даже при весьма малых
давлениях кислорода невозможно. Видно также, что величина ![]()
![]() при х
при х![]()
![]() 1 весьма существенно
зависит от изменения давления кислорода. Следовательно, для получения
качественных изделий необходима стабильность режима охлаждения марганцевых
ферритов. Полностью избежать перевода Мn2+
в Мn3+, очевидно, не удастся даже при полном отсутствии кислорода в
системе, так как возможно образование Мn3+
по схеме
1 весьма существенно
зависит от изменения давления кислорода. Следовательно, для получения
качественных изделий необходима стабильность режима охлаждения марганцевых
ферритов. Полностью избежать перевода Мn2+
в Мn3+, очевидно, не удастся даже при полном отсутствии кислорода в
системе, так как возможно образование Мn3+
по схеме
![]()
![]() Mn3++Fe3+
Mn3++Fe3+
![]()
![]() 0,5.
0,5.
![]()
![]() = f(х);
= f(х);
![]()
![]() о = f(x); б) tспек = 13700С’
о = f(x); б) tспек = 13700С’
![]()
![]() = f(x); a = f(x)
= f(x); a = f(x) ![]()
![]() =f(x)
=f(x)
![]()
![]() 0,95=212,0400
0,95=212,0400
![]()
![]() 0,05=5,1810
0,05=5,1810
![]()
![]() 0,52=64,0744
0,52=64,0744
![]()
![]() 0,48=38,352
0,48=38,352
![]()
![]() 319,6474
319,6474
![]()
![]() 0,02=6,3929
0,02=6,3929
![]()
![]() 0,018=5,8687
0,018=5,8687
![]()
![]() 331,909
331,909
![]()
![]() (PbO)
(PbO)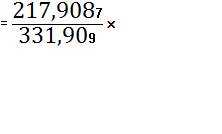
![]() 100%=65,6531%
100%=65,6531%
![]()
![]() (SrO)
(SrO)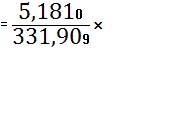
![]() 100%=1,5610%
100%=1,5610%
![]()
![]() (ZrO2)
(ZrO2)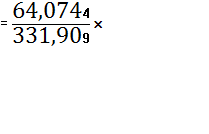
![]() 100%=19,3048%
100%=19,3048%
![]()
![]() (TiO2)
(TiO2)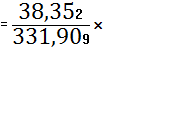
![]() 100%=11,5550%
100%=11,5550%
![]()
![]() (Nb2O5)
(Nb2O5)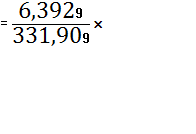
![]() 100%=1,9261%
100%=1,9261%
![]()
![]()
![]()
![]() 0,4103 (кг)
0,4103 (кг)
![]()
![]() 0,0098 (кг)
0,0098 (кг)
![]()
![]() 0,1519 (кг)
0,1519 (кг)
![]()
![]() 0,0722 (кг)
0,0722 (кг)
![]()
![]() 0,0058(кг)
0,0058(кг)
![]()
![]() 82,6574%
82,6574%
![]()
![]() 65,6531=17,0043%
65,6531=17,0043%
![]()
![]() 1,9653%
1,9653%
![]()
![]() 14,5478%
14,5478%
![]()
![]() 2,4250%
2,4250%
![]()
![]() 0,1188 (кг)
0,1188 (кг)
![]()
![]() =0,4103+0,1188=0,5291 (кг)
=0,4103+0,1188=0,5291 (кг)
![]()
![]() 0,0123 (кг)
0,0123 (кг)
![]()
![]() =0,0098+0,0123=0,0221 (кг)
=0,0098+0,0123=0,0221 (кг)
![]()
![]() 0,0909 (кг)
0,0909 (кг)
![]()
![]() 2=0,0722+0,0909=0,1631
(кг)
2=0,0722+0,0909=0,1631
(кг)
![]()
![]() 0,0152 (кг)
0,0152 (кг)
![]()
![]() 2O5=0,0058+0,0152=0,021
(кг)
2O5=0,0058+0,0152=0,021
(кг)
![]()
![]() -Т фазовые диаграммы Mn-Zn-ферритов и
рассмотрены правила их построения, структура и правила пользования ими.
-Т фазовые диаграммы Mn-Zn-ферритов и
рассмотрены правила их построения, структура и правила пользования ими.