Материал: Оптимизация керамической технологии
Оптимизация керамической технологии
Содержание
Введение
. Способы выращивания монокристаллов
.1 Выращивание из раствора в расплаве
.2 Метод Врейнеля
.3 Метод Бриджмена
.4 Метод Чохральского
.5 Метод зонной плавки
.6 Гидротермальное выращивание
.7 Способ выращивания монокристаллов из паровой фазы
. Кристаллизация и рекристаллизация твердых тел
.1 Кристаллизация
.2 Рекристаллизация
. Сущность метода совместного осаждения
. Ферриты, как фазы переменного состава
.1 Структура ферритов
.2 Дефектность ферритов
.3 Нестехиометрия ферритов
5. Особенности
строения P![]()
![]() -Т - фазовых диаграмм на примере
марганец-цинковых ферритов
-Т - фазовых диаграмм на примере
марганец-цинковых ферритов
. Задача
Выводы
Список источников
Введение
Перспективность керамики, как материала будущего, объясняется не только доступностью сырья и низкими затратами на производства, но, также, ее многофункциональностью, безопасностью в эксплуатации и экологическими преимуществами производства.
В применении керамических материалов перспективными являются:
разработка пластичной керамики на основе чистых тугоплавких оксидов металлов; для создания бронепокрытий, защитных покрытий ракет и других летательных аппаратов, которые обеспечивают защиту от коррозии в экстремальных условиях и от радиолокационного обнаружения;
использование графитопластов в химической промышленности для изготовления теплообменной и иной аппаратуры, работающей в агрессивных средах;
применение корундовой керамики с высокой, по сравнению с другими видами, теплопроводностью в ядерной технике;
создание специальных видов керамики, таких как материалы на основе ферритов, используемых в технике высоких энергий, пьезокерамические изделия для радиотехники, акустики и вычислительной техники, керамические твердые электролиты с различной проводимостью.
Возможности оптимизации керамической технологии связаны с увеличением однородности, дисперсности шихты, с ростом активности готового материала за счет интенсификации предшествующих стадий технологического процесса и создания необходимой поверхности для повышения скорости гетерофазных процессов при последующем спекании. Рассмотрение указанных вопросов является важной и актуальной задачей технологии сегнетоэлектрических материалов.
Пьезокерамические элементы находят применение в телефонах, микрофонах, звукоснимателях, ультразвуковых устройствах, сейсмоприёмниках, системах зажигания двигателей внутреннего сгорания, высоковольтных трансформаторах, управляющих реле, аппаратах медицинской диагностики и многих других устройствах.
Поэтому развитие и совершенствование
всех отраслей промышленности силикатных материалов имеет первостепенное
значение.
1. Способы выращивания монокристаллов
.1 Выращивание из раствора в расплаве
(спонтанная кристаллизация)
В качестве легкоплавких флюсов используют обычно
PbO, PbF2, B2O3, Bi2O3,
V2O5 и др. Кристаллизация происходит при охлаждении ниже
точки насыщения. Основными достоинствами метода является то, что кристаллизацию
можно проводить значительно ниже температуры плавления получаемого материала.
Недостатки: загрязнение элементами флюса, необходимость в очень точном
регулировании температуры, использование дорогостоящих платиновых материалов
тиглей [1].
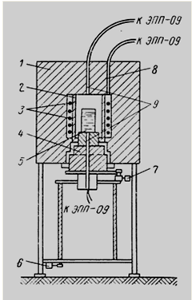
Рис. 1.1. Принципиальная схема установки для выращивания кристаллов из расплава в растворе.
- кристаллизационная печь,2 циллиндрический карборундовый экран, 3 - нагревательные силитовые стержни, 4 - под печи, 5 - тигель,
-устройство для вертикального перемещения,
- устройство для реверсивного вращения,
- термопара-датчик, 9-контрольные термопары
К флюсам предъявляются следующие требования: они не должны быть летучими и токсичными, по возможности минимально входить в состав монокристаллов (если не являются их компонентами), должна быть умеренная вязкость расплавов [1].
Например, для выращивания кристаллов феррограната (ЖИГ) берут шихту, содержащую в мольн. %: 10 Y2O3, 20,4 Fe2O3, 36,8 PbO 27,1 PbF2, 5,5 B2O3. Состав кристаллизующегося целевого продукта Y3Fe5O12 не соответствует по соотношению концентрации основных компонентов составу расплава, как и в случае кристаллизации ферритовых кристаллов из раствора, который был рассмотрен нами выше. Процессы роста монокристаллов при реализации их технологии подчиняются, собственно говоря, тем же основным термодинамическим и кинетическим закономерностям, что и синтез порошковых и пленочных материалов. Так важнейшим фактором является высокотемпературная фазовая диаграмма компонентов шихты в области ликвидуса и солидуса. Рост кристаллов протекает через возникновение зародышей, которые могут в зависимости от температуры и химических потенциалов компонентов растворяться или расти далее, т.е. могут обладать критическими размерами и т.д. [1].
По данному варианту температура выдержки
расплава 1250-1300оС (15 часов), скорость охлаждения после этого до
кристаллизации 0,3-0,5 град/час. Кристаллизацию прекращают при 950-1000оС
и удаляют оставшийся расплав, полученные кристаллы очищают кипячением в азотной
кислоте. Скорость вращения тигля при выращивании 20 об/мин, вращение
осуществляют 15 с в одну сторону и 15 с в другую с 5-секундной паузой[1].
.2 Метод Вернейля
Метод Вернейля реализуется путем просыпки
маленьких порций порошковой шихты в трубчатую печь, где эта шихта расплавляется
во время падения в кислородно-водородном пламени и питает каплю расплава на
поверхности затравки. Затравка при этом вытягивается постепенно вниз, а капля
пребывает на одном и том же уровне по высоте печи. Преимущества данного метода:
отсутствие флюсов и дорогостоящих материалов тиглей; отсутствие необходимости
точного контроля температуры; возможность контроля за ростом монокристалла.
Недостатки: из-за высокой температуры роста кристаллы имеют внутренние
напряжения; стехиометрия состава может нарушаться вследствие восстановления
компонентов водородом и испарения летучих веществ. Скорость выращивания -
несколько мм/час[1].
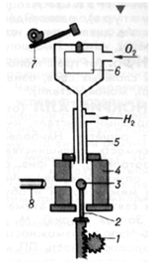
Рис .1.2. Схема установки для выращивания монокристаллов по методу Вернейля
- механизм опускания кристалла,
- кристаллодержатель,
-растущий кристалл,4 - муфель, 5 - горелка,
- бункер, 7 - механизм встряхивания, 8 -катетометр.
1.3 Метод
Бриджмена
Метод Бриджмена - зарождающиеся в нижней части
тигля с расплавом монокристаллы служат затравкой. Тигель опускается в более
холодную зону печи. Нижняя часть тигля - коническая. Скорость выращивания -
также несколько мм/час[1].
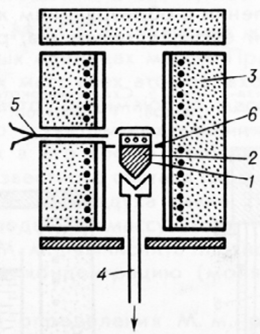
Рис.1.3. Схема установки для выращивания монокристаллов по методу Стокаберга-Бриджмена
- тигель с расплавом, 2 - кристалл,
- печь, 4 - холодильник,
- термопара, 6 - тигель с экраном
.4 Метод Чохральского
По методу Чохральского производят вытягивание
вверх на затравку монокристалла из ванны с расплавом. Нагрев обычно
осуществляют при помощи СВЧ излучения. Для снятия возникающих напряжений
используют дополнительную печь, через которую проходит выращиваемый кристалл и отжигается
[1].
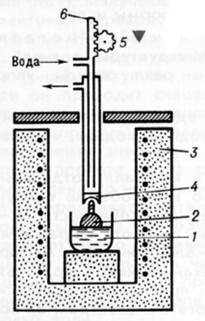
Рис. 1.4. Схема установки для выращивания монокристаллов по методу Чохральского
- тигель с расплавом, 2 - кристалл,
- печь, 4 - холодильник,
,6 - механизм вытягивания.
.5 Метод зонной плавки
Зонная плавка заключается в прогонке зоны
расплава по длине заготовки монокристалла, одновременно в зоне расплава
концентрируются примеси и происходит очистка кристалла, конечную часть которого
затем удаляют. Нагрев осуществляется индукционным, радиационно-оптическим или
другим методом. Скорость выращивания по методам 4 и 5 близка к таковой для 2 и
3 методов. При реализации трех последних способов необходимо регулирование
газовой среды выращивания[1].
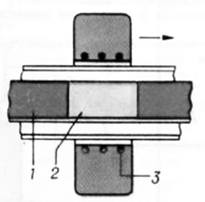
Рис. 1.5. Схема устройства для зонной плавки
.6 Гидротермальное выращивание
Исходные оксиды или готовый сложный оксид
растворяют в водных растворах кислот или щелочей для реализации
гидротермального метода. Выращивание проводят в автоклавах с защитными
коррозионно-стойкими вкладышами, например, для ферритов при 375-725оС и
давлении 1800-2000 атм. Из-за разницы температур в верхней и нижней зонах
автоклава вверху выделяется кристалл. Скорость выращивания - от долей мм до
нескольких мм в сутки. Выращиваемые монокристаллы обычно имеют высокое качество
и характерную кристаллографическую огранку, т.к. растут в условиях более или
менее близких к равновесным [1].
.7 Способ выращивания монокристаллов из паровой
фазы
Что выращивание крупных монокристаллов (весом в
десятки или сотни граммов) из паровой фазы не может иметь практического
использования ввиду малых скоростей роста, присущих этому методу. Поэтому
процессы роста из паровой фазы считаются применимыми лишь для выращивания
эпитаксиальных пленок и в отдельных случаях для получения, например, небольших
пластинчатых монокристаллов самых различных веществ. Высокопроизводительные
методы выращивания монокристаллов из расплавов, как правило, не могут
обеспечить необходимой высокой однородности свойств при получении
диссоциирующих соединений с высокими температурами плавления, а также твердых
растворов двух полупроводников все более широко используют различные методы
выращивания из паровой фазы [1].
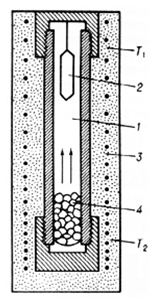
Рис. 1.6. Схема автоклава для гидротермального синтеза
- раствор, 2 - криcталл, 3 - печь, 4 - вещество
для кристаллизации (T1<T2).
Однако не следует думать, что метод выращивания из паровой фазы автоматически устраняет все причины неоднородности кристаллов. Процессы выращивания монокристаллов из паровой фазы являются не менее чувствительными к колебаниям внешних условий и состава питающей фазы, чем методы выращивания из расплавов. Но влияние этих колебаний может быть значительно сглажено, благодаря малым скоростям роста, которые способствую! приближению к равновесию между наращиваемыми слоями кристалла и паровой фазой. Все методы выращивания монокристаллов из паровой фазы (в виде пленок или объемных кристаллов) можно разделить на три большие группы, отличающиеся методом доставки атомов от источника к растущему кристаллу.
Состав растущего кристалла практически идентичен составу источника, а паровая фаза состоит только из атомов или молекул, образующих источник и кристалл; процесс состоит из возгонки или испарения с последующей конденсацией паров [1].
Источник состоит из газообразных молекул сложного состава, содержащих атомы кристаллизующегося вещества. Кристалл заданного состава образуется в результате химической реакции, происходящей на его поверхности (или вблизи нее) и приводящей к выделению атомов кристаллизующегося вещества: методы диссоциации или восстановления газообразных химических соединений [1].
Состав паровой фазы отличен от состава кристалла
и состава источника; паровая фаза состоит из молекул, образованных атомами
вещества источника и атомами посторонних химических элементов, не входящих в
состав кристалла. Выделение атомов кристаллизующегося вещества происходит в
результате реакции диспропорционирования или диссоциации газообразных молекул:
метод реакций переноса (газотранспортных реакций). [1]
2. Кристаллизация и рекристаллизация твёрдых тел
.1 Кристаллизация
Для осуществления процесса кристаллизации в растворе необходимо создать пересыщение. По способам его создания различают два основных метода кристаллизации: 1) охлаждение горячих насыщенных растворов (изогидрическая кристаллизация) и 2) удаление части растворителя путем выпаривания (изотермическая кристаллизация) [8].
Растворимость большинства веществ уменьшается с понижением температуры. Поэтому при охлаждении горячих растворов возникает пересыщение, обусловливающее выделение кристаллов. Этот метод получил название изогидрической кристаллизации, поскольку при его осуществлении количество растворителя (например, воды) остается постоянным [8].
На диаграмме растворимости
охлаждение горячего ненасыщенного раствора, имеющего температуру ti и концентрацию С)
(точка А), до конечной температуры tz условно можно изобразить линией АС, которая пересекает кривую
растворимости в точке В, характеризующей насыщенное состояние раствора при
температуре t'1. Если кристаллизация раствора начинается только после его
охлаждения до температуры t2, при которой и
заканчивается полное снятие пересыщения, то процесс кристаллизации изобразится
линией CD, а конечное состояние раствора - точкой D на кривой растворимости,
соответствующей равновесной концентрации С2 [8].
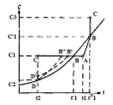
Рис. 2.1. Диаграмма растворимости
В том случае, если раствор не способен к образованию сколько-нибудь заметного пересыщения, процесс его охлаждения и кристаллизации изобразится линией ABD. В зависимости от скорости охлаждения раствора и его способности образовывать пересыщение реальный процесс может протекать также по линиям AB'D'D или AB''D[8].
Изотермическая кристаллизация заключается в том,
что вещества кристаллизуются при неизменной температуре. Между жидкой фазой и
газообразной устанавливается равновесие при данной температуре. Если уменьшить
концентрацию паров над раствором, то растворитель будет испаряться, при этом
концентрация раствора увеличивается и растворенное вещество кристаллизуется.
Такого вида кристаллизация может происходить под вакуумом, в эксикаторах над
водоотнимающими веществами. Изотермическую кристаллизацию проводят в
установках, позволяющих упаривать растворы. В частности, в лабораторном
кристаллизаторе Чернова - Ковзуна[8].
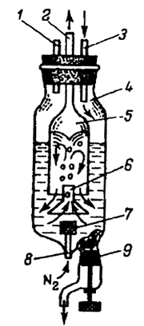
Рис. 2.2. Кристаллизатор Чернова-Ковзуна
Растворитель многократно испаряется и конденсируется. Кристаллизация вещества в этой установке происходит следующим образом. В стеклянную колонку 7 помещают стеклянный перфорированный стакан 8 с веществом, требующим перекристаллизации, а в стеклянную колонку 3 заливают растворитель до середины расширенной части при открытом кране 6, соединяющем две колонки. Растворитель должен заполнить две колонки до одного уровня. Пар кипящего растворителя конденсируется на стенках холодильника и стекает в стакан с веществом, растворяя его [8].
Раствор перетекает в колонку испарения и подвергается там кристаллизации. После того как почти все вещество перейдет из колонки 7 на фильтр 5, весь раствор спускают и снимают с колонки 3 нижнюю часть с фильтром и кристаллами [8].
При добавлении к раствору вещества, понижающего растворимость выделяемой соли, можно вызвать пересыщение раствора и кристаллизацию. Подобный метод кристаллизации получил название высаливания [8].
Вещества, добавляемые в раствор, обычно имеют одинаковый ион с кристаллизуемой солью. Характерными примерами процессов высаливания являются: кристаллизация железного купороса из травильных растворов при добавлении в них концентрированной серной кислоты; высаливание NaCl из рассолов за счет введения в них хлористого магния или хлористого кальция; получение безводного сульфата натрия добавлением к его растворам NaCl; высаливание поваренной солью хлористого бария из гидросульфидных щелоков и др. [8]
Высаливающее вещество лучше вводить в раствор в виде насыщенного раствора, так как при добавлении твердого высаливателя на нем может осаждаться кристаллизующаяся соль, что вызовет замедление или даже прекращение растворения осадителя [8].
Введение органических растворителей в водные растворы неорганических солей увеличивает эффективность процесса кристаллизации, обеспечивая высокую степень извлечения соли из раствора и возможность получения продукта в чистом виде. Недостатком этого способа является сравнительно высокая стоимость органических растворителей, регенерация которых требует проведения дополнительных операций (например, ректификации и дистилляции) и связана с некоторой потерей реагента [8].