Материал: Оптимизация керамической технологии
Выделение кристаллической фазы из раствора можно осуществить за счет пересыщения, возникающего в результате химических реакций. Такой химический метод кристаллизации используется в аналитической практике, а также в ряде химических производств.
В производстве кальцинированной соды
промежуточный продукт (бикарбонат натрия NaHCО3) также
получают вследствие химической реакции, протекающей при абсорбции
аммиачносоляным раствором двуокиси углерода. Эта реакция может быть выражена
суммарным уравнением:[8]
NaCl + NH3 + СО2 + Н2О
-> NaHCО3 + NH4Cl
В образующемся растворе наименее растворимой солью является бикарбонат натрия, который выпадает в виде кристаллического осадка и служит для получения кальцинированной соды [8].
Другими способами получения
кристаллических продуктов в результате химических реакций являются:
кристаллизация хлористого аммония при нейтрализации газообразным аммиаком
водных растворов NH4C1, насыщенных хлористым водородом; осаждение мелкокристаллического
сульфата бария при обработке растворов солей бария (например, ВаС12)
серной кислотой или сернокислыми солями (например, Na2SО4); кристаллизация
нитрата бария при сливании насыщенных растворов хлористого бария и
азотнокислого аммония и др. [8]
2.2 Рекристаллизация
Рекристаллизацией называют зарождение и рост новых зерен с меньшим количеством дефектов строения; в результате рекристаллизации образуются совершенно новые, чаще всего равноосные кристаллы [2].
Зарождение новых зерен при рекристаллизации происходит в участках с наибольшей плотностью дислокаций, обычно на границах деформированных зерен. Чем выше степень пластической деформации, тем больше возникает центров рекристаллизации. Они представляют собой субмикроскопические области с минимальным количеством точечных и линейных дефектов строения. Эти области возникают путем перераспределения и частичного уничтожения дислокаций; при этом между центром рекристаллизации и деформированной основой появляется высокоугловая границах [2].
С течением времени образовавшиеся центры новых зерен увеличиваются в размерах вследствие перехода атомов от деформированного окружения к более совершенной решетке; при этом большеугловые границы новых зерен перемещаются в глубь наклепанного металла [2].
Рассмотренная стадия рекристаллизации называется первичной рекристаллизацией или рекристаллизацией обработки [2].
По завершении первичной рекристаллизации происходит рост образовавшихся зерен при увеличении выдержки или температуры; эта стадия рекристаллизации называется собирательной рекристаллизацией. Этот процесс самопроизвольно развивается при достаточно высоких температурах в связи с тем, что укрупнение зерен приводит к уменьшению свободной энергии металла из-за уменьшения поверхностной энергии (чем крупнее кристаллы, тем меньше суммарная поверхность границ) [13].
Рост зерен происходит в результате перехода атомов от одного зерна к соседнему через границу раздела; одни зерна при этом постепенно уменьшаются в размерах и затем исчезают, а Другие становятся более крупными, поглощая соседние зерна. С повышением температуры рост зерен ускоряется. Чем выше температура нагрева, тем более крупными окажутся рекристаллизованные зерна [13].
Первичная рекристаллизация полностью
снимает наклеп, созданный при пластической деформации; металл приобретает
равновесную структуру с минимальным количеством дефектов кристаллического
строения. Свойства металла после рекристаллизации близки к свойствам
отожженного металла. [13]
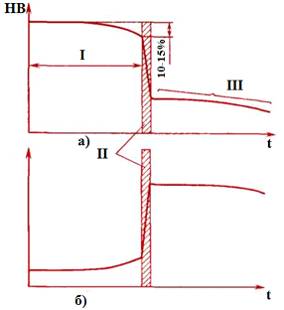
Рис. 2.3.
Схемы изменения твердости (а) и пластичности (б) наклепанного металла при
нагреве
3. Сущность метода совместного осаждения
Совместное осаждение - переход в осадок примесей
(микрокомпонентов), сопутствующий осаждению основного вещества
(макрокомпонента) из раствора, расплава или пара, содержащих несколько веществ.
Совместное осаждение происходит тогда, когда раствор (пар) пересыщен в
отношении вещества, образующего осадок, или расплав переохлажден. Совместное
осаждение начинается лишь по истечении определенного периода; длительность его
можно менять от микросекунд до десятков часов, изменяя исходное пересыщение
(переохлаждение), интенсивность перемешивания, чистоту и температуру среды, из
которой выделяется осадок. Совместное осаждение протекает в две стадии: оно
начинается с захвата примеси в ходе роста частиц осадка при его выделении и
завершается его перераспределением её между осадком и средой. Принципиальная
технологическая схема синтеза при использовании метода совместного осаждения
представлена на Рис. 3.1.[3].
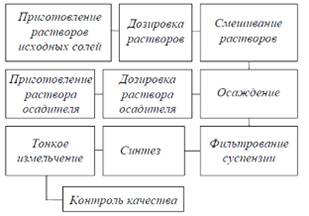
Рис. 3.1. Принципиальная технологическая схема
синтеза при использовании метода совместного осаждения.
Стремление обеспечить максимальную гомогенность синтезируемого материала привело к интенсивным работам по химическим методам синтеза. При этих методах из растворов солей выделяют твердую фазу с однородным распределением компонентов[3].
В химических методах синтеза систем типа ЦТС используют:) Водные растворы нитратов металлов;) Смеси водных растворов Pb(NO3)2 и хлоридов Ti и Zr;) Растворы алкогулянтов металлов в безводных органических растворителях.
При осаждении в качестве осадителя используют растворы аммиака (NH4OH) или бикарбоната аммония (NH4HCO3) в которые добавляют растворы солей. Полнота осаждения достигается введением избытка осадителя и поддержания кислотности среды pH>8. Схема промышленной установки для получения материалов по технологии совместного осаждения представлена на рис. 3.2.
Что метод совместного осаждения довольно просто может быть осуществлен при любом сочетании компонентов, образующих труднорастворимые соединения, но он не может быть применен в том случае, когда в состав материала должен входить компонент, который не образует малорастворимых соединений, или такие соединения растворяются в избытке осадителя [11].
Порошки, полученные описанным методом подвергают
обжигу, при котором происходит термическое разложение (с целью удаления летучих
компонентов) и синтез соответствующих(с целью удаления летучих компонентов) и
синтез соответствующих материалов.[11]
4. Ферриты, как фазы переменного состава
4.1 Структура ферритов
Известно несколько типов структур, которые при наличии в них парамагнитных ионов группы железа и других переходных элементов обладают ферримагнитными свойствами. К таким структурам относятся структуры типа: шпинели, магнетоплюмбита (гексагональные ферриты), граната, перовскита (ортоферриты) [4].
Ферриты первых трех типов структур применяют на практике, их строение и свойства относительно хорошо изучены, а природа их магнетизма укладывается в представления, развитые Неелем. Ферриты со структурой типа перовскита практического применения пока не нашли, неясен также механизм возникновения у них магнетизма [4].
Ферриты - ионные соединения, в которых анионом является кислород. При описании кристаллических решеток ионных соединений можно исходить из принципа плотнейшей упаковки анионов, так как размеры последних, как правило, значительно больше размеров кати онов [4].
Анионы могут образовывать плотнейшую упаковку по одному из возможных типов, а катионы располагаются в пустотах, образующихся при укладке анионов [4].
Геометрически заполнить шарами пространство можно бесчисленным количеством способов, однако в реальных соединениях наиболее часто встречаются два случая.
На слой шаров А, плотно уложенных на плоскости, второй плоский слой шаров В можно наложить только одним способом, а именно: каждый шар В второго слоя положить в лунку, образуемую тремя шарами А нижнего слоя. При этом получается два плотноупакованных слоя[4].
Третий слой можно укладывать по-разному.
По первому способу укладки центры шаров первого и третьего слоев оказываются на одной прямой, перпендикулярной плоскости укладки, т. е. третий слой повторяет первый. С учетом принятых обозначений получаем чередование слоев АВА. Если, четвертый слой повторяет второй и т. д., то получается чередование слоев по типу АВАВАВ…; возникающая решетка отвечает гексагональной сингонии [4].
По второму способу укладки каждый Шар С третьего слоя оказывается в лунке, образуемой шарами второго слоя. Однако под шарами третьего слоя нет шара в первом слое. Получаемый третий слой отличается от первого и второго. Схематически этот вариант показан на рис. 4.1 б, где для наглядности шары на плоскости несколько раздвинуты. При дальнейшей поочередной повторяемости слоев А, В и С получим решетку типа АВСАВСАВС, отвечающую кубической сингонии [4].
В обоих случаях плотность заполнения пространства одинакова - 74,05%, одинаково координационное число шаров - 12, однако симметрия в расположении шаров различна, что и приводит к различию в свойствах кристаллов при прочих равных условиях [4].
Элементарная ячейка гексагональной упаковки базисной плоскостью совпадает с плоскостью плотнейшей упаковки, которая перпендикулярна оси симметрии шестого порядка. Постоянная решетки в базисной плоскости а = 2r (r- радиус шара). Высота элементарной ячейки е равна удвоенной высоте тетраэдра, образованного четырьмя шарами (рис. 4.1 а) [4].
Упаковка АВСАВС… приводит к появлению элементарной ячейки в виде гранецентрированного куба (рис. 4.1 б) Элементраная ячейка кубического типа), в котором плоскость плотноупакованных шаров совпадает с плоскостью. Шары, находящиеся в вершинах куба, одновременно являются вершинами тетраэдров, образуемых ими с тремя шарами в центрах граней куба [5].
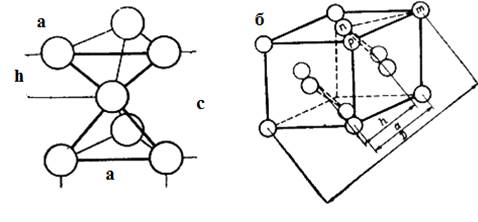
Рис 4.1. а) часть элементарной ячейки
гексагонального типа; б) элементарная ячейка кубического
типа(гранецентрированный куб)
Как указывалось, плотность заполнения шарами пространства при плотнейших упаковках составляет 74,05%, остальная часть пространства - 25,95% - остается в виде пустот между шарами[5].
В плотнейших упаковках можно выделить пустоты двух типов. Одни пустоты - тетраэдрические - образуются четырьмя шарами, расположенными в вершинах тетраэдра (рис. 4.2. а) Тетраэдрические и октаэдрические пустоты). Другие пустоты - октаэдрические - образуются восемью щарами, расположенными в вершинах октаэдра (рис. 4.2., б) [5].
Рис. 4.2. Тетраэдрические (а) и
октаэдрические (б) пустоты.
Название шпинель происходит от природного минерала - благородной шпинели MgAl2O4. При замене в указанной формуле А13+ на Fe3+ получаются феррит-шпинели [9].
Обычно формула шпинели в общем виде такова: Me Fe204 (Me - двухвалентный катион одного из следующих металлов - Со2+, Fe2+, Ni2+, Zn2+, Mg2+, Mn2+ или комбинация 0,5 ат.% Li+ + + 0,5 ат. % Fe3+ и т. д.)[9].
Кристаллическую структуру шпинели можно рассматривать с позиций теории плотнейших упаковок. Анионы О2- образуют плотную кубическую гранецентрированную упаковку, а катионы Ме2+ и Fe3+ располагаются в пустотах. В элементарную ячейку входят восемь формульных единиц MeFe204. Таким образом, 32 аниона О2- образуют плотноупакованную кубическую гранецентрированную элементарную ячейку шпинели. Узлы, занимаемые О2- обычно обозначают как 32с-узлы[9].
При плотной упаковке анионов О2- в элементарной ячейке образуется 64 тетраэдрических и 32 октаэдрических пустоты. В этих пустотах и располагаются катионы Ме2+ и Fe3+, занимающие 8 тетраэдрических пустот (обозначают 8а) и 16 октаэдрических пустот (обозначают 16d) [9].
Элементарную ячейку шпинели можно условно разбить на 8 отдельных кубиков-октантов с ребрами, равными половине параметра ячейки. При этом одинаковое расположение ионов будет наблюдаться в октантах, соприкасающихся ребрами (рис. 4.3. а) Разделение элементарной ячейки шпинели на октанты с одинаковым расположением ионов). Таким образом, можно ограничиться рассмотрением расположения ионов только в двух октантах, так как в остальных эти варианты будут повторяться [9].
Расположение ионов в двух октантах
элементарной ячейки шпинели показано на рис. 4.3. б) (Расположение ионов в
октантах ячейки шпинели) Видно, что тетраэдрические пустоты - или 8а-узлы -
находятся в четырех из восьми вершин куба и в одном октанте в центре куба; в
соседнем октанте центр куба не занят. Октаэдрические пустоты - 16й-узлы -
находятся только в том октанте, где в центре нет 8а-узла. Образование
октаэдрической пустоты для иона I происходит с участием двух ионов О2-
(пунктир), находящихся вне пределов данных октанов [9].
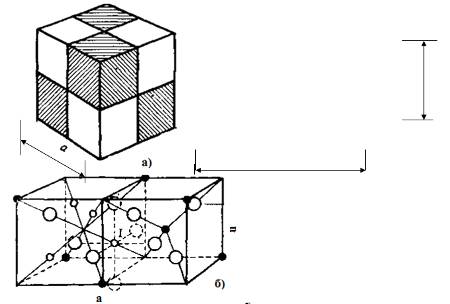
Рис. 4.3 а) Разделение элементарной ячейки
шпинели на октанты с одинаковым расположением ионов; Рис. 4.4. б) Расположение
ионов в октантах ячейки шпинели.[9]
Иногда эти ферриты называют гексагональными. Структуру природного минерала магнетоплюмбита - РЬFe7,5Mn3,5Al0,5Ti0,5О19 - имеет только один представитель гексагональных ферритов - гексаферрит бария BaFe12О19 [5].
Гексаферрит бария - первое соединение, детально исследованное и получившее широкое применение. Возможно, по этой причине название «ферриты со" структурой магнетоплюмбита» привилось и к другим соединениям, имеющим уже несколько отличную структуру[5].
В настоящее время известно много
гексагональных ферритов, а если учесть возможность изоморфных замещений в них,
то в будущем количество гексагональных ферритов увеличится. Эти ферриты имеют
следующие составы:
М-BaFe12O19 или BaО![]()
![]() 6Fe2О3
6Fe2О3
W - BaMe2Fе16О27
или ВаО ![]()
![]() 2МеО
2МеО ![]()
![]() 8Fe2О3
8Fe2О3
Y-Ba2Me2Fe12022
или 2ВаО ![]()
![]() 2МеО
2МеО ![]()
![]() 6Fe2О3
6Fe2О3
Z - Ba3Me2Fe24О41 или ЗВаО ![]()
![]() 2МеО
2МеО ![]()
![]() 12Fe2О3
12Fe2О3
Кроме перечисленных выше гексагональных соединений символом S обозначена структура шпинели, записанная в удвоенном виде - Me2Fe4О8, что сделано для удобства последующего описания гексагональных структур [5].
К гексагональным ферритам с известными допущениями можно подходить с позиций плотнейших упаковок. При этом плотнейшую упаковку образуют ионы О2- и Ва2+, имеющие примерно одинаковые размеры, а ионы Fe3+ и Ме2+ размещаются в пустотах. Все гексагональные ферриты имеют один и тот же параметр элементарной ячейки в базисной плоскости (а = 4,88 А) и весьма различные значения параметра С [5].
Для описания кристаллографических структур гексагональных ферритов удобно провести условное разделение структур по гексагональной оси на отдельные блоки. В этом случае получается, что элементарные ячейки всех гексагональных ферритов можно построить из трех видов блоков, характерных для структур М, Y и S. В структуру гексагональных ферритов входят блоки, отвечающие кубической структуре шпинели, обычно такие блоки обозначают буквой S [5].