Материал: ООИ, капельные инфекции, гноеродные кокки
-
Патогенез туляремии.
Франциселлы проникают в организм через кожу и слизистые глаз, рта, дыхательных путей, желудочно - кишечного тракта. Г.П.Руднев (1970) предложил в патогенезе туляремии выделить следующие стадии:
1. Внедрения и первичной адаптации возбудителя.
2. Лимфогенного заноса.
3. Первичных регионарно - очаговых (туляремийный бубон) и общих реакций.
4. Гематогенных матастазов и генерализации.
5. Вторичной полиочаговости.
6. Реактивно - аллергических изменений.
7. Обратного метаморфоза и выздоровления.
В ряде случаев процесс может ограничиваться первыми тремя фазами.
-
Основные клинические формы туляремии.
Основными клиническими формами туляремии являются:
-
язвенно - бубонная (ульцерогландулярная)
-
глазо - бубонная (окулогландулярная)
-
легочная
-
абдоминальная
-
генерализованная
-
другие формы (в т.ч. ангинозно - гландулярная)
-
Микробиологическая диагностика туляремии.
-
Бактериологический и биологический (материал: пунктат из бубона, гной из конъюнктивы, пленка из зева)
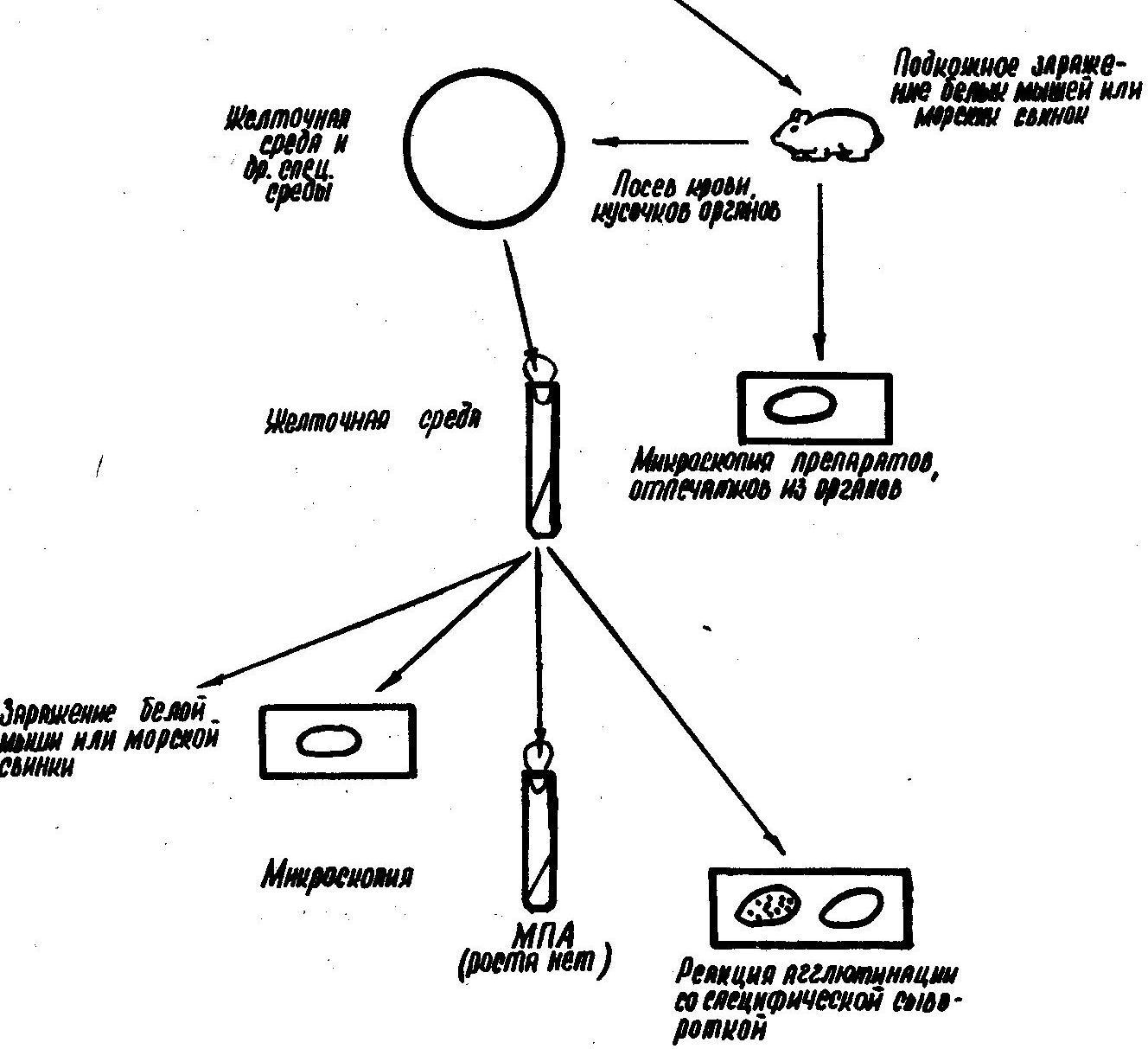
-
Серологический (Реакция агглютинации по типу реакции Райта (с 10-12 дня заболевания, диагностический титр 1:100)
-
В. Аллергический (проба с тулярином – накожная и внутрикожная
(с 5-7 дня заболевания).
-
Особенности выделения чистой культуры возбудителя туляремии.
В учебнике написано только: чистую культуру, как правило, выделяют после накопления ее в восприимчивых лабораторных животных ( мыши, морские свинки).
-
Аллергический метод диагностики туляремии.
Аллергодиагностика (проба с тулярином - туляремийным аллергеном) чаще используется для оценки естественного и вакцинального иммунитета. ГЗТ развивается на первой неделе болезни, а также после вакцинации и сохраняется несколько лет. Метод проводиться на ранних стадиях заболевания и имеют два способа введения тулярина больным: накожные и внутрикожные. Недопустимо использовать накожный тулярин для внутрикожного и наоборот, т.к. разная концентрация в-ва. Результаты учитывают в динамике через 24, 36, 48ч. За положительный результат принимают инфильтрат d 5мм. Могут применяться методы аллергодиагностики in vitro - реакция лейкоцитолиза, РТМЛ и др.
-
Специфическая профилактика туляремии.
Применяют живую туляремийную вакцину. Иммунитет длительный, проверяется с помощью пробы с тулярином. С помощью этой пробы отбирают контингенты на вакцинацию и ревакцинацию.
-
Культуральные свойства стафилококков.
Не требовательны к питательным средам, хорошо растут на обычных средах. На плотных средах колонии круглые, 2 – 4 мм в диаметре, с ровными краями, выпуклые, непрозрачные, окрашены в цвет образуемого пигмента. Рост в жидкой культуре сопровождается равномерным помутнением, со временем выпадает рыхлый осадок. При росте на обычных средах не образует капсулы, однако при посеве уколом в полужидкий агар с плазмой или сывороткой большинство штаммов S.aureus образует капсулу. Бескапсульные штаммы в полужидком агаре растут в виде компактных колоний, капсульные – образуют диффузные колонии.
На территории России выделено 7 основных ландшафтных типов природных очагов туляремии : пойменно - болотный, луго - полевой, степной, лесной, предгорно - ручьевой, тундровый и тугайный (пойменно - пустынный) со своими основными хозяевами возбудителя и эколого - эпидемиологическими особенностями. Человек очень чувствителен к туляремийному микробу, минимальная инфицирующая доза - одна микробная клетка. Животные по чувствительности к этому микроорганизму разделены на четыре группы. Особое значение в условиях Западной Сибири имеют водяные крысы и ондатры. Заражение человека может происходить путем контакта с грызунами или инфицированными ими предметами, алиментарным путем (инфицированные грызунами вода и пищевые продукты), воздушно - пылевым путем, трансмиссивно (иксодовые клещи и другие кровососы). Н.Г.Олсуфьев выделяет две экологические формы возбудителя - “сухопутную”, характеризующуюся передачей через иксодовых клещей (все три подвида), и “водную”, связанную с околоводными видами грызунов и другими организмами - гидробионтами, с преимущественной передачей через воду и укусы комаров (голарктический подвид).
-
Заболевания, которые вызывают стафилококки.
Около 120 клинических форм проявления, которые имеют местный, системный или генерализованный характер. К ним относятся гнойно-воспалительные болезни кожи и мягких тканей (фурункулы, абсцессы), поражения глаз, уха, носоглотки, урогенитального тракта, пищеварительной системы (интоксикации).
-
Межвидовые различия стафилококков.
Основные межвидовые различия у бактерий рода Staphylococcus
|
Признак |
Вид |
||
|
S. aureus |
S. epidermidis |
S. saprophyticus |
|
|
Наличие: плазмокоагулазы |
+ |
– |
– |
|
фосфатазы |
+ |
+ |
– |
|
аргининдигидролазы |
+ |
+ |
– |
|
нитратредуктазы |
+ |
+ |
– |
|
Окисление и ферментация: маннита |
+ |
– |
+ |
|
трегалозы |
+ |
– |
+ |
|
галактозы |
+ |
+ |
– |
|
маннозы |
+ |
+ |
– |
|
рибозы |
+ |
– |
– |
|
Устойчивость к: новобиоцину |
– |
– |
+ |
|
лизостафину |
– |
+ |
+ |
-
Свойства стафилококковых энтеротоксинов.
Они характеризуются антигенной специфичностью, термостабильностью, устойчивостью к действию формалина и пищеварительных ферментов. Устойчивы при диапозоне pH от 4.5 до 10.0. Энтеротоксины низкомолекулярные белки с м.м. от 26 до 34 кД со свойствами суперантиенов
-
Как у стафилококков определяют наличие плазмокоагулазы?
Плазмокоагулазу выявляют путем внесения выделенной культуры в пробирку с цитратной плазмы кролика. Ее можно приготовить в любой лаборатории. У кролика из сердца берут 8 мл крови, вносят в пробирку с 2 мл 5% лимонно-кислого натрия и ставят в холодильник. После полной осадки форменных элементов плазму отсасывают в стерильную пробирку. Она может храниться в холодильнике 8-10 дней. Перед использованием ее разводят 1:5 (1 мл плазмы и 4 мл изотонического раствора хлорида натрия) и разливают в аглютинацийни стерильные пробирки по 0,5 мл. Полную петлю культуры стафилококков эмульгируют в плазме и помещают в термостат на 3 часа, затем оставляют при комнатной температуре на 18-20 часов. Предварительный учет свертывания плазмы проводят через 3 ч, окончательный - на второй день. Очень удобно пользоваться стандартной сухой цитратной плазмы кролика. Перед употреблением в ампулу добавляют 1 мл изотонического раствора хлорида натрия и после полного растворения ее разводят 1:5. Плазма человека малопригодна для постановки реакции плазмокоагуляции, поскольку в ней могут быть консерванты, лекарственные вещества, антитела, которые могут подавлять образование плазмокоагулаза.
Если выделена культура вызывает гемолиз, коагулирует плазму и дает положительную лецитовителазну реакцию, уже на третий день можно выдать результат на наличие S. aureus. Если культура обладает только плазмокоагулаза или только вителазну активность, для окончательного установления вида стафилококка необходимо определить дополнительные критерии патогенности: ферментацию маннита в анаэробных условиях, ДНК-азную активность, продукцию лизоцима, фосфатазы, а также определить чувствительность к новобиоцин.
-
Методы определения чувствительности к антибиотикам
а) Метод дисков. Бумажные диски, пропитанные определенными антибиотиками, помещают на газон исследуемой бактериальной культуры в чашке Петри, Посевы инкубируют в течение 16-24 часов, после чего учитывают результаты опыта по образованию зон задержки роста бактерий.
По диаметру зон задержки роста ориентировочно судят о степени чувствительности бактерий к антибиотикам . Зона задержки роста до 15 мм указывает на слабую, до 25 мм - на среднюю и свыше 25 мм - на высокую чувствительность. Более точные результаты получают при использовании метода серийных разведений.
б) Метод серийных разведений. Этот метод позволяет определить минимальную задерживающую концентрацию антибиотика для данного микроорганизма (МЗК) как на жидких, так и на плотных питательных средах.
МПБ разливают по 2 мл в серию пробирок. Готовят основной раствор антибиотика, для чего берут навеску антибиотика и растворяют в дистиллированной воде из расчета 1 мг антибиотика на мл растворителя.
Левомицетин предварительно растворяют в 96° этиловом спирте из расчета 0,25 мл спирта на 1 мг антибиотика; после полного растворения добавляют такое количество дистиллированной воды, чтобы раствор содержал в 1 мл 1 мг антибиотика.
Тетрациклин и окситетрациклин растворяют в сантинормальном растворе соляной кислоты из расчета 1 мл на 1 мг антибиотика.
Эритромицин сначала растворяют в чистом метиловом спирте из расчета 1 мл на 10 мг эритромицина. После растворения добавляют такое количество дистиллированной воды, чтобы получить раствор, содержащий в 1 мл 1 мг антибиотика.
Исходный раствор антибиотика в количестве 2 мл вносят в первую пробирку с МПБ, перемешивают и получают определенную его концентрацию.
Из первой пробирки 2 мл разведенного антибиотика переносят во вторую пробирку и после перемешивания переносят 2 мл в третью пробирку и т.д. до предпоследней, откуда 2 мл выливают. Последняя пробирка является контролем, в ней нет антибиотика и она свидетельствует о пригодности среды для роста культуры.
После разведения антибиотика во все пробирки вносят по 0,1 мл испытуемой бульонной культуры. Для этого используют 3-4-часовые или 18-часовые культуры, разведенные МПБ в 50 раз.
-
Какие экзотоксины продуцируют стафилококки?
Комплекс секретируемых экзотоксинов:
-
Мембраноповреждающие(α, β, ɤ, δ)
-
Эксфолиативные(А-термостабилен, В-термолабилен)
-
Истинный лейкоцидин-токсин избирательно действует на лейкоциты, разрушая их.
-
Экзотоксин, вызывающий синдром токсического шока
-
Ферменты защиты и агрессии стафилококков.
Факторы агрессии и защиты – плазмакоагулаза, гиалуронидаза, фибринолизин, ДНКаза, лизоцимподобный фермент, лецитиназа, фосфатаза, протеиназа и т.д.
-
Факторы патогенности стафилококков, влияющие на процесс фагоцитоза.
Факторы, угнетающие фагоцитоз – их наличие может проявляться в угнетении хемотаксиса, защите клеток от поглощения фагоцитами, в обеспечении стафилококкам возможности размножаться в фагоцитах и блокировке «окислительного взрыва». Фагоцитоз угнетают :
-капсула
-белок А
-пептидогликан
-тейхоевые кислоты
-токсины.
Кроме того, стафилококки индуцируют синтез некоторыми клетками организма (например спленоцитами) супрессоров фагоцитарной активности.
-
Как определяют гиалуронидазную активность?
Гиалуронидазную активность определяют, прибавляя к 0,5 мл бульонной культуры стафилококка 0,5 мл препарата гиалуроновой кислоты с пупочного канатика. Смесь инкубируют 30 мин при 37 ° С и 10 мин при 4 ° С. В пробирку добавляют 4 капли 15% уксусной кислоты, встряхивают и через 5 мин делают учет результатов. Отсутствие сгустка свидетельствует о наличии гиалуронидазы, наличие сгустка - о ее отсутствии. Для изготовления гиалуроновой кислоты свежую пуповину новорожденных измельчают, заливают двойным количеством дистиллированной воды. Смесь выдерживают 24 ч в холодильнике, затем нагревают и кипятят до свертывания кусочков пуповины. Полученный гиалуронат фильтруют через ватно-марлевый фильтр и проверяют на образование сгустка
-
Мембраноповреждающие токсины, разновидности, механизм действия.
Мембраноповреждающие токсины могут повреждать эритроциты (гемолизины), лейкоциты, макрофаги, тромбоциты и др. Выделяют несколько типов, отличающихся по антигенной структуре, спектру лизируемых клеток, скорости действия. мембраноповреждающие токсины — α, β, ɤ, δ. Ранее их описывали как гемолизины, некротоксины, лейкоцидины, летальные токсины, т. е. по характеру их действия: гемолиз эритроцитов, некроз при внутрикожном введении кролику, разрушение лейкоцитов, смерть кролика при внутривенном введении. Однако оказалось, что такой эффект вызывает один и тот же фактор — мембрано-повреждающий токсин. Он обладает цитолитическим действием в отношении различных типов клеток, которое проявляется следующим образом. Молекулы этого токсина сначала связываются с неизвестными пока рецепторами мембраны клетки-мишени или неспецифически абсорбируются липидами, содержащимися в мембране, а затем формируют из 7 молекул грибовидный гептамер, состоящий из 3 доменов. Домены, формирующие «шляпку» и «край», расположены на внешней поверхности мембран, а домен «ножки» служит трансмембранным каналом-порой. Через нее и происходит вход и выход небольших молекул и ионов, что ведет к набуханию и гибели клеток, имеющих ядро, и осмотическому лизису эритроцитов.
Обнаружено несколько типов мембраноповреждающих (порообразующих) токсинов. Они различаются по ряду свойств. Гемолизин α чаще обнаруживается у стафилококков, выделенных от человека, он лизирует эритроциты человека, кроликов и баранов. Летальный эффект у кроликов вызывает при внутривенном введении через 3—5 мин. Гемолизин β обнаруживают чаще у стафилококков животного происхождения, он лизирует человеческие и бараньи эритроциты (лучше при более низкой температуре). Гемолизин δ лизирует эритроциты человека и многих видов животных. Летальное действие на кролика при внутривенном введении вызывает через 16—24—48 ч. Очень часто у стафилококков обнаруживаются α и ɤ токсины одновременно.