Материал: Нормальная физиология.Ответы к экзамену

Уменьшение осмотического давления крови приводит в начале к набуханию, а затем к разрушению эритроцитов - осмотический гемолиз. Мерой осмотической резистентности эритроцитов (ОРЭ) является концентрация NaCI. Отмечают концентрацию NaCI, предшествующую началу гемолиза - min ОРЭ и концентрацию, предшествующую окончанию гемолиза - max ОРЭ. В норме min ОРЭ составляет от 0,46 до 0,48% NaCI ,а max
ОРЭ - от 0,32 до 0,34% NaCI.
Нередко определяют кислотную резистентность эритроцитов. В основе также лежит принцип разведения.
Скорость оседания эритроцитов
Если предохранить кровь от свертывания, то при ее стоянии эритроциты оседают.
Факторы, влияющие на величину скорости оседания эритроцитов (СОЭ):
1.Белки плазмы крови - при увеличении в плазме крови концентрации белков, особенно грубодисперсных, СОЭ увеличивается.
2.Количество эритроцитов - увеличение количества эритроцитов и приводит к замедлению СОЭ.
Возможно физиологическое увеличение СОЭ (при беременности, тяжелой мышечной работе)
ипатологическое - как правило при патологиях воспалительного характера.
Внорме СОЭ составляет:
умужчин - нижняя граница 4 мм/час, верхняя - 12 мм/час;
уженщин - нижняя граница - 4 мм/час, верхняя - 16 мм /час.
47. Понятие о системах групп крови…
Внастоящее время установлено, что каждая клетка человеческого организма, в том числе и эритроцит, содержит на своей поверхности набор специфических белков - Антигенов, закрепленных генетически, которые и обеспечивают еѐ видовую и индивидуальную специфичность.
Кроме антигенов существует и второй класс белков - антитела к антигенам, которые циркулируют в плазме крови и при взаимодействии с определенным антигеном, расположенным на мембране клетки, способны вызывать реакцию агглютинации, образуя т.н. агглютинационные пары.
На данный момент на поверхности эритроцита обнаружено более 300 различных антигенов, ряд из которых объединен в более чем 20 систем, по которым кровь подразделяется на определенные группы (АВО, Rh-Hr, Кел-Челлано, М, N, S, Даффи, Льюис, Диего, Лютеран и т.д.).
Т.о., принадлежность человека к той или иной группе крови по различным системам обусловлена генетически, является индивидуальной особенностью и не изменяется в течение всей жизни.
Наиболее важной и практически значимой является система АВО.
Воснову деления людей на группы крови по этой системе положено
наличие или отсутствие на поверхности эритроцитов белков-антигенов (агглютиногенов) А и В. Антигенам А и В соответствуют антитела, обозначаемые буквами греческого алфавита и , названные агглютининами. Агглютиноген А и агглютинин , агглютиноген В и агглютинин - образуют т.н. агглютинационные пары. В норме в крови у человека таких комбинаций не встречается, т.е. при отсутствии агглютиногена А в его плазме
крови находится агглютинин |
и наоборот. Исходя из этих положений и образуются 4 возможные комбинации |
||||
антигенов и антител, т.е. система АВО включает в себя 4 группы крови: |
|
|
|||
Группы крови |
|
Агглютиногены |
|
Агглютинины |
|
I (0) |
|
- |
|
и |
|
II (A) |
|
А |
|
|
|
|
|
|
|
|
|
III (B) |
|
В |
|
|
|
|
|
|
|
|
|
IV (АВ) |
|
А и В |
|
- |
|
Классификация по системе АВО:
1. I (0) группа - в эритроцитах не содержатся агглютиногены А и В, в плазме крови имеются агглютинины и .
2.II (A) группа - в эритроцитах у людей с этой группой крови имеется агглютиноген А, а в плазме крови - агглютинин .
3.III (B) группа - в эритроцитах у людей с этой группой крови имеется агглютиноген В, а в плазме крови -
агглютинин .
4. IV (АВ) группа - у людей в этой группой крови в эритроцитах имеются агглютиногены А и В, при этом в плазме крови агглютинины отсутствуют.
Агглютиногены А и В неоднородны по своей структуре, т.е. можно выделить подгрупповые факторы, например
А1, А2........, В1, В2......., и т.д.
Система АВО впервые описана в 1901 году австрийским ученым Ландштейнером. Лишь через 30 лет после этого открытия он был удостоен Нобелевской премии.
Антитела |
и |
являются врожденными. Наиболее интенсивно соответствующие агглютинины вырабатываются |
в |
возрасте 8-10 |
лет. |
||
Антитела |
и |
по своей природе являются соответственно иммуноглобулинами М и G, т.е. представляют собой |
|
крупномолекулярные белки, не способные проникать через сосудистую стенку, в частности, через фетоплацентарный барьер во время беременности, что делает невозможным развитие ситуаций, подобных Резус-конфликту, о котором речь пойдет ниже.
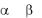
Система резус (Rh-Hr)
Эта следующая по значимости система крови была открыта в 1940 году всѐ тем же Ландштейнером совместно с Винером впервые у макак (Makakus rhezus).
Впоследствии оказалось, что и у 85% людей в эритроцитах содержится белок, названный резус-фактором (Rhфактор). Людей, на эритроцитах которых есть Rh-фактор, называют резус-положительными, а у которых он отсутствует - резус-отрицательными.
Наследуется Rh-фактор как доминантный признак, т.е. будет проявляться фенотипически и в гетерозиготном состоянии.
В настоящее время установлено, что Резус-фактор наследуется с помощью 3-х антигенов: C, D и Е, однако из них только на D-антиген вырабатываются антитела. Таким образом, резус-положительными называются люди, имеющие на поверхности своих эритроцитов D-антиген.
Существуют отдельные народы (н-р: эвены) со 100% Резус-положительным населением. Среди европеоидов 85% резус-положительных
Особенностью данной системы и отличием от системы АВО является то, что против Rh-фактора нет врожденных антител, однако они могут быть выработаны в следующих ситуациях:
1.Если Rh-положительную кровь перелить Rh-отрицательному пациенту.
2.При беременности Rh-отрицательной женщины Rh-положительным плодом.
Для иммунизации достаточно 0,25 мл Rh(+) крови. Rh-антитела, в отличие от агглютининов и , являются не полными, следовательно, их молекулярный вес позволяет им проникать через плацентарный барьер из материнского кровотока в кровоток плода, что, при достаточной концентрации антител может привести к
развитию резус-конфликта. Резус-конфликт может развиться:
1.При повторном переливании Rh-положительной крови Rh-отрицательному пациенту (очень редкая ситуация, страдает реципиент).
2.При повторной беременности Rh-отрицательной женщины Rh-положительным плодом. Эту ситуацию называют резус-конфликтом матери и плода (встречается гораздо чаще, страдает плод: варианты - от гемолитической желтухи новорожденных до внутриутробной гибели плода).
В настоящее время, чтобы избежать Резус-конфликта, таким матерям из группы риска при абортах и родах вводят концентрированные анти-D-антитела, которые агглютинируют Rh(+) эритроциты плода в кровотоке матери и не дают еѐ организму выработать собственные анти-D-антитела.
Правила переливания крови:
Если можно не переливать, то не переливать ! (т.е. по возможности переливать не цельную кровь, а
кровезаменители либо отдельные фракции или компоненты крови, в зависимости от конкретных показаний).
1.Определение групп крови донора и реципиента по системе АВО.
Методы определения групп крови:
а. Определение групп крови по стандартным сывороткам.
б. Определение групп крови по стандартным эритроцитам. в. Перекрестный метод (и по стандартным сывороткам, и по
эритроцитам).
г. Определение групп крови по моноклональным антителам (к антигенам по системе АВО).
2.Определение резус-принадлежности.
3.Проведение пробы на индивидуальную совместимость (смешивают по одной капле кровь донора и реципиента) - контроль совместимости по другим системам крови (нельзя постоянно переливать кровь от одного донора - м.б. иммунизация по другим системам крови).
4.Проведение пробы на биологическую совместимость (переливают по 10-15 мл крови и выжидают 20 минут, затем повторяют процедуру, т.к. возможно появление клиники гемотрансфузионного шока).
Клиника гемотрансфузионного шока:
1.Реакция агглютинации - агглютинаты блокируют зону микроциркуляции - ишемия тканей - боли в пояснице,
одышка, акроцианоз, рефлекторный кашель.
2. Гемолиз - значительное повышение вязкости крови, выход тканевых тромбопластинов (обломки мембран эритроцитов).
3. ДВС-синдром.
Для того, чтобы произошла агглютинация, необходимы следующие условия: 1. Наличие агглютинационной пары.
2. Достаточная концентрация агглютининов. Так, если небольшое количество крови I группы (до 500 мл) ввести в кровеносное русло человеку со II группой, то произойдет разведение агглютининов, они станут неактивными и реакция агглютинации не произойдет.
В настоящее время в плановом порядке переливается только одногруппная кровь!
Однако, в полевых условиях, при экстремальных ситуациях необходимо помнить о втором условии агглютинации. Это позволяет однократно, в объеме до 500 мл использовать для переливания кровь I группы в качестве универсальной по жизненным показаниям (см. схему совместимости групп крови) .

Таким образом, люди с I группой крови являются "универсальными донорами", а с IV - "универсальными реципиентами".
Методы переливания крови:
1.Прямое (по экстренным показаниям, через шприц с тройником и зажимом).
2.Струйное (по экстренным показаниям, донорская стабилизированная кровь).
3.Капельное (по плановым показаниям, донорская стабилизированная кровь).
48. Понятие о гемостазе… Система гемостаза - совокупность процессов, направленных, с одной стороны, на предупреждение и остановку
кровотечения, а с другой - на сохранение жидкого состояния циркулирующей крови. Задача - поддержание адекватного состояния жидкостных характеристик крови. Процессы находятся в динамическом равновесии. Нарушение его будет проявляться:
свертываемости тромбозы, ДВС-синдром. противосвертывающей активности - гемофилии, кровоточивость.
Эволюционно более сильна противосвертывающая система, т.к. физиологические функции кровь может выполнять только в жидком состоянии.
свертывание может увеличиваться лишь локально, затем образовавшийся сгусток будет удален. Однако при нарушении имеющегося равновесия возможно развитие ДВС.
Виды гемостаза:
1. Сосудисто-тромбоцитарный (в 90 % случаев повреждаются мелкие сосуды диаметром до 100 мкм).
2. Плазменный (собственно свертывание крови или гемокоагуляция, обеспечивает остановку кровотечения из более крупных сосудов).
1. Сосудистый компонент:
-спазм сосуда при травме (за счет болевой реакции; механического раздражения сосуда; действия БАВ(серотонина, адреналина).
-уменьшается просвет сосуда и за счет вворачивания интимы, при этом обнажаются волокна коллагена, что имеет важное значение для активации тромбоцитарного гемостаза.
Уже только эти компоненты значительно уменьшают кровотечение, а иногда и могут его остановить.
2. Тромбоцитарный гемостаз:
Тромбоциты
Как лекоциты выполняют в основном защитную функцию, так тромбоциты прежде всего участвуют в свертывании крови.
Тромбоциты - "кровянные пластнки", безъядерные клетки крови, имеют двояковыпуклую форму. Размер - 0,5 - 4 мкм (самые мелкие клетки крови).
Внорме в 1 мм3 крови - 200.000 - 400.000 штук тромбоцитов.
-тромбоцитоз.
-тромбоцитопения,
М.б. и при нормальном содержании тромбоцитов в крови наблюдаться патология со стороны функций тромбоцитов - при тромбоцитопатиях.
Продолжительность жизни - 8-12 дней.
Образуются в красном костном мозге из мегакариоцитов (тромбоцитопоэз).
Функции тромбоцитов:
1.Ангиотрофическая - ежедневно поглощается 35.000 тромбоцитов из 1 мм3 крови за сутки (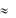 15 % всех циркулирующих тромбоцитов).
15 % всех циркулирующих тромбоцитов).
После глубокой тромбоцитопении через 30 минут 85-90% всех тромбоцитов оказывается в эндотелии. Т.о. сам эндотелий не может поглощать вещества из плазмы (тромбоциты смыкаются с эндотелием и изливают в них свое содержимое).
Исходя из этого, при тромбоцитопениях наблюдается дистрофия эндотелия (пропускает эритроциты (диапедез), петехии (синяки, точечные кровоизлияния).
2.Участие в регенерации сосудистой стенки (стимулируют размножение эндотелиальных и гладкомышечных клеток, синтез волокон коллагена).
3.Способность поддерживать спазм поврежденных сосудов (высвобождают серотонин, катехоламины,
тромбомодулин, тромбоксан).
4.Участие тромбоцитарных факторов в процессах свертывания крови и фибринолиза.
5.Адгезивно-агрегационная функция (образование первичной тромбоцитарной пробки).
1. Адгезия (прилипание активированных тромбоцитов к чужеродной поверхности). Наиболее важные стимуляторы адгезии - волокна коллагена ("+" заряженные группировки), а также кофактор адгезии - ф.
Виллебранда.
2.Агрегация - слияние тромбоцитов в однородную массу, формирование гомогенного тромбоцитарного тромба за счет переплетения псевдоподий.
3.Реакция высвобождения (дегрануляция индукторов агрегации и веществ, поддерживающих спазм сосудов
(АДФ, серотонин, тромбин, адреналин, тромбоксан А2 (мощный стимулятор агрегации и ангиоспазма)), а
также тромбоцитарных факторов свертывания (их 16, обозначаются арабскими цифрами).

4. Ретракция сгустка - (т.к. тромбоцит в псевдоподиях содержит белки, подобные актину и миозину. При взаимодействии с Са+2 - происходит сокращение, в результате чего сгусток уменьшается в объеме, уплотняется. При этом ближе стягиваются и поврежденные ткани, что способствует скорейшей регенерации тканей).
50. Противосвертывающие факторы… Противосвертывающая система обеспечивает поддержание крови в жидком состоянии.
Механизмы, обеспечивающие жидкое состояние крови:
1. В норме сосудистая стенка препятствует свертыванию крови:
-т.к. у эндотелия - контактная инертность (предотвращает активацию XII фактора);
-синтезирует простациклин, (антиагрегант и вазодилятатор);
-имеет на мембране эндотелия гликопротеин тромбомодулин, связываю щий тромбин (не свертывает кровь, но активирует антикоагулянтыпротеины С и S).
-имеет одноименный электрический заряд с форменными элементами крови;
-адсорбирует активные факторы свертывания, особенно тромбин;
2.Большая скорость течения крови;
3.Наличие антикоагулянтов.
Антикоагулянты - это вещества, препятствующие свертыванию крови. Имеющиеся в организме антикоагулянты можно разделить на две группы:
1. Предсуществующие (первичные) - антитромбин III , 2 - макроглобулин (антитромбин IV), гепарин, протеины "С" и "S".
а). Антитромбин III - обеспечивает 75% всей антикоагулянтной активности плазмы. Основной плазменный кофактор гепарина, ингибирует активность тромбина, фф. VIIa, IXa, Xa, XIIa.
б). Гепарин - сульфатированный полисахарид. Образует комплекс с антитромбином III, превращая его в антикоагулянт немедленного действия, что в 1000 раз усиливает его эффекты.
в). Протеины "С" и "S" - синтезируются в печени при участии витамина К. Протеин "С" инактивирует ф. Va, VIIIa.
Протеин "S" снижает способность тромбина активировать ф. Va, VIIIa. г). 2 - макроглобулин - 10-25% антикоагулянтной активности плазмы.
2. Образующиеся в процессе свертывания крови и фибринолиза (вторичные) антикоагулянты:
а). Нити фибрина - (антитромбин I) адсорбируют на себе до 85-90% тромбина крови. Это помогает сконцентрировать тромбин в формирующемся сгустке и предотвратить его распространение по току крови (препятствует ДВС).
б). ПДФ - продукты деградации фибрина, нарушают полимеризацию ФМ, ингибируют фибринолиз и агрегацию тромбоцитов.
Фибринолиз
Главная функция фибринолиза - реканализация (восстановление просвета) закупоренного тромбом сосуда. Основу тромба составляет фибрин. Расщепление фибрина осуществляется протеолитическим ферментом -
плазмином.
Система фибринолиза, как и система свертывания крови, имеет внутренний и внешний механизмы активации. Внутренний механизм - за счет ферментов самой крови (XIIа, калликреин).
Внешний механизм - за счет тканевых активаторов, которые вырабатываются:
-внутренними органами (почки, печень, легкие - н-р: урокиназа);
-форменными элементами крови (лейкоциты);
-микроорганизмами (золотистый стрептококк, стафиллококк - н-р: стрептокиназа).
Конечным итогом деятельности фибринолитической системы является расщепление фибрина до пептидов (ПДФ) и аминокислот. Процесс фибринолиза заканчивается в норме через 4-5 дней. Столько же длится регенерация поврежденного сосуда. Т.е. эти два процесса в ходе эволюции были синхронизированы.
51. Физиологические свойства сердечной мышцы…
Возбудимость, проводимость, сократимость, автоматия.
Автоматия - способность органа приходить в состояние возбуждения под действием импульсов, возникающих в самом органе. Автоматией обладают клетки проводящей системы сердца. Проводящая система сердца образована атипичными кардиомиоцитами, которые имеют, по сравнению с другими кардиомиоцитами,
меньше сократительных белков, митохондрий, т.е. основная функция данных клеток - не сокращение, а генера-
ция импульсов и проведение возбуждения.
Скопления атипичных кардиомиоцитов в сердце: синоатриальный узел, атриовентрикулярный узел, пучок Гиса, ножки пучка Гиса, волокна Пуркинье. Все эти образования атипичной мускулатуры обладают автоматией. Однако способность к автоматии у разных часте проводящей системы сердца различна (эксперимент с питательной средой и выращиванием культуры атипичных клеток, взятых из различных участков сердца): частота их сокращений сначала была различна (80, 40, 10, 1 импульс в минуту). Однако, по мере образования
межклеточных морфологических контактов все клетки стали сокращаться в одном ритме, причем с частотой, характерной для самых активных клеток.
Способность клеток к автоматии: синоатриальный узел - 80 в мин., атриовентрикулярный узел - 30 - 40 в мин., пучок Гиса - 10 в мин., волокна Пуркинье - 0,5-1 в мин.
Это явление уменьшения автоматии по мере удаления от синоатриального узла (от основания к верхушке)
называется убывающим градиентом автоматии.
Синоатриальный узел получил название водителя ритма(пейсмейкер) первого порядка, т.к. задает ритм
всему сердцу и угнетает автоматию других образований. Водителем ритма(пейсмейкер) 2-го порядка
называется атриовентрикулярный узел. Водитель ритма(пейсмейкер) третьего порядка и т.д.
Опыты Гаскела и Станниуса подтверждают изложенные положения.
Особенности возбуждения сердечной мышцы
1. Закон "все или ничего". Сердечная мышца при действии раздражителя либо не отвечает на возбуждение, если раздражитель слабый, либо отвечает полной силой.
В основе закона лежит особенность строения сердца - функциональный синцитий. Мышечные клетки сердца связаны между собой вставочными дисками(нексусы), в этом сходство с гладкой мускулатурой.
2.На графике потенциала действия сердечной мышцы, в отличие от скелетной, на начальном этапе фазы реполяризации регистрируется т.н. "фаза плато", обусловленная входящим током ионов Са++. Этот процесс обусловлен открытием "медленных" кальциевых каналов, продолжающих процесс деполяризации
мембраны кардиомиоцита уже после закрытия Na-евых каналов.
Наличие «фазы плато» приводит к значительному удлинению пика потенциала действия и как следствие значительное увеличение времени « фазы абсолютной рефрактерности», во время которой сердечная мышца
абсолютно невозбудима.
Фазы изменения возбудимости сердечной мышцы.
1.Абсолютная рефрактерность (0,27 сек) - полная невозбудимость.
2.Относительная рефрактерность (0,03 сек) - способность возбуждаться в ответ на сверхпороговый раздражитель. Исходя из того, что продолжительность этих двух фаз в сумме составляет 0,3 сек, можно рассчитать максимально возможную частоту сердечных сокращений (60 сек. : 0,3 сек. = 200/мин.)
3.Супернормальная возбудимость. В эту фазу возбудимость в сердце выше нормы и действие в этот момент даже слабых (подпороговых) раздражителей (рубцы, спайки, атеросклеротические бляшки) может приводить к внеочередному сокращению - экстрасистоле.
Проводимость - способность органа распространять возбуждение на невозбужденные участки.
Последовательность охвата возбуждением отделов сердца:
1.предсердия (правое, а затем и левое); 2. при прохождении возбуждения на желудочки - единственное место, содержащее возбудимые ткани - а/в узел, т.к. в остальных местах - фиброзное кольцо; 3 межжелудочковая перегородка; 4. верхушка; 5. боковые стенки желудочков; 6. основания желудочков.
Скорость проведения возбуждения: предсердие - 1 м/сек, атриовентрикулярный узел - 0,2 м/сек, пучок Гиса -
4м/сек, волокна Пуркинье - 3 м/сек, типичный миокард - 0,8 м/сек.
Следовательно, возбуждение по желудочкам распространяется не диффузно, а последовательно по проводящей системе (это объясняет синхронность сокращения типичных кардиомиоцитов в различных участках желудочков. Кроме того, имеет место задержка проведения возбуждения в атриовентрикулярном узле, что позволяет систоле предсердий опережать систолу желудочков.
Один из вариантов аритмии - экстрасистолия (внеочередное сокращение сердца). Возникает в связи с действием подпороговых по силе раздражителей (постинфарктные рубцы, атеросклеротические бляшки, очаги миокардита) в супернормальную фазу возбудимости, что и приводит к внеочередному сокращению.
В зависимости от локализации в сердце гетеротопного очага импульсации экстрасистолы подразделяются на
предсердные и желудочковые.
На ЭКГ экстрасистолу можно отличить по определенным признакам:
1.Облигатный признак - укорочение интервала RR перед экстрасистолой.
2.Факультативный признак - наличие "компенсаторной паузы" (т.е. удлинение интервала RR после экстрасистолы вследствие выпадения очередного сердечного цикла). Наблюдается в случае, если очередной импульс из синоатриального узла приходится на период абсолютной рефрактерности. При нормоили брадикардии данный признак может отсутствовать.
3.Дополнительный признак для желудочковых экстрасистол - наличие извращенного желудочкового комплекса вместо классической последовательности элементов на ЭКГ (т.к. возбуждение охватывает желудочки сердца не в обычной последовательности).
Экстрасистолы подразделяются на одиночные и групповые.
52. Сердце, его гемодинамические функции...
Сократимость сердечной мышцы.
Виды мышечных сокращений сердечной мышцы.
1. Изотонические сокращения - это такие сокращения, когда напряжение (тонус) мышц не изменяется («изо» - равные), а меняется только длина сокращения (мышечное волокно укорачивается).