Материал: Молекулярно-генетическое исследование гибридизации степного орла и орла-могильника в природных популяциях
Реагенты и материалы:
1. Пинцеты с заостренными концами
2. Лезвия
. Набор для выделения ДНК DNA Prep200 Kit (Diatome, Россия): Лизирующий реагент, 10-кратный Солевой буфер, сорбент NucleoS, элюирующий раствор ЭкстраГен.
Выделение ДНК из мезенхимной пульпы пера (Horváth, et al., 2005) проводили методом сорбции на микрочастицах на основе диоксида кремния (silica) с помощью коммерческого набора Diatome DNA Prep200 Kit по протоколу производителя с некоторыми модификациями.
Для забора мезенхимы пера использовали микрохирургические инструменты: пинцеты с заостренными концами, лезвия. Из очина пера вырезали участок, содержащий мезенхимную пульпу, в котором делали продольный разрез, чтобы облегчить доступ лизирующего реагента к крови. Вырезанный фрагмент пера помещали в стерильную микроцентрифужную пробирку объемом 1,5 мл и заливали Лизирующим реагентом (400 мкл). Образец инкубировали не менее 8 часов при температуре +4°С. Затем термостатировали образец 120 мин при температуре 65°С и центрифугировали 1 мин. при 5000g. Прозрачный супернатант переносили в чистую пробирку, куда добавляли 15 мкл суспензии сорбента NucleoS, предварительно перемешанного на вортексе.
Для связывания ДНК с микрочастицами пробирку со смесью помещали в ротатор и перемешивали 20 мин. Далее центрифугировали 10 сек при 5000g. Не задевая осадка, удаляли супернатант с помощью водоструйного насоса. К осадку добавляли 200 мкл Лизирующего реагента, тщательно перемешивали на вортексе до гомогенного состояния. Добавляли в пробирку 0,5 мл рабочего раствора Солевого буфера (предварительно 5 мл 10-кратного Солевого буфера доводили бидистиллированной водой до метки 50 мл и 96% этиловым спиртом до метки 150 мл). Центрифугировали 10 сек при 5000g. Удаляли супернатант, не задевая осадка, с помощью водоструйного насоса. Добавляли в пробирку 0,5 мл Солевого буфера, перемешивали содержимое пробирки на вортексе, центрифугировали 10 сек при 5000g и осторожно удаляли супернатант с помощью насоса. Снова добавляли Солевой буфер и повторяли процедуру отмывки.
Сушили осадок при температуре 55°С в течение 10 мин, добавляли 50 мкл
элюирующего раствора ЭкстраГен и суспендировали содержимое пробирки на вортексе
10 сек до получения гомогенной суспензии, потом термостатировали 5 мин при
65°С. Ещё раз суспендировали содержимое пробирки на вортексе и центрифугировали
2 мин при 10000 g для осаждения микрочастиц. Супернатант, содержащий выделенную
ДНК, переносили в чистую пробирку и в дальнейшем хранили при температуре -20°С.
Поскольку при выделении из линного пера концентрация и сохранность ДНК в пробе
невелики, оценку качества выделения проводили по результатам ПЦР на фрагмент
D-петли митохондриального генома (фрагмент AND2).
4.2 Разработка специфических праймеров для ПЦР
Последовательности праймеров и температуры отжига приведены в Таблице 1.
Таблица 1. Последовательности праймеров и температуры отжига.
|
Название |
Последовательность 5’-3’ |
Температура отжига (°C) |
|
AND2 (Карякин, и др., 2016) |
for: CCCCCGGGCTAAATCCATGCC rev: CCGCGATTAAGAGGCAGAA |
57 |
|
AK1-6* |
for: CAGCCTCCCCATCCCAGCAAAGA, rev: TCCCCGCGTCCACGTAGAGCAG |
65 |
|
BF7* |
for: GGTGGCAGTGCTAAGGACA, rev: TGAAGCAGCTAAGAAAAACAGT |
57 |
Подбор специфических праймеров на выбранные участки ядерного генома (*)
проводили с помощью программы PrimerSelect из программного пакета LaserGene
(DNAStar, США). Специфичность праймеров проверяли с помощью онлайн-инструмента
Primer BLAST (NCBI). Для исследования структуры D-петли митохондриального
генома степного орла и орла могильника использовали ранее разработанную
библиотеку праймеров AND (Карякин, и др., 2016).
4.3 Полимеразная цепная реакция (ПЦР)
Реактивы:
a) Набор Encyclo Plus PCR kit (Евроген, Россия): 50X смесь полимераз Encyclo, 5X Encyclo Red буфер, смесь дезоксинуклеозидтрифосфатов (10 мМ каждого), стерильная вода для ПЦР.
b) Специфические праймеры (Синтол, Россия)
Протокол:
1) Смеси для ПЦР приготовляли согласно протоколу производителя. На объём одной пробы в 20мкл использовали по 0,4мкл рабочих растворов праймеров (10пМ); 0,4мкл 50-кратных дНТФ; 4мкл 5-кратного буфера; 0,5- 1мкл матрицы; 0,4мкл 50-кратной Taq-полимеразы; оставшийся объём дополняли деионизированной водой.
2) ПЦР с «горячим стартом» и финальной элонгацией 5 мин. при 72°С
проводили на приборе VeritiFast (Applied Biosystems, США). Параметры цикла
реакции: 95°C 30 секунд (денатурация), 55-65°C 30 секунд (отжиг праймеров),
72°C 45 секунд (элонгация), 35 циклов.
4.4 Горизонтальный электрофорез
Реактивы:
1. 50-кратный ТАЕ-буфер (Tris-base 2M, EDTA 0.05M, Укс. к-та
~1.56M).
2. Агароза Biochemical grade (Helicon, Россия).
3. Бромистый этидий (Sigma, США). Протокол:
1. Приготовление 1х ТАЕ-буфера.
10мл 50х ТАЕ-буфера разбавляли дистиллированной водой до отметки
мл. Рабочий трис-ацетатный буфер: Tris-acetate 40mM, EDTA 1mM, рН=7,6.
2. Заливка агарозного геля
В 60 мл буфера ТАЕ растворяли при нагревании (в микроволновой печи) агарозу (0,6 г для 1% геля). Охлаждали полученный раствор примерно до 60°C, добавляли 1,5 мкл бромистого этидия на гель. Размешивали, заливали гель в собранную камеру для заливки (Helicon, Россия). После того, как гель застывал, переносили гель в камеру для фореза, наливали в камеру буфер ТАЕ, удаляли гребенки из геля.
3. Нанесение образцов
3 мкл ПЦР-смеси, содержащей краситель в составе 5х Red буфера, наносили в лунки геля.
4. Гель-электрофорез
Форез проводили при 120 Вольт с помощью источника тока (Эльф, ДНК- технология, Россия) 80 мА в течение получаса. Оценивали расположение образцов по положению лидирующего красителя.
5. Анализ геля проводили на приборе Gel Doc XR 170-8170 170-8171 (Bio-Rad).
6. При наличии дополнительных продуктов ПЦР на электрофоретическом
геле проводили очистку специфического продукта с помощью силика-колонок.
4.5 Очистка ПЦР-фрагментов в агарозном геле
Реагенты и материалы:
1. Набор GeneJET Gel Extraction Kit (Thermo Scientific, США)
2. Этиловый спирт 96% перегнанный
. Микрохирургические инструменты: глазной пинцет, лезвия. Протокол:
1. С помощью стерильных лезвий и пинцета вырезали из геля фрагмент, содержащий специфический продукт, помещали в предварительно взвешенную микроцентрифужную пробирку.
2. По весу геля добавляли двукратный объем Binding buffer, инкубировали при 55°С до полного растворения агарозы.
3. Переносили содержимое пробирки на колонки, центрифугировали 1 мин. при 5000 g, удаляли фильтрат.
4. На колонку наносили 100 мкл Binding buffer, повторяли центрифугирование, удаляли фильтрат.
. Центрифугировали колонку с ДНК 1 мин при 5000 g, чтобы удалить остатки спиртосодержащего буфера.
. Переносили колонку в чистую микроцентрифужную пробирку, наносили на колонку 20 мкл Elution Buffer, инкубировали 5 мин при 65С и центрифугировали 1 мин при 14000 g.
. 1 мкл элюата, содержащего очищенную ДНК, наносили на гель для
проверки качества очистки методом электрофореза (см. выше).
4.6 Секвенирование по Сэнгеру
Перед секвенированием проводили переосаждение ДНК с помощью 70% этанола и
ацетата аммония (125 мМ), центрифугировали в течение 20мин. Остатки исходного
буфера удаляли, добавляли к переосажденным и высушенным образцам по 1мкл 4
пкмоль растворов соответствующих праймеров (отдельно прямого, отдельно
обратного), проводили сиквенсовую реакцию с помощью красителя BigDye 3.1
(Applied Biosystems, США). Проводили денатурацию полученных продуктов
формамидом, после чего ставили капиллярный электрофорез в полиакриламидном
геле. Полученные результаты анализировали с помощью секвенатора ABI 3500
(Applied Biosystems, США).
4.7 Обработка результатов
Обработку результатов секвенирования проводили с помощью программ SeqMan и EditSeq программного пакета LaserGene (DNAStar, США). Полученные консенсусные последовательности выравнивали для поиска полиморфных сайтов в программном пакете Mega 5.2 (MEGA, США).
Поиск по подобию, сравнение представленной последовательности с
последовательностями в базе данных GenBank (для выбора подобных нуклеотидных
последовательностей из более чем 70,000 организмов) осуществляли с помощью Standard Nucleotide BLAST на интернет-ресурсе
https://blast.ncbi.nlm.nih.gov/Blast.cgi.
5. Результаты
5.1 Поиск маркеров
В базе данных GenBank были найдены последовательности трех широко распространенных ядерных маркеров для степного орла Aquila nipalensis и орла-могильника Aquila heliaca: 3 интрон гена лактатдегидрогеназы, 6 экзон гена аденилаткиназы и 7 интрон гена бета-фибриногена.
a. Aquila heliaca partial ldh gene for lactate dehydrogenase, intron 3
GenBank number: AJ601502.1
Aquila nipalensis partial ldh gene for lactate dehydrogenase, intron 3
GenBank number: AJ601503.1
b. Aquila heliaca partial ak1 gene for adenylate kinase 1, exon 6
GenBank number: AJ601473.1
Aquila nipalensis partial ak1 gene for adenylate kinase 1, exon 6
GenBank number: AJ601474.1
c. Aquila heliaca beta-fibrinogen gene, intron 7 and partial cds
GenBank number: AY987198.1
Aquila nipalensis beta-fibrinogen gene, intron 7 and partial cds
GenBank number: AY987199.1
В первом случае по результатам проведения анализа BLAST нуклеотидные
последовательности не имели различий и совпадали на 100%. В случае с
аденилаткиназой наблюдалось 99% идентичности, т.к. имелись несовпадение пары
нуклеотидов и двунуклеотидная вставка в последовательности у орла-могильника; в
третьем случае с бета- фибриногеном наблюдалось 98% идентичности, поскольку
имелось 2 инсерции в последовательности у могильника и несовпадение одной пары
нуклеотидов.
5.2 Подбор праймеров
К маркерам аденилаткиназы и бета-фибриногена с помощью программы Primer Select (DNAStar, США) были подобраны специфические праймеры AK1-6 и BF7.
Критериями подбора праймеров для ПЦР были: температура отжига (45- 65°С), длина праймера (17-24 bp), длина продукта (350-500 bp), отсутствие или минимальное количество вторичных структур (димеров и селф-димеров праймеров, т.н. «шпилек»), специфичность к объектам исследования.
Характеристики предложенных программой пар праймеров к фрагменту BF7
приведены на Рисунке 5.
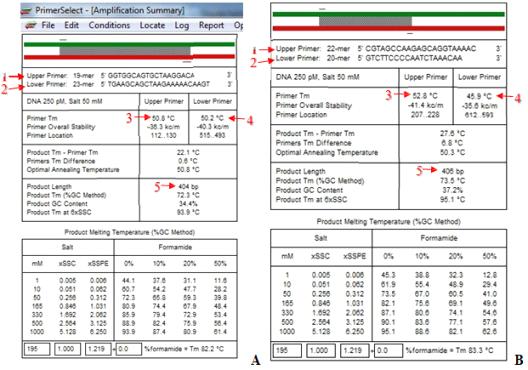
Рисунок 5. «Amplification summary» программы PrimerSelect для подобранных пар праймеров. А - BF7 var. 1, B - BF7 var. 2; 1 - последовательность прямого праймера, 2 - последовательность обратного праймера, 3 - температура отжига прямого праймера, 4 - температура отжига обратного праймера, 5 - длина продукта
Кроме того, начальная температура отжига была проверена по упрощенной
формуле по GC-составу праймеров:
Ta = (N[G]+ N[C])*4 + (N[A]+ N[T])*2 - 5
Диапазон температуры отжига лежит в пределах Ta ± 5°C
Последовательности подобранных праймеров и температуры отжига указаны в
Таблице 2.
Таблица 2. Последовательности специфических праймеров и температуры отжига
|
Название пары |
Последовательность 5’-3’ |
Расчетная температура отжига по GC-составу |
|
AK1-6 |
for: CAGCCTCCCCATCCCAGCAAAGA, rev: TCCCCGCGTCCACGTAGAGCAG |
69°C 69°C |
|
BF7 var 1 |
for: GGTGGCAGTGCTAAGGACA, rev: TGAAGCAGCTAAGAAAAACAGT |
55°C 55°C |
|
BF7 var 2 |
for: CGTAGCCAAGAGCAGGTAAAAC, rev: GTCTTCCCCAATCTAAACAA |
61°C 51°C |
Специфичность праймеров к выбранным последовательностям проверяли с помощью онлайн-поиска в Primer BLAST (NCBI, США) на возможность специфического связывания с ДНК Homo sapiens и грибов группы Ascomycota - возможных источников контаминирующей ДНК в пробах. Кроме того, проверяли специфичность связывания с ДНК близкородственных видов рода Aquila, чтобы получить максимально универсальную систему анализа последовательностей данных маркеров внутри рода.
В результате проведенного анализа пара праймеров BF7 var 2 была исключена из дальнейшего анализа из-за значительной разницы в температурах отжига и отсутствия универсальности (наличия замен на 3’- конце последовательности праймера у Aquila chrysaetos).
Результаты ПЦР для пар праймеров AK1-6 и BF7 var.1 (далее BF7) приведены
на Рисунке 6.
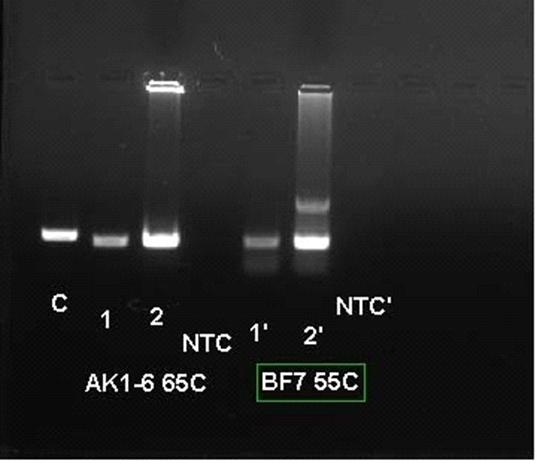
Рисунок 6. Гель-электрофорез продуктов ПЦР-реакции с праймерами AK1-6 (Ta=65°C) и BF7 (Ta=55°C). 1 - Aquila heliaca, 2 - Aquila nipalensis. С - маркерный ПЦР-фрагмент размером 493 bp: NTC - контрольная ПЦР-смесь без добавления ДНК.
Видно, что праймеры AK1-6 позволяют получить специфический продукт с
высоким выходом и без неспецифического связывания. На электрофореграммах
продуктов амплификации с праймерами BF7 присутствуют как специфический продукт,
так и продукты неспецифического связывания в виде дополнительных полос, поэтому
для секвенирования данного маркера требуется дальнейшая очистка ПЦР-продуктов в
геле.
5.3 Характеристика образцов предполагаемых гибридов
AH-K1A - перо особи, найденной в гнезде степного орла на дереве на кромке Урдинских песков в 2013 г. Птица была похожа на гибрид степного
орла и орла-могильника, предположительно являлась самкой. В гнезде находился самец орла-могильника и 1 птенец, близкий по окраске к орлу- могильнику, но с более тёмным бурым фоном кроющих верха крыла. D-петля митохондриального генома линного пера взрослой птицы из гнезда соответствовала орлу-могильнику.
АN12 - линное перо, найденное в типичном гнезде степного орла на земле в 2010г. в Даурии. Кроме того, была сфотографирована птица с нехарактерной окраской. Анализ D-петли митохондриальной ДНК показал, что гаплотип также идентичен одному из гаплотипов орла-могильника.
Кроме того, в анализ последовательности бета-фибриногена 7 интрона был
включен образец ДНК из пера, собранного с гнезда 162AN в 2008 году, для
которого не удалось получить последовательность митохондриальной ДНК по причине
отсутствия специфического связывания праймеров, подобранных для степного орла и
орла могильника и невозможности визуально определить принадлежность пера (рис.
7).

Рисунок 7. Перо образца 162AN (Даурия, 2010 г.)
5.4 Определение пола
Результаты ПЦР-анализа образцов ДНК предполагаемых гибридов с
универсальными праймерами для определения пола у птиц (Fridolfsson, Ellegren,
1999) по фрагменту гена АТФ-зависимой хеликазы CHD1, расположенном в половых
хромосомах, приведены на Рисунке 8.
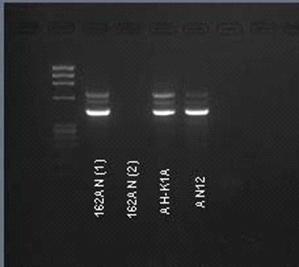
Рисунок 8. ПЦР фрагментов половых хромосом с универсальными праймерами для определения пола птиц (Fridolfsson, Ellegren, 1999). АН-К1А, AN12 - предполагаемые гибриды (самки)
На электрофореграммах образцов AH-K1A и AN12 присутствуют две полосы - размером около 450 bp и более 600 bp. Кроме того, наблюдается присутствие еще одной полосы между этими двумя полосами. Согласно оригинальной методике, полоса 400-450 bp у беркута соответствует продукту амплификации фрагмента W-хромосомы, полоса более 600 bp - продукту амплификации фрагмента Z-хромосомы. Таким образом, оба исследуемых образца принадлежат самкам. Наличие третьей полосы между фрагментами половых хромосом может быть связано с неспецифическим связыванием праймеров у степного орла и более высокой чувствительностью полимеразы по сравнению с оригинальным исследованием, проведенным для беркута.
Кроме того, для сравнения нами были проанализированы с помощью
универсальных праймеров шесть образцов ДНК птенцов филина Bubo bubo.
Результаты молекулярного определения пола приведены на Рисунке 9.
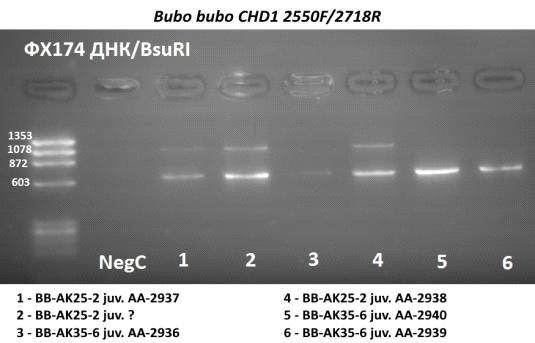
Рисунок 9. ПЦР фрагментов половых хромосом для определения пола птенцов
филина. NegC - негативный контроль, ФХ174 ДНК/BsuRI -
маркер размера молекулярных фрагментов.
У филинов ПЦР-продукты имеют другие размеры: около 1200 bp (что
соответствует продукту W-хромосомы у сов) и около 700 bp (для Z-хромосомы у
сов) соответственно.