Материал: Левкина Е.В. Конспект лекций по Физиологии человека
В плазме находится ряд белков, отличающихся по своим свойствам и функциональному значению: альбумины (около4,5%), глобулины (2-3%)и фибриноген (0,2-0,4%).
Белки плазмы крови выполняют функции регуляторов водного обмена между кровью и тканями. От количества белков зависят вязкость и буферные свойства крови; они играют важную роль в поддержании онкотического давления плазмы.
2.5 Свертывание и переливание крови
Необходимые условия жизнедеятельности организма – жидкое состояние крови и замкнутое кровеносное русло. Эти условия обеспечивает система свертывания крови (система гемокоагуляции), которая сохраняет циркулирующую кровь в жидком состоянии и предотвращает ее потерю через поврежденные сосуды за счет образования кровяных тромбов. Остановка кровотечения называется гемостазом. Однако, при больших кровопотерях и некоторых заболеваниях необходимо переливание крови. При переливании должна строго соблюдаться ее совместимость.
Наиболее распространена ферментативная теория свертывания крови, основоположником которой является профессор Дерптского (Тартуского) университета А. А. Шмидт (1872). В дальнейшем эта теория была значительно дополнена, и в настоящее время считают, что свертывание крови проходит три фазы:
1) образование протромбиназы,
2) образование тромбина,
3) образование фибрина.
Образование
протромбиназы осуществляется под
влиянием тромбопластина (тромбокиназы),
представляющего собой фосфолипиды
разрушающихся тромбоцитов, клеток
тканей и сосудов. Тромбопластин
формируется при участии ионов Са![]() и некоторых плазменных факторов
свертывания крови.
и некоторых плазменных факторов
свертывания крови.
Вторая фаза свертывания крови характеризуется превращением неактивного протромбина кровяных пластинок под влиянием протромбиназы в активный тромбин. Протромбин является глюкопротеидом и образуется клетками печени при участии витамина К.
В третьей фазе свертывания из растворимого фибриногена крови, активированного тромбином, образуется нерастворимый белок фибрин. Нити фибрина образуют основу кровяного сгустка (тромба), прекращающего дальнейшее кровотечение. Фибрин служит также структурным материалом при заживлении ран. Фибриноген это самый крупномолекулярный белок плазмы и образуется в печени.
Основоположниками учения о группах крови и возможности ее переливания от одного человека к другому были К. Ландштейнер (1901) и Я. Янский(1903). В нашей стране переливание крови впервые было проведено профессором Военно-медицинской академии В. Н.Шамовым в 1919г. В 1928г он предложил переливание трупной крови, за что он был удостоен Ленинской премии.
Я. Янский выделил четыре группы крови, встречающиеся у людей. Эта классификация не утратила своего значения и до настоящего времени. Она основана на сравнении антигенов, находящихся в эритроцитах (агглютиногенов), и антител, имеющихся в плазме (агглютининов). Выделены главные агглютиногены (А и В) и соответствующие агглютинины (альфа и бета). Агглютиноген А и агглютинин альфа, а также агглютиноген В и агглютинин бета называются одноименными. В крови человека не могут содержаться одноименные агглютинины и агглютиногены. При встрече их возникает реакция агглютинации, т. е. склеивания эритроцитов, а в дальнейшем и разрушение (гемолиз). В этом случае говорят о несовместимости крови. При переливании несовместимой группы крови у реципиента может возникнуть опасное патологическое состояние – гемотрансфузионный шок. Оно может закончиться гибелью организма.
В эритроцитах крови, отнесенной к I (0) группе, не содержится агглютиногенов, а в плазме имеются агглютинины альфа и бета. В эритроцитах II (А) группы имеется агглютиноген А, а в плазме — агглютинин бета. Для III (В) группы крови характерно наличие агглютиногена В в эритроцитах и агглютинина альфа в плазме. IV(АВ) группа крови характеризуется содержанием агглютиногенов А и В в эритроцитах и отсутствием агглютининов в плазме.
Переливание несовместимой крови вызывает гемотрансфузионный шок— тяжелое патологическое состояние, которое может закончиться гибелью человека. Людям первой (I) группы можно переливать кровь только этой группы, а также эту группу можно переливать людям всех других групп. Поэтому людей с I группой крови называют универсальными донорами. Людям IV группы можно переливать одноименную кровь, а также кровь всех остальных групп, поэтому этих людей называют универсальными реципиентами. Кровь людей II и III групп можно переливать людям с одноименной, а также с IV группой.
В переливании крови большое значение имеет совместимость по резус-фактору. Это дополнительный агглютиноген, который впервые был обнаружен в эритроцитах обезьян-макак породы «резус» в 1938 г. Впоследствии оказалось, что резус-фактор содержится в эритроцитах 85% людей и лишь у 15% людей отсутствует. Если в крови человека есть резус-фактор, она называется резус-положительной. Если же в крови человека нет резус-фактора, она называется резус-отрицательной. При повторном переливании крови реципиенту, несовместимому по резус-фактору с донором, возникают осложнения, связанные с агглютинацией несовместимых донорских эритроцитов. Это является результатом воздействия специфических антирезус-агглютининов, вырабатываемых ретикуло-эндотелиальной системой после первого переливания.
При вступлении в брак резус-положительного мужчины с резус-отрицательной женщиной плод нередко наследует резус-фактор отца. Кровь плода проникает в организм матери и вызывает образование антирезус-агглютининов, которые приводят к гемолизу эритроцитов будущего ребенка. При первой такой беременности для выраженных нарушений у первого ребенка концентрация антирезус-агглютининов бывает невысокой. Поэтому плод рождается живым, но с гемолитической желтухой. При повторной беременности (особенно, если между первым и вторым ребенком довольно большая разница во времени зачатия) в крови матери резко возрастает концентрация антирезусных веществ. Это проявляется не только гемолизом эритроцитов плода, но и внутрисосудистым свертыванием крови, что нередко приводит плод к гибели.
2.6 Регуляция системы крови
Регуляция системы крови включает в себя поддержание постоянства объема циркулирующей крови, ее морфологического состава и физико-химических свойств плазмы. В организме существует два основных механизма регуляции системы крови — нервный и гуморальный.
Высшим подкорковым центром, осуществляющим нервную регуляцию системы крови, является гипоталамус. Кора головного мозга оказывает влияние на систему крови также через гипоталамус. Эфферентные влияния гипоталамуса включают механизмы кроветворения, кровообращения и перераспределения крови, ее депонирования и разрушения. Рецепторы костного мозга, печени, селезенки, лимфатических узлов и кровеносных сосудов воспринимают происходящие здесь изменения, афферентные импульсы от этих рецепторов служат сигналом соответствующих изменений в подкорковых центрах регуляции. Гипоталамус через симпатический отдел вегетативной нервной системы стимулирует кроветворение, усиливая эритропоэз. Парасимпатические нервные влияния тормозят эритропоэз и осуществляют перераспределение лейкоцитов: уменьшение их количества в периферических сосудах и увеличение в сосудах внутренних органов. Гипоталамус принимает также участие в регуляции осмотического давления, поддержании необходимого уровня сахара в крови и других физико-химических констант плазмы крови.
Нервная система оказывает прямое и косвенное регулирующее влияние на систему крови. Прямая регуляция заключается в двусторонних связях нервной системы с органами кроветворения, кровераспределения и кроверазрушения. Афферентные и эфферентные импульсы идут в обоих направлениях и регулируют все процессы, идущие в системе крови. Косвенная регуляция осуществляется с помощью гуморальных посредников, которые влияют на рецепторы кроветворных органов и стимулируют или ослабляют процесс кроветворения.
Среди механизмов гуморальной регуляции крови особая роль принадлежит биологически активным гликопротеидам — гемопоэтинам. Они синтезируются в основном в почках, а также в печени и селезенке. Продукция эритроцитов регулируется эритропоэтинами, лейкоцитов — лейкопоэтинами и тромбоцитов — тромбопоэтинами. Эти вещества усиливают гемопоэз в костном мозге, селезенке, печени, ретикулоэндотелиальной системе. Гемопоэтины содержатся в плазме крови здоровых людей и являются физиологическими стимуляторами кроветворения.
Стимулирующее влияние на гемопоэз оказывают гормоны гипофиза (соматотропный и адренокортикотропный гормоны - АКТГ), коркового слоя надпочечников (глюкокортикоиды), мужские половые гормоны (андрогены). Женские половые гормоны (эстрогены) снижают гемопоэз. С этим связано меньшее, чем у мужчин, содержание эритроцитов, гемоглобина и тромбоцитов в крови женщин. У мальчиков и девочек (до полового созревания) различий в картине крови нет, отсутствуют они и у людей старческого возраста.
2.7 Физиология кровообращения
Кровообращение – совокупность физиологических процессов, обеспечивающих непрерывное движение крови в организме за счет деятельности сердца и сосудов. Посредством кровообращения интегрируются различные функции организма, обеспечивается его участие в реакциях на изменения окружающей среды.
2.7.1 Физиология сердца
Источником энергии, необходимой для продвижения крови по сосудам, является работа сердца. Оно представляет собой полый мышечный орган, разделенный продольной перегородкой на правую и левую половины. Каждая из них состоит из предсердия и желудочков, отделенных фиброзными перегородками. Односторонний ток крови из предсердий в желудочки, а оттуда в аорту и легочные артерии обеспечивается соответствующими створчатыми и полулунными клапанами, открытие и закрытие которых зависит от градиента давлений по обе их стороны.
Толщина
стенок различных отделов сердца
неодинакова и зависит от их функциональной
роли. У левого желудочка она равна
примерно 10-15 мм, у правого — 5-8 мм и у
предсердий — 2-3 мм. Масса сердца составляет
в среднем 250-300 г, а объем желудочков —
250-300 мл. Сердце снабжается кровью
через коронарные (венечные) артерии,
которые начинаются у места выхода аорты,
от ее восходящей части. Кровь через
венечные артерии поступает только в
период расслабления миокарда. Количество
этой крови в покое составляет примерно
200-300 мл![]() ,
а при напряженной физической работе
может достигать 1000 мл
,
а при напряженной физической работе
может достигать 1000 мл
![]() .
.
К основным свойствам сердечной мышцы относятся автоматия, возбудимость, проводимость и сократимость.
Автоматией сердца называется его способность к ритмическому сокращению без внешних раздражений под влиянием импульсов, возникающих в нем самом. Возбуждение в сердце возникает в месте впадения полых вен в правое предсердие, где находится синоатриальный, или синусопредсердный, узел (узел Киса-Флека), являющийся главным водителем ритма сердца. Далее возбуждение по предсердиям распространяется до атриовентрикулярного, или предсердножелудочкового, узла (узел Ашоффа-Тавары), расположенного в межпредсердной перегородке правого предсердия. Затем возбуждение проходит по пучку Гиса, его ножкам и волокнам Пуркинье в мускулатуру желудочков.
Автоматия сердца обусловлена изменением мембранных потенциалов в водителе ритма. Это связано со сдвигом концентрации ионов калия и натрия по обе стороны деполяризованных клеточных мембран. На характер проявления автоматии влияет содержание солей кальция в миокарде, рН внутренней среды и ее температура, некоторые гормоны (адреналин, норадреналин и ацетилхолин).
Возбудимость сердца проявляется в возникновении возбуждения при действии на него электрических, химических, термических и других раздражителей. В основе процесса возбуждения лежит появление отрицательного электрического потенциала в первоначально возбужденном участке, при этом сила раздражителя должна быть не менее его пороговой величины. Сердце или не отвечает на раздражение, или отвечает сокращением максимальной силы. Однако этот закон проявляется не всегда. Степень сокращения сердечной мышцы зависит не только от силы раздражителя, но и от величины ее предварительного растяжения, а также от температуры и состава питающей ее крови.
Возбудимость миокарда непостоянна. В начальном периоде возбуждения сердечная мышца невосприимчива (рефрактерна) к повторным раздражениям, что составляет фазу абсолютной рефрактерности. Данная фаза равна по времени систоле сердца (0,2-0,3 с).
С началом расслабления возбудимость сердца начинает восстанавливаться и наступает фаза относительной рефрактерности. Поступление в этот момент дополнительного импульса способно вызвать внеочередное сильное сокращение сердца — экстрасистолу. При этом период отдыха, следующий за экстрасистолой, длится больше времени, чем обычно, и называется компенсаторной паузой. После фазы относительной рефрактерности наступает период повышенной возбудимости. По времени он совпадает с диастолическим расслаблением и характеризуется тем, что импульсы даже небольшой силы могут вызвать сокращение сердца.
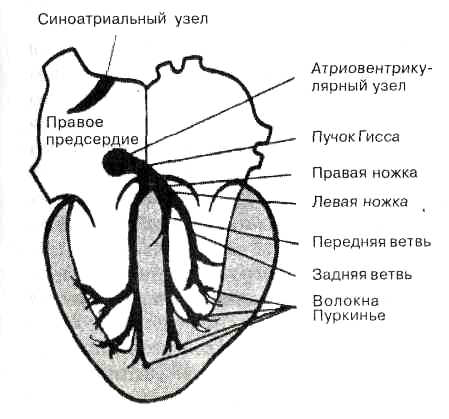
Рисунок 2.2. - Схема расположения водителя ритма (пейсмекера)
и проводящей системы на фронтальном разрезе сердца
Проводимость сердца обеспечивает распространение возбуждения от клеток водителей ритма по всему миокарду (рисунок 2.2). Проведение возбуждения по сердцу осуществляется электрическим путем. Потенциал действия, возникающий в одной мышечной клетке, является раздражителем для других. Проводимость в разных участках сердца неодинакова и зависит от структурных особенностей миокарда и проводящей системы, толщины миокарда, а также от температуры, уровня гликогена, кислорода и микроэлементов в сердечной мышце.
Сократимость сердечной мышцы обусловливает увеличение напряжения или укорочение ее мышечных волокон при возбуждении. Возбуждение и сокращение являются функциями разных структурных элементов мышечного волокна. Возбуждение — это функция поверхностной клеточной мембраны, а сокращение — функция миофибрилл.
Сила сокращения сердца прямо пропорциональна длине его мышечных волокон, т. е. степени их растяжения при изменении величины потока венозной крови. Иначе говоря, чем больше сердце растянуто во время диастолы, тем оно сильнее сокращается во время систолы. Эта особенность сердечной мышцы, установленная О. Франком и Е. Старлингом, получила название закона сердца Франка-Старлинга.
Поставщиками энергии для сокращения сердца служат АТФ и КрФ, восстановление которых осуществляется окислительным и гликолитическим фосфорилированием. При этом предпочтительными являются аэробные реакции.