Материал: Лекция 3.Мед.хим
1
Лекция: «РАСТВОРЫ ВЫСОКОМОЛЕКУЛЯРНЫХ СОЕДИНЕНИЙ».
Ассистент Сидоренко Л.М.
ПЛАН ЛЕКЦИИ.
1.Понятие о растворах высокомолекулярных соединений (ВМС). Биополимеры.
2.Сравнительная характеристика растворов высокомолекулярных соединений, истинных и коллоидных растворов.
3.Краткая структура белка.
4.Белки, как высокомолекулярные электролиты. Изоэлектрическая точка белка и методы ее определения.
5.Устойчивость растворов высокомолекулярных соединений. Методы осаждения биополимеров: высаливание, коацервация и их биологическое значение.
6.Вязкость растворов ВМС. Вязкость крови.
7.Коллоидно-осмотическое давление в растворах ВМС. Мембранное равновесие Доннана.
8.Набухание и растворение ВМС. Механизм набухания. Факторы, влияющие на набухание. Биологическое значение набухания.
9.Застудневание растворов ВМС. Факторы, влияющие на застудневание. Тиксотропия. Синерезис. Биологическое значение этих процессов.
1.ПОНЯТИЕ О РАСТВОРАХ ВЫСОКОМОЛЕКУЛЯРНЫХ
СОЕДИНЕНИЙ (ВМС). БИОПОЛИМЕРЫ.
Высокомолекулярные соединения (ВМС) – это вещества с большой молекулярной массой порядка 104 – 10 6 а.е.м. Макромолекулы построены из большого числа повторяющихся звеньев.
ВМС (или полимеры) получаются в результате полимеризации или поликонденсации. Все полимеры делятся на природные (белки, нуклеиновые кислоты и др.), синтетические (нейлон, полиэтилен и др.) и искусственные, которые получаются в результате химической обработки природных полимеров (например, целлофан, нитроклетчатка и др.)
Синтетические полимеры находят широкое применение в медицине (аппарат «искусственная почка», плазма крови, эндопротезирование и много др.).
Биополимеры являются структурной основой всех живых организмов. К ним относятся, прежде всего нуклеиновые кислоты, белки и их производные: нуклепротеиды, гликопротеиды, липопротеиды и т.д., а ткже гликоген. Эти соединения являются основным строительным материалом для протоплазмы и ядерного вещества клеток и содержатся во многих биологических жидкостях.
Нуклеиновые кислоты являются полимерами, содержащими от десятков до сотен тысяч нуклеотидов. Они являются важнейшим классом биополимеров, выполняя генетические функции и определяя весь ход развития живого организма.
2
Полисахариды (крахмал, гликоген и др.) являются полимерами глюкозы. Они выполняют структурную функцию и являются запасной формой питательных веществ.
Белки являются природными полимерами, которые образуются в результате реакции поликонденсации аминокислот.
Значение белков, нуклеиновых кислот, полисахаридов и их производных чрезвычайно велико, оно подробно рассматривается в курсе биохимии.
2. СРАВНИТЕЛЬНАЯ ХАРАКТЕРИСТИКА РАСТВОРОВ ВМС. ИСТИННЫХ И КОЛЛОИДНЫХ РАСТВОРОВ.
Высокомолекулярные соединения образуют растворы, обладающие свойствами как коллоидных так и истинных растворов.
Свойства растворов ВМС, характерные для коллоидных растворов:
∙размер частиц (молекул ВМС) соответствует размеру коллоидных частиц (10–7 – 10 –9 м);
∙растворы ВМС не проходят через полупроницаемые мембраны;
∙явление светорассеивания (размытый конус Тиндаля);
∙способность к коагуляции;
∙медленно диффундируют.
Свойства растворов ВМС, характерные для истинных растворов:
∙гомогенность;
∙термодинамическая устойчивость;
∙самопроизвольность образования (растворяются в определенных жидкостях, не требуя стабилизаторов);
∙обратимость коагуляции.
ВМС имеют и специфические свойства – они набухают, их растворы обладают высокой вязкостью и способностью желатинироваться. По современной классификации растворы ВМС относят к гомогенным растворам, имеющим ряд свойств коллоидов и специфические свойства.
3. КРАТКАЯ СТРУКТУРА БЕЛКА.
Белки бывают простые и сложные. Простой белок – продукт поликонденсации 20 α-аминокислот. Сложные белки состоят из простого белка и небелковых компонентов.
Различают 4 структуры белка.
Первичная структура белка – это последовательность аминокислот в полипептидной цепи, связанных ковалентной пептидной связью.

3
Структура полипептидной цепи:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
NH2 |
|
|
|
CH |
|
C |
|
NH |
|
CH |
|
C |
|
NH |
|
CH |
|
C |
|||||||
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R1 |
|
O |
|
|
|
R2 |
|
O |
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
R3 |
|||||||||||||||
Вторичная структура белка является пространственной структурой, образуется за счет ближнего взаимодействия водородных и дисульфидных связей. Это приводит к образованию α-спиралей и β-структур.
Третичная структура белка образуется за счет дальнего взаимодействия между макромолекулами. Это межмолекулярные, гидрофобные взаимодействия, а также водородные связи. Каждый белок имеет свою специфическую структуру, называемую конформацией.
Четвертичная структура белка образуется из двух и более полипептидных цепей (например, гемоглобин). Объединение таких субъединиц происходит за счет водородных, дисульфидных, гидрофобных
связей, сил Ван-дер-Ваальса.
Все белки подразделяются на глобулярные и фириллярные.
Глобулярные белки имеют сферическую или эллипсидную форму, например гемоглобин. Глобулярный белок может содержать неаминокислотный фрагмент – простетическую группу. В гемоглобине – гем.
Фибриллярные белки содержат одну или более полипептидных цепей, молекулы их вытянуты, длина во много раз превышает диаметр. Это структурные белки соединительных, эластичных и сократительных тканей, белки волос и кожи.
4. БЕЛКИ КАК ВЫСОКОМОЛЕКУЛЯРНЫЕ ЭЛЕКТРОЛИТЫ. ИЗОЭЛЕКТРИЧЕСКАЯ ТОЧКА БЕЛКА И МЕТОДЫ ЕЁ ОПРЕДЕЛЕНИЯ.
Молекула белка имеет электрический заряд, обусловленный диссоциацией ионогенных групп (– СООН) и (– NH 2): эти группы принадлежат концевым аминокислотам, а также дикарбоновым и диаминовым аминокислотам, расположенным в середине полипептидной цепи. В результате диссоциации образуется биполярный ион (амфиион), имеющий положительный и отрицательный заряд. Схематически диссоциацию можно представить так:
R |
COOH |
|
|
|
COOH |
|
|
COO- +H+ |
|
+ H2O |
|
|
|
R |
|
|
|
R |
|
|
|
|
|
|
|||||
|
|
|
|
|
|
||||
|
NH2 |
|
|
|
NH3OH |
|
|
NH3+ +OH- |
|
Преобладание в |
молекуле белка |
групп – СООН сообщает ему |
|||||||
отрицательный заряд, белок проявляет свойства слабой кислоты. Преобладание групп – NH 2 сообщает белку положительный заряд и основные свойства.

4
В зависимости от реакции среды молекула белка заряжается следующим образом:
а) в кислой среде – положительно:
COO- |
|
|
|
|
COOH |
R |
+ H+ |
|
|
|
R |
|
|
||||
|
|
|
|||
NH3+ |
|
|
|
|
NH3+ |
б) в щелочной среде – отрицательно:
|
COO- |
|
|
|
|
COO- |
R |
+OH- |
|
|
|
R |
+ H O |
|
|
|||||
|
|
|
||||
|
NH3+ |
|
|
|
|
2 |
|
|
|
|
|
NH2 |
Таким образом, заряд белка зависит от реакции среды, соотношения количества карбоксильных групп и степени их диссоциации.
Биполярный ион или амфион принято называть цвиттер-ионом.
Значение рН, при котором белок находится в изоэлектрическом состоянии, т.е. в состоянии, при котором число положительных и
отрицательных зарядов одинаково, общий заряд равен нулю, называется
изоэлектрической точкой белка (ИЭТ).
Изоэлектрическая точка является важной характеристикой белков. Каждый
белок имеет свою индивидуальную ИЭТ. Существуют следующие методы ее определения:
1.По электрофоретической подвижности. При проведении электрофореза белок при значении рН, равному ИЭТ, не перемещается в электрическом поле.
2.По степени коагуляции (высаливания). В ИЭТ наблюдается наибольшее помутнение раствора и белок выпадает в осадок.
3.По скорости желатинирования. Желатинирование (или застудневание) происходит быстрее всего в ИЭТ.
4.По величине набухания. Наименьшее набухание белка происходит в пробирке, где рН ближе к ИЭТ.
5.УСТОЙЧИВОСТЬ РАСТВОРОВ ВМС. МЕТОДЫ ОСАЖДЕНИЯ БИОПОЛИМЕРОВ: ВЫСАЛИВАНИЕ,КОАЦЕРВАЦИЯ. ИХ
БИОЛОГИЧЕСКОЕ ЗНАЧЕНИЕ.
Основным фактором термодинамической устойчивости растворов биополимеров (ВМС) является их высокая гидрофильность, которая обусловлена наличием таких гидрофильных групп, как – NH 2, – COOH , – OH,
–SH, – CO – NH –, пептидные связи и др.
Врезультате вокруг макромолекулы образуется монослой растворителя, называемый сольватной или гидратной оболочкой. Дополнительным фактором устойчивости является наличие заряда на молекуле белка, обусловленное ионогенными группами. Растворы ВМС самопроизвольно не осаждаются.
Чтобы лишить высокомолекулярные частицы устойчивости, необходимо удалить гидратную оболочку и снять электрический заряд.
Одним из методов осаждения белков является высаливание.
5
ВЫСАЛИВАНИЕ:
Высаливание – это процесс осаждения белков с помощью концентрированных растворов солей. Для высаливания чаще всего используют соли Na2SO4, (NH4)2SO4, фосфаты.
Высаливание наиболее эффективно в ИЭТ белка, что и используется для её определения. Учитывая механизм осаждающего действия электролитов и других водоотнимающих средств, немецкий биохимик Кройт предложил общую схему высаливания.
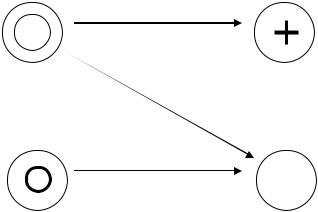
Схема высаливания по Кройту.
+
электролит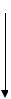
спирт, ацетон
большая
концентрация
электролита
спирт, ацетон
электролит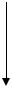
Из схемы видно, что необходимо удалить гидратную оболочку (спиртом или ацетоном) и снять заряд электролитом. Последовательность этих действий не имеет значения. Для осаждения многих белков достаточно большой концентрации одного электролита, особенно сульфатов, которые обеспечивают снятие и заряда, и дегидратацию частицы.
Высаливающее действие электролитов зависит от способности их ионов гидратироваться. Ученый Гофмейстер установил последовательность высаливающего действия анионов и катионов.
Лиотропный ряд анионов:
SO42– > F– > (цитрат)3– > (тартрат)2– > (ацетат)– > Сl– > NO3– > Br– > CNS–
Лиотропный ряд катионов:
Li+ > Na+ > K+ > Rb+ > Cs+ > Mg2+ > Ca2+ > Sr2+ > Be2+
Процесс высаливания используется для приготовления некоторых лечебных сывороток и противокоревого α-глобулина, а также для разделения белков на фракции при биологических исследованиях.