Материал: Курсовая по микробиологии
Заключение
Таким образом, значение биологического азота велико и многообразно. Являясь одним из основных звеньев экологизации сельскохозяйственного производства, биологический азот позволяет получать высокие стабильные урожаи, обеспечивая воспроизводство почвенного плодородия.
Его рациональное использование в сочетании с оптимальным обеспечением сельскохозяйственного производства минеральными азотными удобрениями даст возможность успешно решить общую проблему азота в земледелии страны.
Улучшение обеспечения сельскохозяйственных культур биологическим азотом может быть осуществлено путем создания с помощью генной инженерии азотфиксирующих форм высших растений. Это обеспечит получение в сельскохозяйственном производстве огромного агроэкономического эффекта.
-
Практическая часть
-
Объект исследований
Для микробиологического анализа был взят чернозем типичный. Чернозем – это плодородная земля, имеющая черный оттенок цвета, земля, наделенная огромным количеством гумуса и имеющая зернисто-комковатую структуру. Как правило, черноземные почвы формируются в лесу, а так же на суглинках и глинах при умеренно-континентальном климате.
На сегодняшний день чернозем можно по праву считать самой лучшей для фермеров, земледельцев и садоводов почвой, почвой, на которой прекрасно растут, как цветы, деревья и кустарники, так и плодовые культуры, такие, как томаты, огурцы, перцы и т.п. Следовательно, чернозем – это прекрасная садовая земля, отличная земля для огородов, а так же для домашних комнатных растений.
На территории нашего государства черноземные почвы в большинстве своем преобладают в Западной Сибири, на Северном Кавказе, в Поволжье, в центрально-черноземных областях, а так же их можно увидеть сегодня на территории Украины, в Северной и Южной Америке, в Китае и ряде европейских государств.
Чернозем подразделяют специалисты на 5 основных видов. 1. Выщелоченный. Он формируется в лесостепной зоне в процессе отмирания разнотравно-злаковых растений. 2. Оподзоленный. Присущ широколиственным травянистым лесам. 3. Обыкновенный. Формируется лесостепной зоне в процессе отмирания разнотравной растительности. 4. Типичный. Формирование типичного чернозема происходит на суглинках, в лугово-степных зонах и в лесостепных регионах в результате распада разнотравно-злаковых культур. 5. Южный. Формируется он в результате отмирания типчаково-ковыльной растительности в степных зонах в южной их части.
-
Отбор образцов почвы
Пробы почвы отбираются на каждом из участков в его пяти точках по диагонали или по «конверту» (четыре точки по углам и одна в центре).
Если исследователя интересуют последствия непосредственного внесения химического вещества в почву, то пробы отбираются поверхностно (0—1 см) стерильным инструментом (нож, шпатель) в количестве 0,3—0,5 кг в одной точке.
Если изучается воздействие химического вещества на микрофлору почвенного горизонта, то для отбора проб почвы пользуются следующей методикой. Каждая точка, в которой проводится отбор проб почвы, представляет собой центр выбранного для исследования 1 м2 территории. Здесь выкапывается шурф размером 0,3 х 0,3 м и глубиной 0,2 м. Поверхность одной из стенок шурфа очищают стерильным ножом. Затем из этой стенки вырезают почвенный образец, размер которого обусловлен заданной навеской. Так, если необходимо отобрать 200 г почвы, размер образца 20 см х 3 см х 3 см; 500 г — 20 см х 5 см х 30 см.
При изучении воздействия пестицидов и других химических веществ на микрофлору и процессы самоочищения в более глубоких слоях почвы, для отбора проб почвы пользуются шурфом глубиной до 1 м. Пробы отбираются из стенки шурфа стерильным инструментом через каждые 10 см.
Отобранные образцы помещают в стерильную посуду и доставляют в лабораторию. При невозможности приступить к исследованию почвы немедленно, допускается хранение образца при температуре 4—5°С, но не более 24 часов. 2.1 Подготовка и обработка почвы для анализа
Для приготовления среднего образца объемом 0,5 кг почву всех образцов одного участка высыпают на стерильный плотный лист бумаги, тщательно перемешивают стерильным шпателем, отбрасывают камни и прочие твердые предметы. Затем почву распределяют на месте ровным тонким слоем в форме квадрата. Диагоналями почву делят на 4 треугольника. Почву из двух противоположных треугольников отбрасывают, а оставшуюся вновь перемешивают, опять распределяют тонким слоем и делят диагоналями и так до тех пор, пока не останется примерно 0,5 кг.
Перед посевом почву диспергируют, т.е. почву с соблюдением условий стерильности просеивают через сито диаметром 3 мм. При просеивании сито сверху покрывают стерильной бумагой.
-
Определение влажности
Влажность почвы – содержание в почве влаги в твердом, жидком и газообразном состоянии. Влажность почвы определяется в процентах от массы сухой почвы или от ее объема. От соотношения влаги и воздуха в почве зависит в значительной степени рост и развитие растений.
Для расчета влажности применяется следующая формула:
А%
=
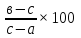 ,
где
,
где
[А] – влажность почвы
[в] – масса бюкса с влажной почвой
[с] – масса бюкса с сухой почвой
[а] – масса пустого бюкса
Расчеты:
а = 24,9
в = 30,2
с = 28,6
А% = 43,24%
Следовательно, что при такой влажности 1 г сырой почвы имеет 0,43 г абсолютно сухой почвы.
-
Метод учёта численности
При определении численности бактерий сначала готовят суспензии, навеску почвы переносят в колбу ёмкостью 250 мл, содержащую 90 мл стерильной водопроводной воды, интенсивно сбалтывают вращательным движением в течение 10 минут и дают отстояться грубым частицам почвы. Затем методом разведения готовят суспензии, содержащие разное количество почвы. С этой целью из предыдущего разведения стерильной пипеткой переносят по 1 мл суспензии в последующую пробирку, содержащую также 9 мл стерильной водопроводной воды. В первой пробирке 1 мл суспензии, приготовленной по этому методу, соответствует разведению 10^-1 . Последующие составляют 10^-2,10^-3,10^-4 и т.д.
-
Методы посева
Из полученных разведений проводят посев на плотные среды. Используется техника посева в толщу плотной среды. В чашку Петри добавляют 1 мл исследуемой культуры ( в нашей работе несколько разведений), потом приливают 15-20 мл расплавленной и охлажденной до 48°С плотной питательной среды и перемешивают. Культуру и среду смешивают энергичными круговыми движениями чашки и дают затвердеть на ровной горизонтальной поверхности, а после помещают в термостат. Колонии вырастают в толще и на поверхности среды и если среда прозрачная, то могут быть легко подсчитны.
В тех случаях, когда после подсчета колоний может возникнуть необходимость в выделении чистой культуры и ее идентификации для определения количества жизнеспособных микроорганизмов, используют метод поверхностного посева. Питательную среду разливают в чашки Петри и после застывания подсушивают, переворачивая чашки вверх дном и выдерживая их открытыми в термостате 30 мин при температуре 37°С (или в ламинарном боксе 1-2 ч). В центр маркированной чашки Петри вносят заданное количество исследуемого жидкого материала или его разведения и немедленно равномерно распределяют по поверхности среды стерильным стеклянным или пластиковым шпателем до тех пор, пока на агаре не останется видимых следов жидкости. Чашки с посевами переворачивают, помещают в термостат, установленный на соответствующий температурный режим.
Так же используется метод обрастания комочков. Поверхность геля покрывают стерильным кружком фильтровальной бумаги, по которому раскладывают (по трафарету) 30 комочков почвы (диаметром 1—2 мм).
Плотность обрастания комочков почвы целлюлозе-разрушающими микроорганизмами можно выразить в процентах.
Палочкой с оттянутым концом (предварительно ее слегка проводят над огнем и смачивают водой) захватывают комочек почвы (диаметр 1—2 мм) и по трафарету помещают на поверхность эмалевой пластины.
Через некоторое время в зависимости от активности нитрифицирующих бактерий (спустя 7, 14, 21 день) вокруг отдельных комочков почвы появляются зоны растворения мела, свидетельствующие об обрастании комочков почвы нитрифицирующими бактериями.
Чашки вынимают и подвергают анализу: определяют процент обрастания комочков почвы нитрифицирующими бактериями, изучают по морфологии их представителей и продукты жизнедеятельности.
-
Используемые питательные среды для количественного и качественного анализа микроорганизмов
Мясопептонный агар (МПА)- Универсальная твердая питательная среда на натуральной основе для культивирования широкого спектра микроорганизмов. Предназначена для выращивания и изучения культурально-морфологических свойств микроорганизмов различных таксономических групп. На МПА выявляют бактерии хемотрофы. При приготовлении среды к готовому мясопептонному бульону (до стерилизации или после нее) добавляют 2-3% измельченного агар-агара и кипятят, помешивая, на слабом огне до полного расплавления агара. МПА можно варить в автоклаве или аппарате Коха. Готовую среду, если нужно, осветляют, фильтруют и стерилизуют 20 мин при 120° С.
Сусло-агар (СА)- применяют для первичного посева материала с целью выделить дрожжи или грибы. Состоит из 1 л пивного сусла и 18-20 г агара, рН 6,5-7. Стерилизация-при 112°С в течение 15 мин.
Среда Ваксмана- используется для выявления актиномицетов. Состав: (NH4)2SO4 – 0,2 г; KH2PO4 – 3 г; MgSO4×7H2O – 0,5 г; CaCl2×6H2O – 0,25г; FeSO4 ×7H2O – следы; сера (S) порошком – 10 г; дистиллированная вода- 1л.
Среда Гетчинсона- выявляет целлюлозорасщепляющие микроорганизмы. Состав (г/л): NaNO3 - 2,5; FeCl3 - 0,01; K2HPO4 - 1; MgSO4*7H2O - 0,3; NaCl - 0,1; CaCl2 - 0,1; pH среды доводят до 7,2, добавлением 20% - го раствора Na2CO3; дистиллированная вода; МПА.
Среда Эшби- выявляет азотобактер путем раскатывания комочков почвы. Состав (г): сахароза — 20,0; К2НР04 — 0,2; MgS04-7H20 — 0,2; NaCI — 0,2; FeS04 — 0,1; СаСОз — 5,0; вода дистиллированная — 1000 мл. В среду рекомендуется вносить смесь микроэлементов — 1 мл/л.
-
Учет численности микроорганизмов на плотных средах
Таблица 1
Учет микроорганизмов велся на 2-3 сутки инкубации.
-
Количественная и качественная оценка микроорганизмов на мпа
|
Разведение |
Общее количество микро-организмов |
Среднее количество колоний |
Количество микроорганизмов в 1 г абсолютно сухой почвы (КОЕ/г) |
Количество колоний доминирующих микроорганизмов |
Доминирующие формы микроорганизмов на 1 г (КОЕ/г) |
Доля доминирующих форм в общей численности |
|
10-4 |
95 |
76 |
17,6*10^5 |
74 |
17,2*10^5 |
97,7% |
|
56 |
Количество микроорганизмов в 1 г абсолютно сухой почвы:
Общее количество микроорганизмов = общее кол-во колоний × разведение/ масса абсолютно сухой почвы
1) Общее количество микроорганизмов в 4-ом разведении = 76×104/ 0,43 = 17,6*10^5
Количество микроорганизмов доминирующей формы в 1 г абсолютно сухой почвы:
1) Общее количество доминирующих микроорганизмов в 4-ом разведении = =74×104/ 0,43 =17,2*10^5