Материал: Качественный и количественный анализ диметилсульфоксидов нефти
На основе температурной зависимости эффективных
констант скоростей накопления сульфоксидов в координатах уравнения Аррениуса
проведена оценка значений эффективной энергии активации (табл. 3, 4). Данные
таблиц 3 и 4 показывают, что с увеличением концентрации окисляемого сульфида
наблюдается тенденция к снижению энергетического барьера реакции.
Предварительная выдержка катализатора в пероксиде водорода также снижает
эффективную энергию активации, вследствие чего возрастают скорость окисления и
выход целевого продукта реакции (табл. 2 - 4).
Глава III
Кинетические закономерности окисления нефтяных сульфидов в присутствии
растворенного кислорода
В присутствии пероксида водорода и растворенного кислорода (900С, 2 часа) углеводороды фракции дизельного топлива практически не окисляются, на что указывает отсутствие гидропероксидов (иодометрия) и карбоновых кислот (алкалиметрия). Пероксид водорода слабо окисляет (900С) сульфиды дизельного топлива (R2S) и поэтому скорость накопления сульфоксидов лежит в пределах ошибки эксперимента (± 5%); в этих условиях также не проявляется окислительное воздействие растворенного кислорода. Поэтому была изучена возможность радикально-цепного окисления как углеводородной цепи сульфида, так и смеси углеводородов под действием растворенного кислорода в присутствии пероксида водорода и катализатора молибденовой кислоты при дополнительном барботаже кислородом воздуха.
При барботаже воздуха через реакционную смесь не
изменяется вид кинетических кривых, и они трансформируются в прямые линии в
координатах уравнения (1.II)
с коэффициентом корреляции 0.993 ÷ 0.995. Однако
эффективная константа скорости накопления сульфоксидов, найденная из этих
трансформаций кинетических кривых, возрастает до некоторого предельного
значения при увеличении объемной скорости барботажа (рис.3.).
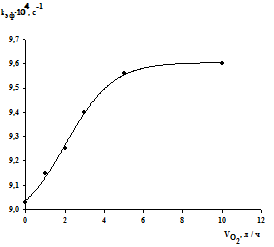
Рис.3. Зависимость эффективной константы
скорости реакции от скорости подачи кислорода. [H2MoO4]
= 0.005% масс., [Н2О2]0= 5.9 % масс. продолжительность окисления 2.5 ч
Возрастание удельной скорости накопления сульфоксидов на 6.5 % при барботаже реакционной смеси кислородом воздуха может быть вызвана двумя причинами. Во-первых, кислород воздуха может окислить углеводороды дизельного топлива до гидропероксидов, которые наряду с пероксомолибденовой кислотой способны окислять сульфиды до сульфоксидов. Во-вторых, рост эффективной константы скорости накопления сульфоксидов может быть связан с улучшением гидродинамического режима проведения данной гетерофазной реакции в результате более эффективного перемешивания водной и органической фаз реакционной системы.
Известно, что углеводороды окисляются по
радикально-цепному механизму. Окисление углеводородов ускоряется добавками
радикального инициатора и замедляется в присутствии ингибиторов. Введение в
реакционную смесь добавок радикального инициатора - персульфата аммония (ПСА)
не повлияло на скорость процесса (табл. 5). На удельную скорость накопления
сульфоксидов не оказывают влияния также и добавки фенола,
являющегося
ингибитором пероксильных радикалов (табл. 5).
Таблица 5. Эффективные константы скорости накопления сульфоксидов в опытах с добавлением фенола, персульфата аммония и без добавок. Т = 600С, [R2S] = 1.5% масс., [H2MoO4] = 0.005% масс., [Н2О2]0= 5.9 % масс.
|
Добавленный реагент |
Без добавок |
[ПСА]=1.4·10ˉ² моль/л |
[PhOH]=10ˉ³ моль/л |
[PhOH]=10ˉ² моль/л |
|
kэф ·104, c-1 |
9.6±1.8 |
9.7±1.8 |
9.6±1.7 |
9.6±1.7 |
Таким образом, в системе «углеводород + нефтяные
сульфиды + пероксид водорода + молибденовая кислота + вода» не протекает
радикально-цепное окисление органических соединений. Очевидно, продувка
реакционной смеси воздухом улучшает гидродинамический режим протекания реакции
окисления нефтяных сульфидов.
Глава IV
Автокатализ в реакции перекисного окисления нефтяных сульфидов в присутствии
оксида молибдена (VI)
Оксид молибдена (VI)
проявляет каталитическую активность в реакции окисления нефтяных сульфидов,
однако расходование сульфидов и накопление сульфоксидов протекает с
возрастающей во времени скоростью (рис.6).
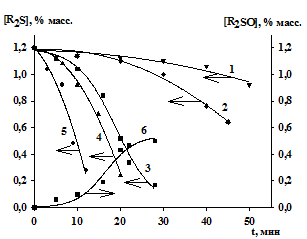
Рис. 6. Кинетические кривые
расходования сульфидов и кинетическая кривая накопления сульфоксидов (6). [R2S]0 = 1.2 %
масс., [H2O2]0 = 4.7 %
масс, [МоО3] = 0.001 % масс., Т0С: 50 (1), 60 (2), 70 (3, 6), 80 (4), 90 (5),
продолжительность окисления 50 мин
Сопоставление экспериментальных данных рис.1 и рис.6 показывает, что механизм окисления сульфидов в присутствии МоО3 имеет отличительные признаки по сравнению с вышеприведенной схемой окисления в присутствия молибденовой кислоты, на что указывает вид кинетических кривых расходования сульфидов и накопления сульфоксидов в этой реакции (рис. 6), типичный для автокаталитических реакций.
Как и в случае молибденовой кислоты, предварительная выдержка катализатора МоО3 в пероксиде водорода ускоряет реакцию, хотя и сохраняется автокаталитический характер (рис.7).
Автокаталитический характер реакции означает, что в ходе окисления сульфидов образуется дополнительное количество активной формы катализатора. Для объяснения полученных экспериментальных данных предложена следующая схема реакции:
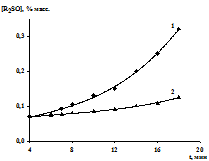
Рис. 7. Кинетические кривые накопления
сульфоксидов с выдержкой МоО3 в H2O2
(1) и без выдержки (2). Т = 600С, [R2S]0
= 1.2 % масс., [МоО3] = 0.001 % масс., [H2O2]0
= 4.7 % масс
![]() (1.1)
(1.1)
![]() (1.2)
(1.2)
![]() (2)
(2)
![]() (3)
(3)
![]() (1.3)
(1.3)
Согласно схеме, ответственными за автокатализ являются стадии (1.2) и (1.3). В данной схеме учтена побочная реакция (1.1) распада пероксида водорода. Остальные стадии являются такими же, как и при катализированном молибденовой кислотой окислении сульфидов.
Кинетический анализ данной схемы проведен для начальной стадии и развившегося окисления.
Начальная стадия процесса. Опираясь на данные рис. 7 можно заключить, что лимитирующей стадией выступает, вероятнее всего, реакция (1.2). Взаимодействие MoO3 с H2О2 происходит относительно медленно и поэтому предварительное выдерживание оксида молибдена (VI) в пероксиде водорода (рис. 7) позволяет накопить до начала опыта определенную концентрацию активной формы катализатора. Вклад стадии (1.3) в образование H2MoO5, скорее всего, мал из-за низкой концентрации H2MoO4.
Скорости расходования R2S
и H2MoO4
в стадии (2) равны
![]() (5.I)
(5.I)
Скорость расходования H2MoO5
лимитируется, в свою очередь, скоростью ее образования в стадии (1.2) и поэтому
V2 = V1.2
![]() (5.II)
(5.II)
С учетом этих соотношений получаем
![]() (5.III)
(5.III)
т.е. скорость расходования сульфида зависит от текущей концентрации пероксида водорода.
Для нахождения текущей концентрации пероксида
водорода рассмотрим расходование H2О2
в стадиях (1.1) и (1.2) (расходованием H2О2
в стадии (1.3) пренебрегаем вследствие малой скорости из-за низкой концентрации
H2MoO4)
![]()
![]()
![]()
![]() (5.IV)
(5.IV)
![]() (5.V)
(5.V)
В присутствии оксида молибдена (VI)
пероксид водорода действительно расходуется по закону реакции первого порядка,
о чем свидетельствует линейная трансформация кинетической кривой в координатах
уравнения (5.IV) и
литературные данные (Харлампиди Х.Э.) (рис.8). Тангенс угла наклона
логарифмической анаморфозы равен сумме констант k1.1
+ k1.2 = 0.16 ± 0.02
мин-1.
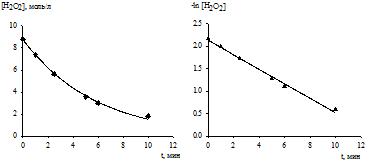
Рис. 8. Кинетическая кривая и
логарифмическая анаморфоза расходования пероксида водорода. Т = 700С, [R2S]0 = 1.2 %
масс., [МоО3] = 0.001 % масс., [H2O2]0 = 4.7 %
масс
Для нахождения уравнения кинетической кривой
расходования сульфида выражение для [H2О2]t
подставили в уравнение (5.III)
и провели соответствующие математические преобразования
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Действительно, кинетические кривые расходования сульфидов (рис. 6) описываются уравнением (5.VI), на что указывает линеаризация этих кривых в координатах уравнения (5.VII).
Из тангенса угла наклона логарифмических
анаморфоз вычислены значения суммы k1.1
и k1.2, температурная
зависимость которых описывается уравнением Аррениуса:
ln(k1.1
+ k1.2) = (-4.2 ± 1.7)
- (10.5 ± 4.9)∙103/RT
При Т = 700С значение k1.1 + k1.2 = 0.14 ± 0.03 мин-1 практически совпадает со значением суммы k1.1 + k1.2 = 0.16 ± 0.02 мин-1, полученной по данным расходования пероксида водорода. Такое совпадение эффективной константы скорости расходования пероксида водорода, полученной из разных экспериментальных данных, свидетельствует о том, что на начальной стадии окисление сульфидов действительно лимитируется реакцией (1.2).
На начальной стадии активная форма катализатора образуется в основном из оксида молибдена (VI). Однако по мере накопления H2MoO4 в развившемся окислении начинает доминировать реакция (1.3).
Развившееся окисление. Процесс лимитируется
стадией (3) и расходование сульфидов описывается уравнением
![]() (5.VIII)
(5.VIII)
В условиях квазистационарности
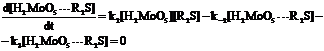
![]() (5.IX)
(5.IX)
Если принять концентрацию пероксомолибденовой кислоты также квазистационарной, получаем
![]() (5.X)
(5.X)
С учетом соотношений (5.IX)
и (5.X) уравнение
приобретает вид
![]() (5.XI)
(5.XI)
Из уравнения (5.XI)
следует, что скорость расходования сульфидов пропорциональна сумме k1.2+k1.3[H2MoO4].
По мере накопления H2MoO4
в стадии (3) начинает выполняться условие k1.3[H2MoO4]
>> k1.2 и поэтому
активная форма катализатора образуется из молибденовой кислоты. Порядок реакции
по пероксиду водорода первый, что подтверждается экспериментальными данными.
Порядок реакции по сульфидам должен быть переменным и зависит от соотношения
концентраций R2S
и H2O,
точнее от соотношения величин k2[R2S]
и k -1.3[H2O].
При высоких концентрациях [R2S]0
и малой [H2O]0
выполняется неравенство k2[R2S]
>> k -1.3[H2O]
и тогда в уравнении (5.XI)
во второй дроби можно пренебречь величиной k
-1.3[H2O].
В этом случае
![]() (5.XII)
(5.XII)
Порядок реакции по сульфиду и воде нулевой. Скорость реакции будет зависеть от текущей концентрации пероксида водорода и накопившейся молибденовой кислоты.
При условии k -1.3[H2O] >> k2[R2S] (много воды и мало сульфида) пренебрегаем k2[R2S] и получаем
![]() (5.XIII)
(5.XIII)
Из уравнения следует, что порядок по сульфиду первый, порядок по воде отрицательный (-1). Это означает, что в технологическом процессе нужно подобрать оптимальное содержание воды, т.к. избыточная концентрация H2O отрицательно сказывается на скорости процесса.
Глубокие стадии. По мере расходования сульфидов начинает реализовываться условие уравнения (XIII) и снижение скорости расходования R2S вызывается влиянием двух факторов:
снижением концентрации сульфидов;
обратной пропорциональной зависимостью скорости реакции от концентрации воды.
Таким образом, процесс окисления сульфидов дизельного топлива протекает в условиях автокатализа: скорость реакции зависит не только от содержания оксида молибдена (VI), но и от концентрации накапливающейся молибденовой кислоты.
При использовании данной схемы
автокаталитического окисления сульфидов следует учитывать, что даже на
начальных стадиях начинает нарушаться материальный баланс (табл. 8).
Таблица 8. Материальный баланс в реакции окисления сульфидов. Т = 700С, [R2S]0 = 1.2 % масс., [H2O2]0 = 4.7 % масс, [МоО3] = 0.001 % масс
|
t, мин |
0 |
5 |
10 |
16 |
20 |
22.5 |
28 |
|
([R2S]+[R2SO]), % масс. |
1.20 |
1.18 |
1.16 |
1.03 |
0.95 |
0.81 |
0.71 |
|
|
|
|
|
|
|
|
|
Нарушение материального баланса, видимо, связано с дальнейшим окислением сульфоксида до сульфона.
Автокаталитический характер реакции перекисного
окисления сульфидов сохраняется и при применении смешанной каталитической
системы МоО3 + Н2МоО4 (рис. 9), однако при увеличении массовой доли
молибденовой кислоты уменьшается время достижения максимальной скорости реакции
(табл. 9)
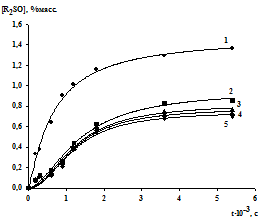
Рис. 9. Кинетические кривые накопления
сульфоксидов, в реакциях окисления сульфидов смешанной каталитической системой MoO3+
Н2МоО4, [R2S]0
= 1.5% масс, [Н2О2]0= 5.9 % масс.T=
600С, доля Н2МоO4, % : 1 -
100, 2 - 60, 3 - 50, 4 - 40, 5 - 0
Таблица 9. Значения максимальной скорости и времени достижения максимальной скорости в реакциях окисления сульфидов со смешанной каталитической системой MoO3 + Н2МоО4 . [R2S]0 = 1.5 % масс, T = 600С, [Н2О2]0= 5.9 % масс. продолжительность окисления 1.5 ч
|
Доля Н2МоO4, % |
Время достижения максимальной скорости, с |
Максимальная скорость Vmax·104 , % масс/c |
|
0 |
240 |
3.4 |
|
40 |
230 |
3.6 |
|
50 |
200 |
4.0 |
|
60 |
170 |
4.2 |
|
100 |
0 |
13.3 |