Материал: Качественный и количественный анализ диметилсульфоксидов нефти
Качественный и количественный анализ диметилсульфоксидов нефти
Курсовая работа
Качественный
и количественный анализ диметилсульфоксидов нефти
Содержание
Введение
Глава I Кинетический анализ схемы перекисного окисления нефтяных сульфидов
Глава II Изучение влияния способа приготовления катализатора на кинетику перекисного окисления нефтяных сульфидов
Глава III Кинетические закономерности окисления нефтяных сульфидов в присутствии растворенного кислорода
Глава IVАвтокатализ в реакции перекисного окисления нефтяных сульфидов в присутствии оксида молибдена (VI)
Глава V Сравнение активности молибденовой и вольфрамовой кислот в реакции окисления нефтяных сульфидов
Заключение
Литература
Введение
окисление нефтяной сульфид
Средние фракции сернистых и высокосернистых нефтей содержат значительные количества сульфидов, служащих сырьем для получения концентратов сульфидов, сульфоксидов и сульфонов. Содержание сульфидов в широкой фракции дизельного топлива составляет примерно 2% масс. Основная масса сульфидов в нефти представлена диалкилсульфидами, производными тиофена. Идея о возможности производства сульфоксидов окислением нефтяного сырья была высказана еще в 60-х годах прошлого века, однако пути промышленной реализации данного относительно дешевого способа получения ценного продукта до сих пор не найдены.
Потенциальным потребителем нефтяных сульфоксидов в качестве составного компонента ингибиторов для защиты металлов от коррозии и асфальто-смолистых и парафиновых отложений (АСПО) является нефтедобывающая промышленность на всех стадиях добычи, подготовки, транспортировки и переработки нефти. Применяемые в настоящее время ингибиторы изготавливаются на основе дорогостоящих аминов иностранного производства.
Известно, что сульфоксиды выступают промежуточными продуктами в реакции окисления сульфидов и способны окисляться до сульфонов, что снижает выход целевого продукта. Предлагаемые в литературе методы окисления нефтяных сульфидов до сульфоксидов, как правило, малоселективны, и поэтому выход сульфоксидов невысок. В связи с этим актуально исследование кинетики и механизма окисления нефтяных сульфидов в условиях межфазного катализа и поиск новых каталитических систем для данной реакции.
Работа выполнена при поддержке Фонда Бортника содействия развитию инновационных проектов и при частичном финансировании по программе «Создание и модернизация химических технологий и материалов для инновационного развития экономики Республики Башкортостан» Государственной научно-технической программы Республики Башкортостан на 2011-2012 годы.
Цель исследования. Разработка перспективного для практического применения метода получения нефтяных сульфоксидов путем окисления нефтяных сульфидов. Основной задачей является изучение кинетических закономерностей и механизма окисления нефтяных сульфидов для достижения выхода целевого продукта - сульфоксида более 90%.
Научная новизна. Предложены схемы катализированного и автокатализированного пероксосоединениями молибдена и вольфрама окисления нефтяных сульфидов до сульфоксидов в условиях межфазного катализа и проведен их кинетический анализ. Предлагаемые схемы обоснованы и подтверждены экспериментальными данными.
Установлено, что ключевыми в механизме реакции перекисного катализированного окисления нефтяных сульфидов являются стадии образования и расходования комплекса пероксомолибденовой кислоты с исходным сульфидом. Экспериментально найдены условия реакции: гидродинамический режим, температура, соотношение начальных концентраций субстрата, пероксида водорода и катализатора, способствующие достижению максимально возможной концентрации ключевого интермедиата и высокому (более 90 %) выходу целевого продукта - сульфоксида.
Показано, что предварительная выдержка катализатора в пероксиде водорода снижает индукционный период реакции окисления нефтяных сульфоксидов.
Впервые показано, что окисление сульфидов дизельного топлива в присутствии оксида молибдена (VI) происходит в режиме автокатализа. Проведена интерпретация полученных экспериментальных результатов на основе кинетического анализа схемы автокаталитического окисления сульфидов. Кинетические закономерности данной реакции сохраняются также при перекисном окислении сульфидов в присутствии смешанного катализатора MoO3 + Н2МоО4, однако триоксид молибдена менее эффективен по сравнению с молибденовой кислотой и поэтому в его присутствии наблюдается более низкий выход целевого продукта.
Добавки полярных растворителей в окисляемую систему увеличивают взаимную растворимость реагентов и поэтому положительно влияют на данную межфазную реакцию.
Кинетические закономерности окисления сульфидов до сульфоксидов в присутствии соединений шестивалентного вольфрама и пероксида водорода аналогичны закономерностям, полученным при перекисном окислении в присутствии соединений молибдена. Каталитическая активность вольфрамовой кислоты ниже по сравнению с активностью молибденовой кислоты.
Глава I
Кинетический анализ схемы перекисного окисления нефтяных сульфидов
В литературном обзоре рассмотрено современное состояние знаний о механизме жидкофазного перекисного катализированного окисления сульфидов до сульфоксидов на границе водной и органической фаз.
Эксперимент проведен с использованием широко апробированных методов анализа продуктов реакции - нефтяных сульфоксидов (объемный анализ, УФ-спектрометрия, потенциометрия) и кинетического анализа схем химических реакций.
При катализированном молибденовой кислотой в
присутствии пероксида водорода окислении нефтяных сульфидов широкой фракции
дизельного топлива с температурой кипения 180 - 3000С накопление сульфоксидов в
условиях проведенных экспериментов протекает с убывающей во времени скоростью (рис.
1).
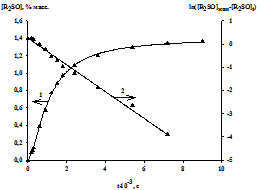
Рис.1. Кинетическая кривая накопления сульфоксидов (1) и ее трансформация (2) в координатах уравнения (1.III). Т = 600С, [R2S]0 = 1.5% масс., [H2MoO4] = 0.005% масс, [Н2О2]0= 5.9 % масс., продолжительность окисления 2.5 ч.
Примечание: концентрация нефтяных сульфидов приведена в расчете на элементарную серу
На основании литературных данных и
полученных результатов предложена следующая схема окисления нефтяных сульфидов
в сульфоксиды:
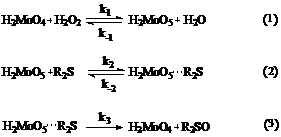
На основе предложенной схемы
проведен кинетический анализ данной реакции. Наиболее вероятно, что
лимитирующей является стадия (3), скорость которой описывается уравнением
![]() (1.I)
(1.I)
Применение условия квазистационарности и условия
материального баланса дает уравнение кинетической кривой накопления
сульфоксидов
![]() (1.II)
(1.II)
![]()
Заключение о достижении равновесия стадии (1) сделано на основании следующего экспериментального факта. На кинетической кривой накопления сульфоксида при окислении сульфида (рис. 1) достаточно быстро (~ 3 мин) достигается максимальная скорость реакции. По нашему мнению, максимальная скорость накопления сульфоксида достигается в момент установления максимально возможной равновесной концентрации пероксомолибденовой кислоты. Поэтому в дальнейшем при вычислении количественных параметров, описывающих данную реакцию, использовали участок кинетической кривой от момента установления максимальной скорости накопления сульфоксида до достижения предельной концентрации (рис. 1).
Кинетические кривые накопления
сульфоксидов линейны в координатах уравнения (1.II) (рис. 1)
на глубину превращения до 95 %. Коэффициент корреляции линеаризации кинетических
кривых накопления сульфоксидов при катализированном перекисном окислении
сульфидов лежит в пределах 0.990÷0.996. По тангенсу
угла наклона трансформаций кинетических кривых в координатах уравнения (1.II) определены
значения эффективной константы скорости kэф.
(табл.1).
Таблица 1. Влияние начальной концентрации сульфидов на эффективную константу скорости накопления сульфоксидов. Т = 600С, [H2MoO4] = 0.005% масс., [Н2О2]0= 3.9 ÷7.8 % масс. продолжительность окисления 2.5 ч
|
[Н2О2]0, моль/л |
1.60±0.15 |
2.40±0.05 |
3.20±0.20 |
|
[R2S]0, % масс. |
1.00 |
1.50 |
2.00 |
|
kэф·104, с-1 |
4.10±0.30 |
7.50±0.60 |
9.50±0.60 |
|
|
|
|
|
Как видно из данных таблицы 1, с увеличением [H2O2]0 возрастает kэф. Повышение концентрации пероксида водорода смещает равновесие стадии (1) вправо и поэтому возрастает [H2MoO5]равн.. В соответствии с уравнением (1.II), увеличение равновесной концентрации пероксомолибденовой кислоты приводит к росту эффективной константы скорости накопления сульфоксидов (табл.1).
Глава II
Изучение влияния способа приготовления катализатора на кинетику перекисного
окисления нефтяных сульфидов
Окисление нефтяных сульфидов (R2S) в модельных системах R2S + H2O2 и R2S + H2MoO4 практически не происходит и скорость реакции лежит в пределах ошибки эксперимента. Следовательно, несмотря на способность соединений молибдена образовывать комплексы, в последней модельной системе не образуются каталитически активные интермедиаты. Пероксид водорода также проявляет недостаточную окислительную активность. При совместном введении H2MoO4 и H2O2 нефтяные сульфиды окисляются до сульфоксидов (рис. 2). На кинетической кривой накопления сульфоксидов имеется небольшой индукционный период, по завершении которого наблюдается максимальная скорость реакции, а затем скорость процесса убывает во времени (рис. 2, кривая 2).
Наиболее вероятно, что индукционный период
связан с установлением равновесия в реакции
![]() (1)
(1)
С целью устранения индукционного периода катализатор предварительно выдерживали в течение 30 минут в пероксиде водорода. Предварительное выдерживание смеси H2O2 + H2MoO4 способствовало исчезновению индукционного периода (рис. 2, кривая 1).
При таком способе проведения
процесса окисления возрастает также выход целевого продукта, определенный в
виде отношения [R2SO]![]() / [R2S]0 при
варьировании как начальной концентрации сульфидов, так и температуры (табл. 2)
/ [R2S]0 при
варьировании как начальной концентрации сульфидов, так и температуры (табл. 2)
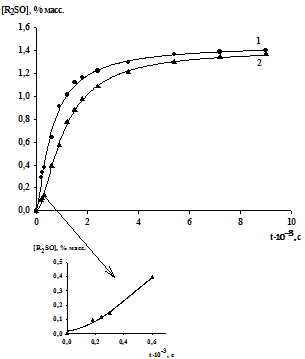
Рис. 2. Кинетические кривые накопления
сульфоксидов с выдержкой катализатора в пероксиде водорода (1) и без выдержки
(2) Т = 600С, [R2S]0
= 1.5% масс, [Н2О2]0= 5.9 % масс, [H2MoO4]
= 0.005% масс, продолжительность окисления 2.5 ч
Таблица 2. Зависимость выхода сульфоксидов от начальной концентрации нефтяных сульфидов и температуры. [H2MoO4] = 0.005% масс., [Н2О2]0= 3.9 ÷7.8 % масс. продолжительность окисления 2.5 ч
|
[Н2О2]0,, % масс. |
[R2SO] |
|||||
|
|
с выдержкой катализатора в пероксиде водорода |
без выдержки катализатора в пероксиде водорода |
||||
|
|
500С |
600С |
500С |
600С |
700С |
|
|
3.9 |
60.8 |
90.4 |
92.4 |
51.6 |
86.8 |
90.4 |
|
5.9 |
73.6 |
93.1 |
94.4 |
68.3 |
90.9 |
92.5 |
|
7.8 |
79.2 |
94.8 |
95.6 |
70.2 |
92.4 |
94.2 |
Наличие небольшого периода индукции не нарушает
линейную трансформацию кинетических кривых накопления сульфоксидов в
координатах уравнения (1.II)
с коэффициентом корреляции более 0.990, откуда вычислены эффективные константы
скорости накопления сульфоксидов (табл. 3 и 4). Данные таблиц свидетельствуют о
том, что при предварительном выдерживании катализатора возрастает эффективная
константа скорости образования целевого продукта окисления сульфидов во всем
изученном диапазоне концентраций и температур.
Таблица 3. Эффективные константы скорости накопления сульфоксидов и оцененные значения энергий активации в опытах без выдержки катализатора в пероксиде водорода, [H2MoO4] = 0.005% масс, [Н2О2]0= 3.9 ÷7.8 % масс., продолжительность окисления 2.5 ч
|
[Н2О2]0, % масс. |
kэф·104, с-1 |
Еа, кДж/моль |
||
|
|
500С |
600С |
700С |
|
|
3.9 |
3.7±0.2 |
4.1±0.3 |
5.8±0.5 |
26.0 |
|
5.9 |
7.2±0.7 |
7.5±0.6 |
9.1±0.6 |
10.0 |
|
7.8 |
9.2±0.3 |
9.5±0.6 |
9.7±0.5 |
2.7 |
Таблица 4. Эффективные константы скорости накопления сульфоксидов и оцененные значения энергий активации в опытах с выдержкой катализатора в пероксиде водорода. [H2MoO4] = 0.005% масс, [Н2О2]0= 3.9 ÷7.8 % масс., продолжительность окисления 2.5 ч
|
[Н2О2]0, % масс. |
kэф·104, с-1 |
Еа, кДж/моль |
||
|
|
500С |
600С |
700С |
|
|
3.9 |
4.4±0.1 |
4.7±0.2 |
6.3±0.4 |
15.9 |
|
5.9 |
9.0±0.7 |
10.3±0.5 |
10.7±0.1 |
8.0 |
|
7.8 |
10.5±0.5 |
10.8±0.8 |
11.0±0.8 |
2.2 |
Полученные экспериментальные результаты можно объяснить следующим образом. При одновременном смешивании R2S, Н2МоО4, Н2О2 пероксомолибденовая кислота образуется in situ и ее квазистационарная концентрация как промежуточного продукта зависит от того в какой мере достигнуто равновесие стадии образования (1) и стадии расходования
Вероятно, в опытах с предварительной выдержкой катализатора в течение 30 минут наиболее полно устанавливается равновесие стадии (1) и поэтому достигается более высокая квазистационарная концентрация каталитически активной формы (Н2МоО5). Как показано ранее, константа скорости накопления сульфоксидов линейно зависит от равновесной концентрации Н2МоО5. Вследствие этого в опытах с предварительной выдержкой катализатора наблюдаются более высокая скорость процесса и выход целевого продукта окисления (табл. 2 - 4).