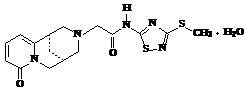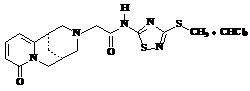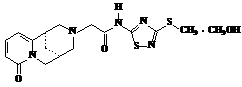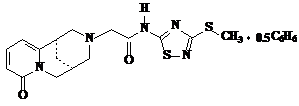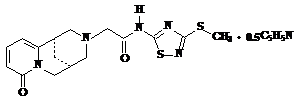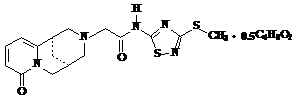Материал: Изучение кристаллизации N-(3-метилтио-5-ацетамидо-1,2,4-тиадиазолил) цитизина в различных средах
1.3 КРАТКОЕ ОБОБЩЕНИЕ ПРЕДСТАВЛЕНИЙ
О КЛАТРАТООБРАЗОВАНИИ И ПОЛИМОРФИЗМЕ
Таким образом, изучение явлений клатратообразования, начатое в 1947 году Г. Пауэллом, и полиморфизма является на сегодняшний день весьма актуальным. Об этом можно судить из современных многочисленных и разнообразных исследований в этих областях. Исходя из обсужденных нами выше данных, можно сделать следующие выводы:
1. Объекты клатратной химии разнообразны, от молекулярных комплексов неорганических соединений до биоорганических полимолекулярных комплексов.
2. Псевдополиморфы, сольваты и гидраты тоже являются клатратными соединениями.
. На формирование клатратов влияет фактор растворителя.
. Полиморфные модификации пока не имеют однозначно общепринятой номенклатуры, хотя инициативы в направлении унификации имеются.
. В КБСД содержатся примерно 3 % полиморфов, 16% сольватов и 10% гидратов.
. Клатратные и полиморфные соединения
широко используются на практике и в промышленности.
ГЛАВА 2. ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
.1 ХАРАКТЕРИСТИКА
ОБЪЕКТОВ ИССЛЕДОВАНИЯ
Хинолизидиновый алкалоид цитизин выделен из семян растения ракитника (Cytisus laburnum L.) и термопсиса ланцетолистного (Thermopsis lanceolata R. Br.) - оба из семейства бобовых (Leguminosae). Алкалоид относится к веществам “ганглионарного” действия и в связи с возбуждающим действием на дыхательный центр рассматривается как дыхательный аналептик (выпускается препарат под названием “Цититон”). В последние годы обнаружены новые биоактивные свойства, в частности, цитизином стали пользоваться как средством для отвыкания от курения (таблетки “Лобесил” <#"876019.files/image007.gif">
R = (CH2)n-CH3,
где
n=0 - 5
При исследовании рентгеноструктурным анализом кристаллов N-(3-метил- и -этилтио-5-ацетамидо-1,2,4-тиадиазолил)цитизинов, полученных из различных растворителей, обнаружили, что N-(3-метилтио-5-ацетамидо-1,2,4-тиадиазолил)цитизин может формировать кристаллосольваты 1 - 6.
В данной работе в кристаллохимическом аспекте представляло интерес изучение влияния температуры и эффекта среды на формирование кристаллов, изучение стереохимии и конформационных особенностей пространственного строения молекул в кристалле, изучение на наличие явлений сольватообразования.
|
|
|
|
|
1 |
2 |
3 |
|
|
|
|
|
4 |
5 |
6 |
2.2 КРИСТАЛЛОСОЛЬВАТЫ N-(3-МЕТИЛТИО-5-АЦЕТАМИДО-1,2,4-ТИАДИАЗОЛИЛ)ЦИТИЗИНА
Результаты РСА показали, что в кристаллах 1, 2,
3, 4, 5 и 6 содержатся молекулы кристаллизационной воды, хлороформа, метанола,
бензола, пиридина и диоксана соответственно, т.е. при кристаллизации происходит
явление включения. Если, в кристаллах 1, 2 и 3 сольватные (гостевые) молекулы
включаются в соотношении 1:1, то в 4, 5 и 6 молекулы растворителя содержатся в
соотношении 2:1 (в независимой части элементарной ячейки имеются две молекулы N-(3-метилтио-5-ацетамидо-1,2,4-тиадиазолил)цитизина
(4а и 4b; 5а и 5b;
6а и 6b;) и одна молекула
сольвата). Хотя, кристаллы, выращенные из водных метанола, этанола и ацетона
растут в виде гидратов (1), которые устойчивы в атмосфере.
(1)
•
СНСl3
(2)
•
СН3OH
(3)
•
0.5С6Н6
(4)
•
0.5С5Н5N
(5)
•
0.5С4Н8O2
(6)
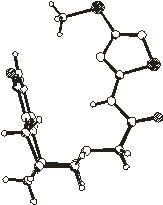
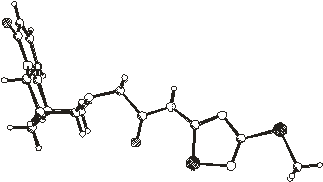
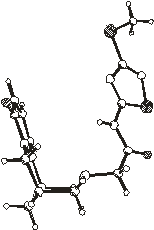
Строение молекулы N-(3-метилтио-5-ацетамидо-1,2,4-тиадиазолил)цитизина
в кристаллах 1 - 6 приблизительно в одинаковой проекции (перпендикулярной
плоскости четырех атомов С7, С9, С11, С13) показано на рис.2.1. Относительно
жесткое цитизиновое ядро в этих 1 - 6 структурах конформационно не
различается
и
практически не отличается от найденного для самого цитизина и в его разных
производных по атому N12.
, 3 2
а, 5a, 6a 4b, 5b, 6b
Рис.2.1. Пространственное строение
молекул в кристаллах 1 - 6
Громоздкий N-(3-метилтио-5-ацетамидо-1,2,4-тиадиазолил)ный
фрагмент (атомы N12-…-С18) во всех (1 - 6) независимо
найденных молекулах практически плоский с точностью ±0.016 (1), ±0.013 (2), ±0.058 (3), ±0.054 (4а), ±0.095 (4b) Å, ±0.106 (5а), ±0.139 (5b), ±0.096 (6а), ±0.137 (6b) Å. В этом
фрагменте (син-, анти-) расположение карбонильной и S-CH3 групп
относительно пятичленного кольца в молекулах 1, 3, 4а, 4b, 5a, 5b, 6a и 6b идентичны,
а в 2 S-CH3 группа
перевернута приблизительно на 180º относительно тиазолильного
кольца по сравнению предыдущими структурами, хотя лежит в плоскости этого
кольца (табл.2.1). В этом фрагменте карбонильная группа и атом S1
тиазолильного кольца взаимно син-расположены. В этих структурах не
зафиксировано образование инвертомеров (рассматриваемые как Z и
Е-изомеры), которые могут возникать из-за заторможенного вращения вокруг C15-N2 связи.
Таблица 2.1.
Торсионные углы вокруг связей -N12-C14-, -C14-C15- и -C17-S2-,
характеризующие конформацию молекул в структурах 1 - 6
Структура
С11-N12-C14-C15
N12-C14-C15-N2
N4-C17-S2-C18
1
-171.5
-167.6
3.7
2
-141.5
-0.7
178.1
3
-160.9
-174.6
0.8
4a
64.9
176.2
-0.4
4b
-161.7
44.8
-4.5
5a
64.6
177.3
-1.2
5b
-161.3
43.6
-4.9
6a
69.4
168.0
-3.3
6b
-162.9
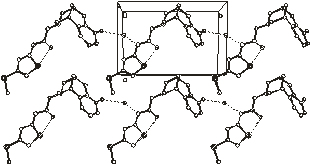
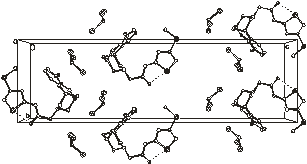
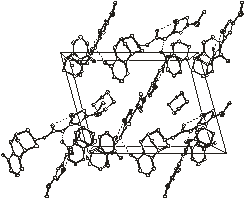
34.1 Упаковка молекул в кристаллосольватах 1 - 6
показана на рис.2.2.
В кристалле 1 обнаруживается межмолекулярная
Н-связь с участием молекулы воды по схеме: >N2-H…Ow-H…O1=.
Молекулы N-(3-метилтио-5-ацетамидо-1,2,4-тиадиазолил)цитизина,
преобразованные винтовыми осями 21 посредством кристаллизационной
молекулы воды, образуют бесконечную цепь вдоль оси b.
Параметры Н-связи N2-H…Ow
следующие: расстояния N2…Ow
2.780 Å и Н…Оw
2.02 Å, а угол N2-H…Ow
равен 147º. Для следующей
Н-связи (Ow-H…O1)
эти параметры соответственно равны: расстояния Ow…O1
2.720 Å и H…O1
1.87 Å, а угол Ow-H…O1
равен 162º. Также в
кристаллической структуре 1 наблюдается внутримолекулярное короткое
взаимодействие между карбонильным кислородом (О2) и серой (S1)
тиазолильного кольца (2.570 Å).
1
2
2
3 4
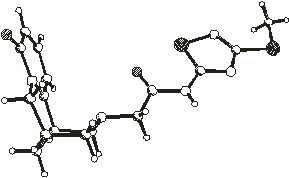
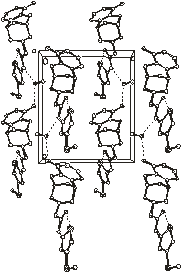
Рис.2.2. Упаковка молекул в
кристаллических структурах 1 - 4
В кристалле 2 сольватная молекула
хлороформа располагается в пустотах упаковки молекулы «хозяина» и также
находится на расстоянии Ван-дер-ваальсовых взаимодействий от окружающих ее
молекул (рис.2.2). Причиной этому возможно является более «складывающаяся»
конформация молекулы. Также в кристаллической структуре 2 наблюдается
внутримолекулярное короткое взаимодействие между карбонильным кислородом (О2) и
серой (S1)
тиазолильного кольца (2.661 Å).
Аналогичную с структурой 1,
водородную связь образует в кристалле 3 сольватная молекула метанола, где также
обнаруживается межмолекулярная Н-связь с участием молекулы метанола по схеме: >N2-H…Oм-Н…О1=. В
кристалле молекулы N-(3-метилтио-5-ацетамидо-1,2,4-тиадиазолил)цитизина,
транслированные вдоль оси b через сольватную молекулу
метанола, образуют бесконечную цепь (рис.2.2). Параметры Н-связи N2-H…Oм следующие:
расстояния N2…Oм 2.720 Å и Н…Ом 1.97 Å, а угол N2-H…Oм равен 167º. Для другой
Oм-H…O1 Н-связи
эти параметры соответственно равны 2.690, 1.96 и 167º. Также в
кристаллической структуре 3 наблюдается внутримолекулярное короткое
взаимодействие между карбонильным кислородом (О2) и серой (S1)
тиазолильного кольца (2.603 Å).
В кристалле 4, как и в 1, 3 атомы N2 и О1 двух
независимых молекул участвуют в образовании межмолекулярной Н-связи. Кроме
того, наблюдается межмолекулярное короткое взаимодействие S…S (расстояние
S1b…S2b (1-x, -0.5+y, 1-z) 3.650 Å короче суммы
Ван-дер-ваальсовых радиусов). Две независимо найденные молекулы производного
цитизина связаны Н-связью N2b-H2b…О1a и N2a-H2a…O1b при
преобразовании симметрией трансляции. Параметры этой связи соответственно
следующие: 2.830, 2.10, 143º и 2.730, 1.89 164º. Также в
кристаллической структуре 4 наблюдается внутримолекулярное короткое
взаимодействие между карбонильным кислородом (О2) и серой (S1)
тиазолильного кольца (2.704
Å и
2.641 Å
для
O2a-S1a и O2b-S1b
соответственно). Эти межмолекулярные контакты в кристалле образуют трехмерный
каркас. Сольватная молекула бензола в кристалле расположена в пустотах этого
каркаса (упаковки) и находится на расстоянии Ван-дер-ваальсовых взаимодействий
окружающих его молекул.
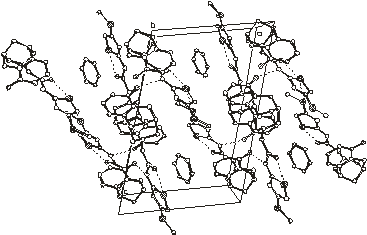
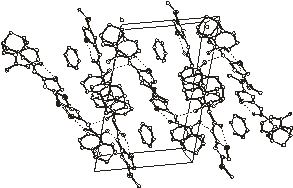
6
Рис.2.3. Упаковка молекул в кристаллических
структурах 5 и 6
Упаковка молекул в
кристаллосольватах 5 и 6 показана на рис.2.3. В асимметрической части
кристаллических упаковок 5 и 6 находятся две молекулы N-(3-метилтио-5-ацетамидо-1,2,4-тиадиазолил)цитизина
(хозяина) и одна молекула растворителя (гостя).
В кристалле 5 анализ упаковки
показывает наличие межмолекулярных взаимодействий между конформационно
различными молекулами хозяина по схеме N-H…O=С,
благодаря которым образуется бесконечная лента вдоль оси b, состоящая
из последовательно расположенных молекул a и b. Параметры
этих взаимодействий следующие: расстояния N2a…O1b 2.710 Å и H2a…O1b 1.93 Å, угол N2a-H2a…O1b равен 171º, а также
расстояния N2b…O1a 2.830 и H2b…O1a 2.10 Å, угол N2b-H2b…O1a равен 143º. Также в
кристаллической структуре 5 наблюдается внутримолекулярное короткое
взаимодействие между карбонильным кислородом (О2) и серой (S1)
тиазолильного кольца (2.693 Å и 2.625 Å для O2a-S1a и O2b-S1b
соответственно).
В структуре 6 анализ упаковки также
показывает наличие межмолекулярных взаимодействий между конформационно
различными молекулами хозяина по аналогичной схеме, наблюдаемой в 5. Параметры
этих взаимодействий следующие: расстояния N2a…O1b 2.720 Å и H2a…O1b 1.71 Å, угол N2a-H2a…O1b равен 165º, а также
расстояния N2b…O1a 2.850 и H2b…O1a 2.20 Å, угол N2b-H2b…O1a равен 142º. Также в
кристаллической структуре 6 наблюдается внутримолекулярное короткое
взаимодействие между карбонильным кислородом (О2) и серой (S1)
тиазолильного кольца (2.713 Å и 2.615 Å для O2a-S1a и O2b-S1b соответственно).
Сравнение вышеуказанных параметров
для кристаллических структур 4, 5 и 6 подтверждает их изоструктурность.
В этих структурах не зафиксировано
образование инвертомеров, которые могут возникать из-за заторможенного вращения
вокруг -N2-C15-связи.
Таким образом, анализ
пространственного строения N-(3-метилтио-5-ацетамидо-1,2,4-тиадиазолил)цитизина
в структурах 1 - 6 показывает, что в кристалле наблюдается 4 конформера,
различающихся расположением тиадиазолилного фрагмента относительно цитизинового
ядра. Следовательно, конформерия
вокруг N12-C14 и C14-C15 связей N-(3-метилтио-5-ацетамидо-1,2,4-тиадиазолил)ного
заместителя возможно способствует образованию разных кристаллосольватов N-(3-метилтио-5-ацетамидо-1,2,4-тиадиазолил)цитизина
в зависимости условий кристаллизации (от среды).
ГЛАВА 3. ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
.1 ПОЛУЧЕНИЕ МОНОКРИСТАЛЛОВ
ИЗУЧЕННЫХ ВЕЩЕСТВ
Монокристаллы сольватов N-(3-метилтио-5-ацетамидо-1,2,4-тиадиазолил)цитизина,
подходящие для РСА были выращены из водного раствора этанола, предварительно
абсолютизированных растворов хлороформа, метанола, бензола, пиридина и диоксана
путем медленного испарения при комнатной температуре (исключения составляют
только монокристаллы сольвата N-(3-метилтио-5-ацетамидо-1,2,4-тиадиазолил)
цитизина с пиридином, выращенные в холодильнике (-3ºC)). При этом
было замечено, что при использовании водного раствора метанола или других
водных органических растворов также предпочтительно включались молекулы воды и
образовывались гидраты.
.2 ОПРЕДЕЛЕНИЕ КРИСТАЛЛОГРАФИЧЕСКИХ
ПАРАМЕТРОВ И СБОР ЭКСПЕРИМЕНТАЛЬНЫХ ДАННЫХ
Монокристаллы для проведения РСА
предварительно отбирались с помощью микроскопа МБС-9, нестабильные были покрыты
оболочкой эпоксидной смолы. Далее трехмерный набор отражений отобранного
монокристалла получен на соответствующем дифрактометре.
Дифракционные данные соединений были
получены на дифрактометре Stoe Stadi-4
(графитовый монохроматор). Трехмерный набор отражений для этих кристаллов
получен на том же дифрактометре w/2q-методом сканирования, для
монокристаллов с использованием MoKα-излучения.
Сбор данных дифрактометром STOE
осуществляется под управлением программы STADI-4,
работающей в среде операционной системы WINDOWS. Для
повышения точности эксперимента проведенном на дифрактометре Stoe Stadi-4
вводилась поправка на поглощение методом Psi scan. Далее полученные наборы
отражений обрабатывались с помощью программы XRED. Она
применяет следующую корректуру на измеренную интенсивность: фактор поляризации
Лоренца, масштабирование относительно стандартных отражений, сферическая,
эмпирическая или числовая корректировка на поглощения.
Стандартные стадии типичного
рентгеноструктурного эксперимента, проведенные нами на дифрактометре Stoe Stadi-4,
заключались в следующем:
установление гониометрической
головки и центрирование кристалла в четырёхкружном дифрактометре.
определение параметров элементарной
ячейки и типа решетки Браве.
уточнение и центрирование матрицы
ориентации - расположения осей кристалла по отношению гониометра
четырехкружного дифрактометра.
ввод стандартных отражений (обычно
используются 3 осевых отражения) и сбор данных - интенсивностей отражений с H K L.
Сбор данных осуществляется
автоматически, дифрактометр ежечасно проверяет контрольные отражения. В случае
изменения их интенсивности более чем на 10% или после 8 часов сбора данных
дифрактометр автоматически заново уточняет матрицу ориентации.
.3 РАСШИФРОВКА И УТОЧНЕНИЕ СТРУКТУР
В настоящее время используется
большое количество программ для расшифровки и уточнения кристаллической структуры.
Нами использованы для расшифровки структур широко распространенная программа
SHELXS-97 и модели
структур уточнялись методом наименьших квадратов (МНК) по программе SHELXL-97.
Комплексная программа SHELX была создана 1970 году в
Кембриджском Университете, для расшифровки и уточнения низкомолекулярных
структур и была распространена в марте 1972 года. После компиляции программы
для IBM 370 было
создана версия SHELX-76. В связи с появлением все более
мощных компьютеров и совершенствованием техники эксперимента,
совершенствовалась, и программа SHELX и стало возможным применение
этой программы даже для уточнения макромолекул (белковых молекул). Программа
применяет прямой расчет структурных факторов, не обращаясь к суммированию на
основе алгоритма быстрого преобразования Фурье, и поэтому работает гораздо
медленнее, чем специально разработанные для уточнения макромолекул программы.
Но это компенсируется более высокой точностью и универсальностью и в некоторой
степени лучшей сходимостью, что в конечном счете уменьшает объем необходимого
ручного вмешательства в процесс построения модели. Большим достоинством
программы является простота ее использования, интуитивный интерфейс и
возможность применения практически на любых типах компьютеров. На сегодняшний
день программа SHELX распространяется бесплатно для
академических институтов и университетов в версиях для различных популярных
операционных систем.
Исследованные нами кристаллические
структуры определены прямыми методами по программе SHELXS-97 и
уточнялись МНК в последовательно полноматричном изотропно-анизотропном
приближении по программе SHELXL-97 для неводородных атомов. Атомы, не найденные
в исходном Фурье-синтезе, были локализованы из серии последовательных
разностных синтезов электронной плотности. После локализации всех неводородных
атомов проведены уточнения структуры МНК. Стандартным показателем точности
определения структуры служил R-фактор:
гдеR
- фактор расходимости;
Fнаб -
наблюдаемые амплитуды структурных факторов, т.е. таких факторов, которые
получаются на основе экспериментальных измерений интенсивности дифрагированного
пучка;
Fвыч -
амплитуды, рассчитанные на основе постулированной пробной структуры;
hkl - индексы
отражения от ряда параллельных плоскостей, а также
координаты точки обратной решетки.
Все атомы водорода в структурах были выявлены
объективно из разностного синтеза электронной плотности и включены в уточнение
с изотропными тепловыми параметрами.
Материалы рентгеноструктурного
анализа (параметры ячеек, координаты атомов, длины связи и валентные углы) в
виде CIF файла депонированы в КБСД (табл.3.1), которые можно получить по
веб-линку: www.ccdc.cam.ac.uk/data_request/cif.
Таблица 3.1.
Основные кристаллографические параметры
рентгеноструктурного эксперимента исследованного структуры.
Структура
1
2
3
4
5
6
Молекулярная
формула
C16H19N5O2S2 ·H2O
C16H19N5O2S2 ·СHCl3
C16H19N5O2S2 ·СH3OН
2(C16H19N5O2S2)·C6H6
2(C16H19N5O2S2)·C5H5N
2(C16H19N5O2S2)·C4H8O2
Mr/гмол-1
395.50
496.85
409.52
833.11
834.06
843.07
Сингония
Моноклинная
Ромбическая Моноклинная
Моноклинная
Моноклинная
Пространственная
группа
P 21
P212121
P21
P 21
P 21
P 21
Z
2
4
2
2
2
2
a, Å
8.003(5)
7.25(2)
8.211(2)
11.130(7)
11.060(6)
11.978(10)
b, Å
11.847(7)
9.51(1)
11.994(7)
11.448(9)
11.427(7)
11.389(9)
c, Å
9.867(5)
32.28(5)
10.272(6)
16.747(9)
16.581(7)
16.025(7)
β
99.52(5)
92.64(4)
105.30(5)
105.61(3)
105.59(5)
V, Å3
921.9(9)
2227.5(8)
1010.6(8)
2058(2)
2018.3(19)
2105.7(3)
r,
г/см3
1.425
1.482
1.345
1.344
1.372
1.330
Размеры
кристалла (мм)
1.00х0.75x0.75
0.80х0.30x0.15
1.00х0.75x0.72
1.00х0.50x0.30
0.50х0.25х0.25
0.50х0.25x0.10
Область
сканирования 2q
2.0£q£25º
2.23£q£25º
1.50£q£27.5º
1.50£q£26.00º 1.77£q£26º
mexp
(см-1)
0.32
0.62
0.29
0.28
0.29
0.28
Число
отражений
1672
2220
2438
4259
4195
4365
Число
отражений с I>2s(I)
1568
1297
2212
3478
2536
2155
R1 (I>2s(I)
и общее)
0.0301 (0.0343)
0.0977 (0.1692)
0.0315 (0.0377)
0.0449
(0.0635)
0.0777 (0.1489)
0.0967(0.2109)
wR2
0.0657 (0.0685)
0.2264 (0.2810)
0.0766 (0.0818)
0.0896
(0.1040)
0.1005 (0.1256)
0.1080(0.1410)
S
1.14
1.10
1.12
1.16
1.22
1.23
Разностные
пики элек-тронной плотности (e.Å-3)
0.17 и -0.15
0.35 и -0.34
0.17 и -0.15
0.18 и
-0.21
0.23 и
-0.23
0.26 и
-0.22
CCDC
652423
652422
652424
652425
706492
706491
REFCODE
IFILIT
IFILEP
IFILOZ
IFILUF
LAJDAD
LAJCUW
ЗАКЛЮЧЕНИЕ
1. Определены методом РСА 6 новых
кристаллических структур N12
производных цитизина. В исследованных структурах выявлены геометрические
характеристики молекул и природа внутри- и межмолекулярных взаимодействий.
2. Установлено, что N-(3-метилтио-5-ацетамидо-1,2,4-тиадиазолил)цитизины
могут образовывать различные сольваты в зависимости от среды кристаллизации -
являются клатратогенами.
. Установлено, что в исследованных
кристаллосольватах N-(3-метилтио-5-ацетамидо-1,2,4-тиадиазолил)цитизинов
молекулы растворителя расположены в замкнутых пустотах «криптатного» типа.
. Выявлено, что в изученных
кристаллических структурах сольватов N-(3-метилтио-5-ацетамидо-1,2,4-тиадиазолил)цитизинов
молекула хозяина принимает только четыре конформации, различающиеся
расположением тиадиазолильного фрагмента относительно цитизинового ядра.
СПИСОК ИСПОЛЬЗОВАННОЙ ЛИТЕРАТУРЫ . Хакимова
Т.В., Пухлякова О.А., Шавалеева Г.А., Фатыхов А.А., Васильева Е.В., Спирихин
Л.В.. Синтез и стереохимия новых N-замещенных
производных цитизина // Хим. природ. соедин. -Ташкент, 2001. -№ 4. -С. 301-305.
. Краснов
K.A.,
Карцев В.Г., Горовой A.С.,
Хрусталев В.Н. Химическая модификация растительных алкалоидов III.
Исследование пространственного строения
1,3-диметил-5-арилметил-5-цитизилметилбарбитуровых кислот методами РСА и ЯМР //
Хим. природ. соедин. -Ташкент, 2002. -№ 5. -С. 367-373.
. Palin
D.E., Powell H.M. The structure of molecular compounds. Part III. Crystal
structure of addition complexes of quinol with certain volatile compounds // J.
Chem. Soc. -Cambridge, 1947. -P. 208-221.
5. Powell
H.M. The structure of molecular compounds. Part IV. Crystal structure of
addition complexes of quinon with certain volatile compounds // J. Chem. Soc.
-Cambridge, 1948. -P. 61-69.
6. Schlenk
H., Holman R.T. Urea and thiourea adductions of C5-C42-hydrocarbins // J. Amer.
Chem. Soc. -Washington, 1952. -V.
74. -P.
1720-1723.
7. Schlenk
H., Holman R.T. The urea complexes of unsaturated fat acids // Science.
-Washington, 1950. -V. 112. -P. 19-20.
8. Clapp
L.B. The chemistry of the coordination compounds. -New York: Reinhold
Publishing Corp., 1956. -35 p.
9. Ketelaar
J.A. Chemical constitution. -New York: Elsevier Pub. Co., 1958, -363 p.
10. Cramer
F., Dietche W. Ocdusion compounds. XV. Resolution of racemates with
cyclodextrins // Ber. -Weinheim, 1959. -V.92. -P.378-384.
11. Haleblian
J.K. Characterization of habits and crystalline modification of solids and
their pharmaceutical applications // J. Pharm. Sci. -Malden,
1975. -V.64.
-P.
1269-1288.
12. Китайгородский
А.И. Молекулярные кристаллы. -М.: Наука, 1971. -424 с.
. Китайгородский
А.И. Смешанные кристаллы. -М.: Наука, 1983. -277 с.
14. Belosludov
V.R., Lavrentiev M.Yu., Dyadin Yu.A. Theory of Clathrates
<http://www.springerlink.com/content/n04222wk1687w60k/?p=ea3c21635af4457fb826419091a4b6a3&pi=0>
// J. Inclus. Phenom. -Amsterdam,
1991. -V.
10. -P.
399-422.
15. Никитин
Б.А. Избранные труды. Исследования по химии благородных газов. -М.:
Издательство АН СССР, 1956. -104 с.
. Powell
H.M. The structure of molecular compounds. Part IV. Clathrate compounds // J.
Chem. Soc. -Cambridge, 1948. -P. 61-73.
17. Дядин
Ю.А., Терехова И.С., Родионова Т.В., Солдатов Д.В. Полвека клатратной химии //
Журн. структур. химии. -Новосибирск, 1999. -Т. 40, -№ 5. -С. 797-808.
. Breck
D.H. Zeolite Molecular Sieves: Structure, Chemistry and Use. -New York: Wiley,
1974. -771 p.
19. MacNicol
D.D., McKendrick J.J., Wilson D.R. Clathrates and molecular inclusion phenomena
// Chem. Soc. Rev. -Cambridge,
1978. -V.
7. -P.
65-87.
20. Гойхман
А.Ш., Соломко В.П. Высокомолекулярные соединения включения. -Киев: Наукова
думка, 1982. -531 с.
. Davies
J.E.D., Kemula W., Powell H.M., Smith N.O. Inclusion compounds -Past, present,
and future
<http://www.springerlink.com/content/t356272wt8110x71/?p=6ecd1adf64b14604991d852f5b21d95f&pi=1>
// J. Inclus. Phenom.
-Amsterdam,
1983. -V.
1. -P. 3-44.
22. Weber
E., Josel H.-P. A proposal for the classification and nomenclature of
host-guest-type compounds // J. Inclus. Phenom. -Amsterdam,
1983. -V.
1. -P.
79-85.
23. Дядин
Ю.А., Удачин К.А., Бондарюк И.В. Соединения включения. -Новосибирск: НГУ, 1988.
-92 с.
. Georges
Tsoucaris, Jerry L. Atwood and Janusz Lipkowsky. Crystallography of
Supramolecular Compounds. NATO ASI Series, Series C: Mathematical and Physical
Sciences. -Dordrecht, Kluwer Academic Publishers, 1996. -520 p.
25. Pedersen
C.J. Cyclic polyethers and their complexes with metal salts
<http://pubs.acs.org/doi/abs/10.1021/ja00986a052> // J. Amer. Chem. Soc. -Washington,
1967. -V.
89. -P.
2495-2496.
26. Pedersen
C.J. Cyclic polyethers and their complexes with metal salts
<http://pubs.acs.org/doi/abs/10.1021/ja01002a035> // J.
Amer. Chem.
Soc. -Washington,
1967. -V.
89. -P.
7017-7036.
27. Pedersen
C.J. The discovery of crown ethers
<http://www.springerlink.com/content/p8k87751712jl727/?p=89a1e60ab9454899aa5a032c50c331e3&pi=0>
// J. Inclus. Phenom. -Amsterdam,
1988. -V.
6. -P.
337-350.
28. Lehn
J.-M. Cryptates: inclusion complexes of macropolycyclic receptor molecules //
Pure Appl. Chem. -Research
Triangle Park, 1978. -V.
50. -P.
871-892.
29. Lehn
J.-M. Supramolecular chemistry - Scope and perspectives: Molecules -
Supermolecules - Molecular devices // J. Inclus. Phenom. -Amsterdam,
1988. -V.
6. -P.
351-396.
30. Cram
D.J. The design of molecular hosts, guests, and their complexes
<http://www.springerlink.com/content/nh0512537010u206/?p=904d9f07d2c449749aca49f9265f026a&pi=2>
// J. Inclus. Phenom. -Amsterdam, 1988. -V. 6. -P. 397-413.
31. Lehn
J.-M. Supramolecular Chemistry: Concepts and Perspectives. -Weinheim: VCH,
1995. -340 p.
32. Лен
Ж.-М. Супрамолекулярная химия: Концепции и перспективы. -Новосибирск: Наука,
1998. -334 с.
. Lindoy
L.F. The Chemistry of Macrocyclic Ligand Complexes. -Cambridge: Cambridge
University Press, 1989. -288 p.
34. Костромина
Н.А., Волошин Я.З., Назаренко А.Ю. Клатрохелаты: синтез, строение, свойства.
-Киев: Наукова думка, 1992. -233 с.
. Gerbeleu
N.V., Arion V.B., Burgess J. Template Synthesis of Macrocyclic Compounds.
-Weinheim: Wiley-VCH, 1999. -576 p.
36. Vicens
J., Böhmer V. Calixarenes: A Versatile Class of Macrocyclic
Compounds. -Dordrecht: Kluwer Academic Publishers, 1991. -263 p.
37. Szejtli
J. Cyclodextrin Technology. -Dordrecht: Kluwer Academic Publishers, 1988. -450
p.
38. Hedges
A.R. Industrial Applications of Cyclodextrins
<http://pubs.acs.org/doi/abs/10.1021/cr970014w> // Chem. Rev. -Washington,
1998. -V.
98. -P.
2035-2044.
39. Uekama
K., Hirayama F., Irie T. Cyclodextrin Drug Carrier Systems
<http://pubs.acs.org/doi/abs/10.1021/cr970025p> // Chem. Rev. -Washington,
1998. -V.
98. -P.
2045-2076.
40. Hashimoto
H. Present Status of Industrial Application of Cyclodextrins in Japan
<http://www.springerlink.com/content/j768830x6335gnp2/?p=dca1d7b0ae404bbc87a660d366ebfdf5&pi=11>
// J. Inclus. Phenom. -Amsterdam,
2002. -V.
44. -P.
57-62.
41. McCrone
W.C. Polymorphism. In Physics and chemistry of the organic solid state. In 2
volumes. -New
York: Wiley Interscience, 1965. -V. 2. -P.
725-767.
42. Haleblian
J., McCrone W.C. Pharmaceutical applications of polymorphism // J. Pharm. Sci. -Malden,
1969. -V.
58. -P.
911-929.
43. David
R., Giron D. Crystallization / Handbook of Powder Technology. -Amsterdam, 1994.
-V. 9. -P. 193-241.
44. Henck
J.-O., Griesser U.J., Burger A. Polymorphism of drug substances. An economic
challenge? // Die Pharmazeutische Industrie. -Aulendorf,
1997. -V.
59. -P.
165-169.
45. Byrn
S.R. Solid state chemistry of drugs. -New York: Academic Press, 1982. -pp.
7-10.
46. Byrn
S.R., Pfeiffer R.R., Stowell J.G. Solid state chemistry of drugs. -West
Lafayette: SSCI, Inc, 1999. -pp. 17-41.
47. Van
Der Sluis P., Kroon J. Solvents and X-ray crystallography // J. Cryst. Growth.
-Amsterdam, 1989. -V. 97. -P. 645-656.
48. Threlfall
T. Analysis of organic polymorphs // Analyst. -Cambridge, 1995. -V. 120. -P.
2435-2460.
49. Kitamura
S., Chang L.C., Guillory J.K. Polymorphism of mefloquine hydrochloride // Int.
J. Pharm. -Amsterdam, 1994. -V. 101. -P. 127-144.
50. Nguyen
N.A.T., Ghosh S., Gatlin D.J.W. Physicochemical characterization of the various
solid forms of carbovir, an antiviral nucleoside // J. Pharm. Sci. -Malden,
1994. -V. 83. -P. 1116-1123.
51. Kiaoka
H., Ohya K. Pseudopolymorphism and phase stability of
7-piperidino-1,2,3,5-tetrahydroimidazo-[2,1-b]quinazoline-2-one
(DN-9693) // J. Therm. Anal. Calorim. -Amsterdam, 1995. -V. 44. -P. 1047-1056.
52. Brittain
H.G., Ranadive S.A., Serajuddin A.T.M. Effect of humidity-dependent changes in
crystal structure on the solid-state fluorescene properties of a new HMG-COA
reductase inhibitor // Pharm. Res. -Amsterdam, 1995. -V. 12. -P. 556-559.
53. Kitaoka
H., Wada C., Moroi R., Hakusui H. Effects of dehydration on the formation of
levofloxacin pseudopolymorphs // Chem. Pharm. Bull. -Tokyo, 1995. -V. 43. -P.
649-653.
54. Caira
M. R., Peinaar E.W., Lotter A.P. Polimorphism and pseudopolymorphism of the
antibacterial snitrofurantoin // Mol. Cryst. Liq. Cryst., Sci. Technol. A.
-Philadelphia, 1996. -V. 278. -P. 241-264.
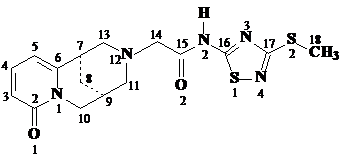 • H2O
• H2O
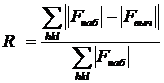 (3.1)
(3.1)