Материал: Инфракрасная спектроскопия и ее практическое применение в фармацевтическом анализе
Общая конструкция ИК-спектрометра включает: источник излучения,
диспергирующую систему (монохроматор) и регистрирующий элемент (детектор).
Специфика ИК-излучения приводит к особенностям в устройстве каждого элемента.
Область спектра
ν, см-1
λ, мкм
Применение
Ближняя
12500-4000
0,8-2,5
Качественный и количественный анализ на Н-содержащие
функциональные группы, множество сорбентов основных частот из средней
ИК-области.
Средняя
4000-625
2,5-16,7
Колебательная или основная ИК-область. Типичные линии
поглощения функциональных групп, главным образом в диапазоне 1400-4000 см-1,
а диапазон 600-1400 называют область "отпечатков пальцев".
Дальняя
625-30
16,7-330
Область колебаний с малой энергией, в особенности у
неорганических и металлорганических соединений. Исследование скелетных и крутильных
колебаний, а также колебаний решетки твердых тел.
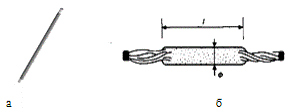
Источник излучения в ИК-спектрометре должны перекрывать большой интервал
длин волн. Из них наиболее распространены стержни из карбида кремния (глобар)
или из оксидов редкоземельных элементов (штифт Нернста), нагреваемые током до
1500 и 800 С. Кривая интенсивности излучения этих источников имеет вид кривой
излучения абсолютно черного тела. Они дают мощное ИК-излучение, но
преимущественно в ближней ИК-области и быстро падающее с увеличением длины волны
(это изменение мощности компенсируется программированным раскрытием входной
щели прибора). В длинноволновой части ИК-спектра применяют ртутно-кварцевые
лампы высокого давления.
Рис. 12. Стержень из карбида кремния (а) (глобар) и Штифт Нернст
Рис. 13. Ртутно-кварцевые лампы высокого давления
В монохроматоре диспергирующими элементами могут служить призмы в
ИК-области материалов с подходящей дисперсией или дифракционные решетки. Призмы
из стекла или кварца неприменимы, поскольку не пропускают ИК-излучение, и
обычно используют призмы, изготовленные из некоторых солей. От призм требуется
достаточно большая диспергирующая способность, но она падает с уменьшением
длины волны. Так призма из NaCl обеспечивает точность около 2 см-1 в
области 650 см-1 и около 30 см-1 в области 3000 см-1.
Поэтому обычно используют 3-4 сменных призмы из монокристаллов LiF, NaCl, KBr.
Дисперсия материала призмы обычно сильно меняется с температурой, поэтому необходимо
термостатирование прибора. Солевую оптику следует беречь от повышенной
влажности.
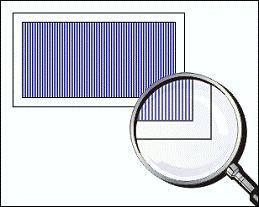
В настоящее время все чаще в качестве диспергирующих элементов применяют
дифракционные решетки. У них больше дисперсия, которая мало зависит от длины
волны и почти не зависит от температуры, но решетки могут давать наложение
спектров высших порядков, что требует использования в приборе хороших
спектральных фильтров.
Рис. 14. Дифракционная решетка
Детектирование ИК-излучения основано преимущественно на тепловом его
действии. Для средней ИК-области в качестве приемников излучения применяют
чувствительные термопары (термостолбики) и термометры сопротивления
(болометры), покрытые чернью. Используют также пневматические приемники (ячейка
Голея), в которых газ в зачерненной камере с гибкой стенкой меняет давление под
действием излучения. В длинноволновой области применяют также другую группу
приемников: фотонные приемники с фотопроводимостью.
Среди ИК-спектрометров наиболее распространены диспергирующие сканирующие
приборы, в которых спектры последовательно сканируются и регистрируются с
помощью одноканального приемника. По схеме освещения такие приборы бывают
однолучевыми и двулучевыми. В однолучевых спектрометрах для освещения щели используют
одно сферическое зеркало.
Теперь чаще используют двухлучевую систему, которая позволяет выравнивать
фон, то есть линию полного пропускания, и компенсировать как поглощение
атмосферными Н2О и СО2 так и ослабление пучков окнами
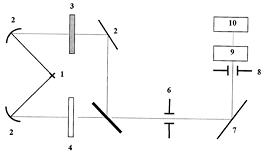
кюветы и растворителем. Упрощенная блок-схема двухлучевого сканирующего
ИК-спектрометра с дифракционной решеткой представлена на рис. 15.
Рис. 15. Схема инфракрасного двухлучевого спектрофотометра
ИК-излучение от источника 1 делится на два пучка системой зеркал 2.
Рабочий пучок проходит через кювету с образцом 3, а пучок сравнения - через
компенсатор фона 4. С помощью дискомодулятора 5 пучки попеременно направляются
на входную щель монохроматора 6 и через нее - на дифракционную решетку 7, которая
разлагает излучение в спектр и направляет его на выходную щель 8.
Монохроматическое изображение щели попадает на приемник - висмутовый болометр
9. В отсутствии исследуемого образца интенсивности рабочего пучка и пучка
сравнения одинаковы, в приемнике сигналы от этих пучков вычитаются; на выходе
сигнал отсутствует. При поглощении рабочего пучка исследуемым веществом на
приемник попадают лучи различной интенсивности, в результате чего в приемнике
возникает переменный сигнал. После усиления и преобразования сигнала приводится
в движение перо самописца 10. При медленном повороте решетки щель 8
последовательно вырезает узкие участки спектра, и на ленте самописца
вычерчивается кривая зависимости пропускания от длины волны.
Серийные одно- и двухлучевые спектрофотометры, используемые для изучения
низкомолекулярных соединений, имеют достаточную разрешающую способность для
исследования большинства полимеров. Однако для работы в дальней области
спектра, которая в исследовании полимеров играет очень важную роль, необходимы
специальные вакуумные спектрофотометры с дифракционными решетками.
Современные спектрометры позволяют регистрировать ИК-спектры
газообразных, жидких и твердых образцов. Для получения ИК-спектра полимера или
органического соединения необходимо всего от 1 до 10 мг вещества.
В большинстве случаев спектры соединений регистрируют либо в виде
растворов веществ в хлороформе, четыреххлористом углероде, сероуглероде, либо в
виде твердых прозрачных таблеток, полученных прессованием под давлением мелко
размолотой смеси вещества с бромидом калия. Иногда использую метод съемки
ИК-спектра вещества в виде мелко растертой суспензии в вазелиновом или
минеральном масле.
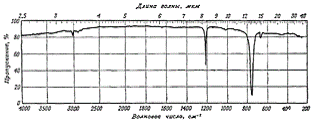
В случае регистрации ИК-спектра соединений в растворах или суспензиях
необходимо вычитать полосы поглощения растворителей или суспензионной среды
[19].
Рис. 16. ИК-спектр хлороформа
10. Специфические особенности фармацевтического анализа
Фармацевтический анализ - это наука о химической характеристике и
измерении биологически активных веществ на всех этапах производства: от
контроля сырья до оценки качества полученного ЛВ, изучения его стабильности,
установления сроков годности и стандартизации ЛФ. Фармацевтический анализ имеет
свои специфические особенности, отличающие его от других видов анализа. Эти
особенности заключаются в том, что анализу подвергают вещества различной
химической природы: неорганические, элементорганические, радиоактивные,
органические соединения от простых алифатических до сложных природных биологически
активных веществ. Чрезвычайно широк диапазон концентраций анализируемых
веществ. Объектами фармацевтического анализа являются не только индивидуальные
ЛВ (субстанции), но и смеси, содержащие различное число компонентов.
Способы фармацевтического анализа нуждаются в систематическом
совершенствовании в связи с созданием новых ЛС и непрерывным повышением
требований к их качеству. Причем растут требования как к степени чистоты ЛВ,
так и к количественному содержанию. Поэтому необходимо широкое использование
для оценки качества ЛС не только химических, но и более чувствительных
физико-химических методов.
К фармацевтическому анализу предъявляют высокие требования. Он должен
быть достаточно специфичен и чувствителен, точен по отношению к нормативам,
обусловленным ГФ, ФС и другой НД, выполняться в короткие промежутки времени с
использованием минимальных количеств испытуемых Л С и реактивов.
Фармацевтический анализ в зависимости от поставленных задач включает различные
формы контроля качества ЛС: фармакопейный анализ, постадийный контроль
производства ЛВ, анализ ЛФ индивидуального изготовления, экспресс- анализ в
условиях аптеки и биофармацевтический анализ.
Составной частью фармацевтического анализа является фармакопейный анализ.
Он представляет собой совокупность способов исследования ЛВ и ЛФ, изложенных в
Государственной фармакопее или другой нормативной документации. На основании
результатов, полученных при выполнении фармакопейного анализа, делается
заключение о соответствии ЛС требованиям ГФ (ФС, ФСП). При отклонении от этих
требований ЛС к применению не допускают [3].
Заключение о качестве ЛС можно сделать только на основании анализа пробы
(выборки). Порядок ее отбора указан либо в частной ФС, либо в общей статье ГФ
XI (вып. 2).
Выполнение фармакопейного анализа позволяет установить подлинность Л В,
его чистоту, определить количественное содержание фармакологически активного
вещества или ингредиентов, входящих в состав ЛФ. Несмотря на то что каждый из
этих этапов имеет свою конкретную цель, их нельзя рассматривать изолированно.
Они взаимосвязаны, взаимно дополняют друг друга и отражают комплексный характер
оценки качества ЛС. Так, например, температура плавления, растворимость, рН
среды водного раствора и т.д. являются критериями как подлинности, так и чистоты
ЛВ. Указанные особенности фармакопейного анализа существенно отличают его от
норм и требований к методам анализа, используемых в Государственных стандартах
(ГОСТ) и технических условиях (ТУ).
В ФС описаны методики соответствующих испытаний применительно к тому или
иному фармакопейному ЛС. Многие из этих методик идентичны. В целях унификации
способов анализа в ГФ включены общие фармакопейные статьи (ОФС), в которых
систематизированы сведения о выполнении испытаний на ряд ионов и функциональных
групп, а также единых методов количественного определения. Для обобщения
большого объема частных сведений по фармакопейному анализу будут рассмотрены
основные критерии фармацевтического анализа и общие принципы испытаний на
подлинность, чистоту и количественного определения ЛВ [18].
Для проверки качества препаратов испытательные центры или центры контроля
качества лекарственных средств (ЦККЛС) должны обладать необходимым арсеналом
аналитического оборудования. В статье даны рекомендации по выбору аппаратуры,
оцениваются сильные и слабые стороны представленных на рынке приборов и
лабораторных материалов, представлена основная номенклатура оборудования ЦККЛС.
Вопросы организации микробиологической лаборатории, оборудование для
испытания на бактериальные эндотоксины, организация деятельности ЦККЛС, система
менеджмента качества будут представлены в следующих публикациях.
Инфракрасная (ИК) спектроскопия в средней области (от 4000 до 400 см-1) в
настоящее время является методом номер один для установления подлинности
фармацевтических субстанций. Он может применяться и в отношении лекарственных
препаратов (т. е. дозированных лекарственных средств, готовых к применению),
однако современный фармакопейный анализ предполагает в таком случае
предварительное извлечение действующего вещества из лекарственной формы. (Есть
исследования, которые демонстрируют возможность прямого получения ИК-спектров
препаратов при относительно высоком содержании основного вещества в
препарате.)
Метод ИК-спектроскопии является фармакопейным. В Государственной
фармакопее (ГФ) XII (ч. 1, с. 62) имеется соответствующая общая фармакопейная
статья (ОФС) "Спектрометрия в инфракрасной области".
Современный ИК-спектрометр обычно работает по принципу преобразования
Фурье, т. е. использует интерферометр, что выгодно отличает его от
дисперсионных приборов.
Также следует отметить, что современный ИК-спектрометр - прибор с
большими возможностями, не все из которых требуются при проведении рутинного
контроля качества ЛС. Поэтому при приобретении такого прибора для ЦККЛС
необходимо выбирать набор приспособлений, приставок и программного обеспечения
к основному прибору, который будет реально востребован.
В подавляющем большинстве случаев для получения ИК-спектров используют
два способа:
• прессование таблеток с бромидом калия (основной вариант); Для получения таблеток необходимы:
• специальный пресс с пресс-формами и другими приспособлениями;
• спектроскопически чистый бромид калия (KBr для ИК-спектроскопии);
• соответствующие держатели в кюветном отделении прибора.
Для получения суспензии в вазелиновом масле необходимы:
• ступка, не содержащая пор (например, агатовая) с таким же пестиком
(поры накапливают влагу, попадания которой в образец необходимо избегать);
• спектроскопически чистое минеральное (вазелиновое) масло (масло для
ИК-спектроскопии);
• стекла из бромида калия или другого материала, прозрачного в рабочем
диапазоне ИК-спектра (суспензия помещается между стеклами);
• соответствующие держатели в кюветном отделении прибора. При получении
ИК-спектров жидких веществ могут подойти стекла из бромида калия, которые
используются и для сканирования спектров суспензий.
Естественно, что различные фирмы-производители конструктивно могут
реализовывать получение спектров разными способами, о чем необходимо
консультироваться, приобретая прибор.
Следует также учесть, что могут оказаться востребованными и другие
варианты пробоподготовки, предусмотренные ОФС. Их также следует обсудить с
поставщиком при покупке прибора [2].
Заключение
Инфракрасная спектроскопия с каждым годом получает всё более широкое
распространение как весьма ценный физический метод исследования строения
молекул и мощный аналитический метод.
Внедрение спектроскопии в сферу фармацевтического анализа ЛС послужило мощным
толчком для её развития и совершенствования. Благодаря многообразию
возможностей применения, высокой точности результатов и чувствительности
обнаружения, существенном сокращении времени проведения анализа,
ИК-спектроскопия достигла высшей степени экономической эффективности [5].
1. Аверко-Антонович И.Ю. , Бикмуллин Р.Т.: Методы
исследования структуры и свойств полимеров. Учебное пособие / КГТУ. Казань. -
2002. - 604 с.
. Арзамасцев А.П., Дорофеев В.Л. Современные требования
к Стандартизации и контролю качества лекарственных средств. // Новая аптека.
Эффективное управление. 2007 - №4- С. 54-57.
. Арзамасцев А.П., Дорофеев В.Л. Стандартные образцы
для фармакопейного анализа. // Вопросы биологической медицинской и фармацевтической
химии. 2010 - №5С. 6-10.
. Беллами JI. Инфракрасные спектры сложных молекул
М.:1983, 432 с.
. Бёккер Ю. Мир химии. Спектроскопия. Перевод с
немецкого Л.Н.Казанцевой. Москва -2009. - 522с.
. Бранд Дж. Применение спектроскопии в органической химии.
М.: Мир. - 1967. - 280 с.
. Государственная фармакопея Российской Федерации XII издания 2 часть, Москва 2010
. Кеслер Н, Методы инфракрасной спектроскопии в
химическом анализе. М.: Мир, 1984,-287 с.
. Коптюг В.А. Атлас спектров для криминалистических подразделений
МВД СССР. Выпуск 8. Новосибирск- 1991г. -477с.
. Крищенко В.П. Ближняя инфракрасная спектроскопия.
М.: 1997. -638с.
. Кросс А.Д. Введение в практическую инфракрасную
спектроскопию Пер с англ. М.: Иностранная литература, 1981. - 110 с.
. Крылов А. С., Втюрин А. Н., Герасимова Ю. В.
Обработка данных инфракрасной Фурье-спектроскопии. Методическое пособие.
Красноярск, Институт физики СО РАН, 2005. - 48 с.
. Купцов А.Х., Жижин Г.Н. Фурье-КР и фурье-ИК-спектры
полимеров. М.: Физматлит,- 2001. -316 с.
. Наканиси К. " Инфракрасные спектры и строение
органических соединений" М.: Мир,- 1965. -216с.
. Норрис К.Х. Приборы для ближней инфракрасной
спектроскопии // Применение спектроскопии в ближней инфракрасной области для
контроля качества продукции (4-й сборник научных трудов по ИКС). М.:
Интерагротех, 1989.-С. 5-10.
. Пентин Ю.А. , Л.В. Вилков: Физические методы
исследования в химии. - М.: Мир. - 2003. - 367 с.
. Садчикова Н.П., Арзамасцев А.П., Титова A.B. Метод
ближней ИК-спектроскопии в системе контроля качества лекарственных средств
(обзор) // Вопросы биологической медицинской и фармацевтической химии.
-2010.-№1. С. 16-20.
. Садчикова Н.П., Арзамасцев А.П., Титова A.B.
Современное состояние проблемы применения ИК-спектроскопии в фармацевтическом
анализе лекарственных средств // Хим.-фарм.ж. 2008. - №.8. - С. 26-30.
. Тарасов К.И., Спектральные приборы,
"Машиностроение", Л., 1968.
. Тарасевич Б.Н. Основы ИК спектроскопии с
преобразованием Фурье. Подготовка проб в ИК спектроскопии. Москва- 2012. -22с.
. Тарасевич Б.Н. ИК спектры основных классов
органических соединений. Справочные материалы. Москва -2012. -52с.
. Тарутина Л.И., Позднякова Ф.О. Спектральный анализ
полимеров. - Л.: Химия. - 1986. - 248 с.
. Сливкин А.И. Атлас ИК-спектров лекарственных веществ.
А.И. Сливкин, О.В. Тринеева, Е.Е. Логвинова, А.С. Чистякова, Л.Ю. Яковлев, И.И.
Механтьев. Издательско-полиграфический центр Воронежского государственного
университета- 2013.- 172с.

Список
использованной литературы