Материал: Грамположительные аэробные Кокки
16
|
стенки грамположительных бактерий |
Феромоны |
Сигнальные белковые молекулы, |
|
регулирующие плотность популяции |
|
(кворум-сенсинг) |
Бета-лактамаза |
Разрыв бета-лактамного кольца, |
|
инактивирование бета-лактамных |
|
антибиотиков |
4. Прочие факторы патогенности |
|
Стафилококковый ингибитор |
Ингибирование системы комплемента |
комплемента (SCIN) |
|
Протеин S. aureus, ингибирующий |
Ингибирование хемотаксиса |
хемотаксис (CHIPS) |
нейтрофилов |
Устойчивость к солям и жирным |
Размножение в потовых и сальных |
кислотам. |
железах |
Внеклеточные полисахариды |
Образование экзополисахаридной |
|
матрицы на слизистых оболочках или на |
|
плотных поверхностях (формирование |
|
биопленок) |
Капсула Клеточная стенка
Цитоплазматическая мембрана
MSCRAMM |
Токсины |
|
Экзоферменты
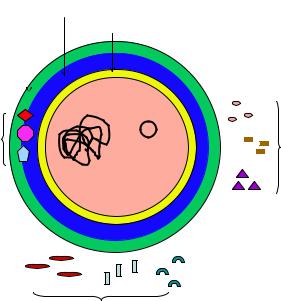
Рисунок 18 – Факторы патогенности стафилококков.
Факторы патогенности золотистого стафилококка детерминируются не только хромосомными генами, но и генами интегрированных профагов (9NM1, 9NM2, 9NM3, 9NM4) и автономных плазмид. Гены, определяющие патогенность стафилококков, сгруппированы в острова патогенности. Наиболее полный набор представленных факторов патогенности встречается у штаммов золотистого стафилококка. Штаммы других видов стафилококков могут иметь лишь некоторые факторы патогенности.
17
Факторы патогенности стафилококков по выполняемой функции можно подразделить на следующие группы:
1.Факторы, обеспечивающие адгезию стафилококков (клампинг-фактор, тейхоевые кислоты, капсула и др.).
2.Факторы, способствующие распространению стафилококков по тканям организма (гиалуронидаза, устойчивость к жирным кислотам).
3.Факторы с токсической функцией (токсины).
4.Факторы, препятствующие фагоцитозу (полисахаридная капсула, белок А).
5.Факторы, инактивирующие защитные системы организма (факторы с антилизоцимной, антиинтерфероновой, антикомплементарной, антикарнозиновой, антилактоферриновой, антигемоглобиновой активностями).
Микробные поверхностные компоненты, распознающие адгезивные матриксные молекулы (MSCRAMM), или адгезины взаимодействуют с различными рецепторами клеток макроорганизма (муцином слизистых оболочек, протеогликанами соединительной ткани и эндотелиоцитов), белками внеклеточного матрикса (коллагеном, фибронектином, ламинином и др.), сывороточными белками (витронектином, фибриногеном и др.).
Фибронектин-связывающие белки. Фибронектин присутствует в организме в виде фибриллярной сети на клеточной поверхности и во внеклеточном матриксе. Фибронектин-связывающие белки стафилококков способствуют как
адгезии бактерий на поверхности клеток, так и распространению их во внеклеточном пространстве.
Коллаген-связывающий белок экспрессируется некоторыми штаммами золотистого стафилококка, выступает фактором адгезии и играет важную роль в патогенезе остеомиелита и септического артрита.
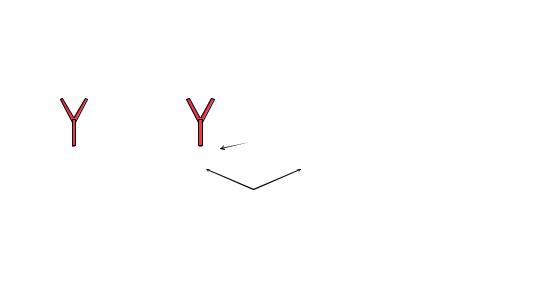
Белок А стафилококков располагается поверхностно, связан с пептидогликаном клеточной стенки бактерий, термолабилен, не разрушается трипсином. Белок А способен связываться с Fс-фрагментом IgG, образующийся при этом комплекс блокирует опсонизирующую активность антител и предотвращает поглощение бактерий фагоцитами (рисунок 19).
|
Способ связывания IgG |
Связывание молекулы IgG |
с бактериальной клеткой |
|
|
с белком А через Fc-фрагмент |
для ее опсонизации |
|
|
(препятствие фагоцитозу) |
(помощь фагоцитозу) |
|
Белок А
Клеточная стенка
Рисунок 19 – Схема антифагоцитарного действия белка А стафилококка.
Клампинг-факторы |
стафилококков (хлопьеобразующие факторы ClfA и |
ClfB) представляют собой |
фибриноген-связывающие белки клеточной стенки. |
18
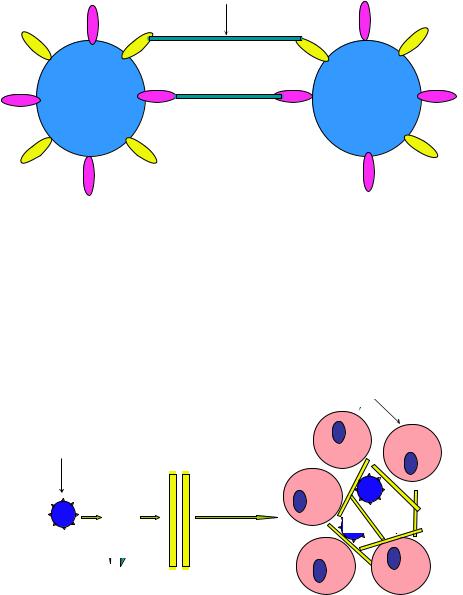
Наличие этих факторов приводит к склеиванию стафилококков в виде хлопьев при контакте микробных клеток с плазмой крови (рисунок 20).
Фибриноген
S. aureus |
S. aureus |
|
ClfB
 ClfA
ClfA
Рисунок 20 – Склеивание стафилококков с участием клампинг-факторов.
Внешне этот феномен напоминает реакцию агглютинации, поэтому некоторые авторы называют его реакцией плазмоагглютинации. В результате превращения фибриногена в фибрин вокруг микробных клеток при участии клампинг-фактора формируется псевдокапсула, защищающая бактерии от фагоцитирующих клеток хозяина (рисунок 21).
Макрофаги организма
Стафилококк с клампинг-фактором
Фибриноген Фибрин
Формирование
псевдокапсулы
Рисунок 21 – Формирование псевдокапсулы под влиянием клампинг-фактора стафилококка.
Эластин-связывающий белок принимает участие в бактериальной колонизации тканей, богатых эластином (легкие, кожа, стенки кровеносных сосудов).
Капсула стафилококков препятствует фагоцитозу (защита бактерий от опсонизации комплементом и соответственно комплемент-опосредованного поглощения фагоцитами), но способствует адгезии бактерий к клеткам организма и распространению патогенов по тканям. Микрокапсула обнаруживается у 70%

19
штаммов стафилококков. Роль капсулы в фагоцитозе бактерий отражена на рисунке 22.
Фагоцитоз
Опсонизация
Комплемент
Бактерия
Отсутствие Капсульная фагоцитоза
бактерия
Комплемент
Рисунок 22 – Роль бактериальной капсулы в комплемент-опосредованном фагоцитозе.
Энтеротоксины стафилококков обусловливают пищевые отравления. Энтеротоксины А, В, С1, С2, С3, D, Е, F являются термостабильными низкомолекулярными белками. Они устойчивы к действию спирта, формалина, протеолитических ферментов. Энтеротоксины взаимодействуют с эпителиальными клетками и активируют их ферментные системы, вызывая увеличение в клетках кишечного эпителия количества циклического аденозинмонофосфата (цАМФ) и циклического гуанидинмонофосфата (цГМФ). В результате этого увеличивается секреция солей и воды в просвет желудочно-кишечного тракта, развивается обильная рвота и диарея.
Токсин синдрома токсического шока (TSST-1) вызывает развитие нейротропных и вазотропных эффектов за счет резкой стимуляции выделения фактора некроза опухоли (ФНО-α) и интерлейкина 1. Синтез этого токсина связан с наличием профага (лизогенная конверсия).
Эксфолиативные токсины А и В вызывают разрушение межклеточных контактов между кератиноцитами в гранулярном слое эпидермиса и его отслойку или эксфолиацию (рисунок 23).
Рисунок 23 – Процесс отслойки эпидермиса в результате действия эксфолиативных токсинов.

20
Эксфолиативный токсин А является термостабильным и контролируется хромосомными генами, а эксфолиативный токсин В - термолабильный и детерминируется плазмидными генами.
Цитолитические токсины вызывают образование пор в клеточных мембранах (рисунок 24), в результате чего нарушается осмотическое давление и происходит лизис клеток (эритроцитов) или их набухание и гибель (лейкоцитов).
Рисунок 24 – Схема образования пор в клеточной мембране цитолитическими токсинами.
Альфа-гемолизин (альфа-токсин) формирует поры в мембране клеток, в результате чего снижается их активность и происходит лизис. Именно альфагемолизин обусловливает бета-гемолиз, проявляющийся на кровяном агаре при культивировании S. aureus.
Бета-гемолизин представляет собой сфингомиелиназу. Он разлагает сфингомиелин (компонент клеточных мембран) с образованием фосфохолина и керамидов, что способствует проникновению возбудителя в ткани.
Лейкоцидин Пантона-Валентина (PVL) – токсин, вызывающий дегрануляцию и разрушение лейкоцитов. Эпидемиологически он ассоциируется с тяжелыми инфекциями кожи и некротической пневмонией. Синтез PVL кодируется двумя генами (luk-S-PV и luk-F-PV), которые переносятся между разными штаммами S. aureus с помощью бактериофагов. PVL синтезируется преимущественно штаммами внебольничного метициллин-резистентного золотистого стафилококка – MRSA (рисунок 25).
|
|
Устойчивый |
|
|
к метициллину S. aureus, |
Чувствительный |
Устойчивый |
продуцирующий PVL |
|
||
к метициллину |
к метициллину |
|
S. aureus |
S. aureus |
|
Рисунок 25 – Схема формирования метициллин-резистентного золотистого стафилококка, продуцирующего лейкоцидин Пантона-Валентина (PVL).