Материал: Гиндуллина Хром-метода анлза
7.В каком хроматографическом методе основной фактор, определяющий удерживание компонента – растворение в неподвижной фазе?
8.Назовите три способы детектирования в газовой хроматографии.
9.Какова роль основных узлов в газовом хроматографе?
5.4. Характеристики удерживания
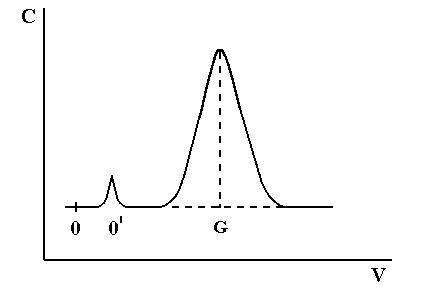
Если поток газа-носителя, содержащий десорбированное ве-ще- ство, проходит через чувствительный элемент прибора, фикси-рующего мгновенное изменение концентрации вещества в газе (детектор), то на записывающем устройстве этого прибора получается кривая, называемая хроматографическим пиком или кривой элюирования.
На рисунке 1.6. изображена типичная кривая элюирования. По оси абсцисс отложен объем элюата (можно отложить время хроматографирования). Ее параметры, называемые характеристиками удерживания, могут служить средством идентификации компонентов разделяемой смеси.
Рис.1.6.
Кривая
проявительного анализа (хроматографический пик)
Время от момента ввода анализируемой пробы до регистрации максимума пика называют временем удерживания (элюирования) tR .(отре-
зок OG на графике). Время удерживания складывается из двух составляющих – времени пребывания вещества в подвижной и неподвижной фазах. Первое фактически равно времени прохождения через колонку
несорбируемого компонента (отрезок ОО/ на графике). Значение tR не
зависит от количества пробы, но зависит от природы вещества и сорбента, скорости потока газа-носителя, а также упаковки сорбента и может
26

меняться от колонки к колонке. Поэтому для характеристики истинной удерживающей способности следует ввести исправленное время удер-
живания tR/
tR/ = tR − t0 |
(1.4) |
Величиной, не зависящей от скорости потока газа-носителя, является удерживаемый объем VR – это объем газа-носителя, который должен быть пропущен от момента ввода пробы до появления максимума пика на хроматограмме.
VR = F ЧtR |
(1.5), |
где F – объемная скорость потока, мл/с.
Объем для вымывания несорбируемого компонента VO включает в себя объем колонки, не занятый сорбентом
Приведенный удерживаемый объем V / |
равен: |
||
|
|
R |
|
V / = V − V |
(1.6) |
||
R |
R |
0 |
|
При постоянных условиях хроматографирования (скорость потока, давление, температура, состав фаз) значения характеристик удерживания строго воспроизводимы могут быть использованы для идентификации компонентов в качественном анализе и для физико-химических исследований.
Рассмотренные характеристики удерживания называются абсолютными. Кроме того, в хроматографии часто используют относительные характеристики удерживания.
При расчете относительного времени удерживания приведенное время удерживания какого-либо вещества относят к приведенному времени удерживания стандартного вещества:
tотн = tR/ |
/ |
(1.7) |
|
tст |
|
В качестве относительных параметров удерживания широко используют индексы Ковача. В отличие от относительных объемов индекс удерживания при выборе стандарта связан не с произвольно выбранным веществом, а с веществами, к которым предъявляют определенные требования. Во-первых, стандарт может представлять собой лишь нормальный алкан. Во-вторых, за стандарт берутся два соседних алкана, один из которых элюируется до, а другой после анализируемого соединения.
Индекс удерживания I какого-либо компонента рассчитывается по формуле:
|
lgt/ |
− lgt/ |
|
|
|
I = 100 |
R,i |
|
R,z |
+ 100z |
(1.8), |
lgt/ |
|
− lgt/ |
|||
|
|
|
|
||
|
R,z+ 1 |
R,z |
|
|
|
27
где tR/ ,i – приведенное время удерживания анализируемого i-го компо-
нента; tR/ ,z и tR/ ,z+ 1 – приведенные времена удерживания н-алканов, z – число углеродных атомов.
5. 5. Теоретические представления в газовой
хроматографии
В процессе хроматографического разделения часто происходит размывание пиков. Это явление обусловлено процессами, протекающими в колонке, например, медленностью сорбции и десорбции и др. Это приводит к тому, что разделение компонентов может вообще не произойти при значительной разнице в коэффициентах распределения.
Для объяснения специфического для хроматографии процесса размывания обычно используют теорию эквивалентных теоретических тарелок Мартина и Синджа и диффузионно-массообменную (кинетическую) теорию Ван-Деемтера.
5.5.1. Теория эквивалентных теоретических тарелок
По аналогии с теорией дистилляционных колонн хроматографическая колонка мысленно разбивается на ряд последовательных теоретических ступеней-тарелок, через которые периодически проходят порции газа. Каждая тарелка содержит подвижную (газовую) и неподвижную (жидкую или твердую) фазы. Предполагается, что за время нахождения порции газа на тарелке успевает установиться равновесие между подвижной и неподвижной фазами для всех компонентов. Таким образом, хроматографический процесс – многоступенчатый и состоит из большого числа актов сорбции и десорбции (в газо-адсорбционной хроматографии) или растворения и испарения (в газо-жидкостной хроматографии), а сама колонка рассматривается как система, состоящая из совокупности многих ступеней-тарелок.
Длина участка колонки, на которой достигается состояние равновесия между концентрацией вещества в подвижной и неподвижной фазах, называется условно высотой, эквивалентной теоретической тарелке
(ВЭТТ). Существует простая зависимость:
H = |
L |
(1.9), |
|
N |
|||
|
|
где L – длина хроматографической колонки, см; N – число теоретических тарелок; Н – высота, эквивалентная теоретической тарелке, см.
28

Для вычисления числа теоретических тарелок (ч.т.т.) измеряют ширину хроматографического пика на половине высоты, w 1/2 .Тогда
N = |
5,54 |
ж |
t/ |
ц2 |
= |
5,54 |
ж V / |
ц2 |
(1.10), |
|
з |
w |
ч |
з |
w |
ч |
|||||
|
|
|
R |
|
|
|
|
R |
|
|
|
|
и |
1/ 2 ш |
|
|
и |
1/ 2 ш |
|
||
где w 1/2 –ширина полупика, выраженная в единицах времени (мин) или объема, мл.
Количественной мерой размывания хроматографических полос, т.е. эффективности колонки является ВЭТТ. С увеличением числа т.т. эффективность хроматографической колонки возрастает.
Втеории теоретических тарелок реальный хроматографический процесс заменен идеальным, по которому хроматографическая полоса размывается вследствие равновесных процессов между подвижной и неподвижной фазами. Такое рассмотрение размывания хроматографической полосы не вскрывает сущности процесса и не дает информации о том, как подобрать такие условия, которые позволили бы уменьшить величину Н и тем самым повысить эффективность хроматографической колонки.
5.5.2.Кинетическая теория
Втеории скоростей не делается допущений о наличии равновесных условий в колонке. Эта теория рассматривает динамику процесса распределения вещества между двумя фазами. Согласно упрощенному уравнению Ван-Деемтера, величина Н зависит от ряда параметров хроматографической колонки:
H = A + B |
F |
+ CF |
(1.11), |
|
|
|
|
где Н – высота, эквивалентная теоретической тарелке, см; F – линейная |
|||
скорость прохождения газа-носителя через колонку, см/с; А, В, С – константы.
Согласно этому уравнению, размывание хроматографической полосы, а следовательно, и снижение эффективности разделения связаныс тремя основными факторами:
1. Вихревая диффузия (слагаемое А). Хроматографическая колонка заполняется твердым зерненым сорбентом, поэтому газ-носитель перемещается по колонке через множество взаимосвязанных каналов. Одни молекулы могут продвигаться более короткими путями, другие – более длинными. Время пребывания последних молекул в колонке соответственно возрастает, что приводит к размыванию хроматографического пика. Вихревая диффузия уменьшается, если частицы твердого сор-
29
бента имеют одинаковые размеры и правильную форму и колонка плотно упакована.
2.Молекулярная диффузия. Слагаемое В/F характеризует размывание пиков, вызываемое диффузией анализируемого вещества в га- зе-носителе. (Диффузия в жидкой фазе ничтожно мала.) При бесконечно малой скорости газа-носителя вещество перемещается вниз по колонке под действием собственной молекулярной диффузии. Величина В/F, а следовательно, и Н в этом случае бесконечно большие.
3.Сопротивление массопередаче (член СF). Эта величина харак-
теризует скорость распределения вещества между газом-носителем и неподвижной жидкой фазой. Чем меньше толщина слоя жидкости на твердом носителе и чем меньше вязкость этой жидкости, тем быстрее устанавливается равновесие.
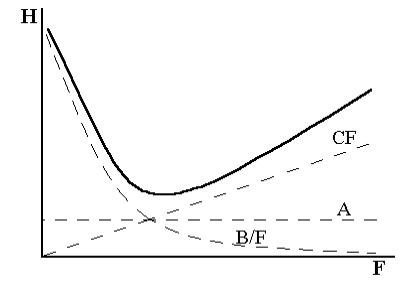
Рис.1.7.
Графическое
изображение
уравнения ВанДеемтера
Влияние каждого слагаемого уравнения (1.11) на величину Н в зависи-
мости от линейной скорости подвижной фазы показано на рисунке 1.7. При выборе колонки необходимо решать, уменьшить ли величину
Н или уменьшить время разделения, повышая скорость потока газа-но- сителя, но сохраняя приемлемо малое значение Н. Член А не зависит от скорости газа-носителя и он весьма низкий в хорошо заполненной колонке. Член В/F с ростом скорости газа-носителя уменьшается, а СF, наоборот, увеличивается. Поэтому стараются подобрать такую скоростьF, при которой В и С компенсировали бы друг друга, а величина Н была минимальной.
30