Материал: Гиндуллина Хром-метода анлза
При этом применяют такие формы записи: например, 0,1 н H2SO4, с(H2SO4) = 0,1 моль экв/л = 0,1 мэкв/мл; с(1/2 H2SO4) = 0,1 моль/л, где 1/2 – фактор эквивалентности (f). Если f=1, то предпочтительнее использовать термин «молярная» концентрация.
Эквивалентом называется такая часть атома, иона или молекулы, которая химически равноценна (эквивалентна) одному иону водорода в данной кислотно-основной реакции или одному электрону в данной окислительно-восстановительной реакции. Единицей количества эквивалента вещества является моль.
Например, в реакции
2NaOH + H2SO4 Ђ Na2SO4 + 2H2O или NaOH + 1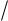 2 H2SO4 Ђ 1
2 H2SO4 Ђ 1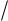 2 Na2SO4 + H2O
2 Na2SO4 + H2O
эквивалент серной кислоты будет равен 1/2H2SO4, где 1/2 – фактор эквивалентности.
Фактор эквивалентности (f) – это число, показывающее, какая часть моля вещества равноценна одному иону водорода в данной кис- лотно-основной реакции или одному электрону в данной окислительновосстановительной реакции.
Фактор эквивалентности может быть равен 1 или меньше 1, например, f (NH4OH)=1; f (H2SO4 )=1/2; f(KMnO4)= 1/5 и т. д.
Для нахождения фактора эквивалентности вещества обязательно надо указывать реакцию, в которой данное вещество участвует. В реакциях кислотно-основного взаимодействия фактор эквивалентности равен f=1/[H+], где [H+] – число ионов водорода, отдаваемое или присо-
единяемое одной молекулой или одним ионом.
Для нахождения f в окислительно-восстановительной реакции составляют полуреакции и вычисляют его значение по формуле
f = 1/z, где z – число электронов, отдаваемое или присоединяемое одной молекулой или одним ионом в данной полуреакции.
Например, в полуреакции I2 + 2e → 2I − f (I2 ) =1/2, а f (I– ) = 1.
Молярной массой эквивалента вещества (Мэ) называют массу одного моль эквивалента этого вещества, равную произведению фактора эквивалентности на молярную массу вещества (М). Например:
Мэ(H2SO4) = f(H2SO4 )×M(H2SO4 )=1/2×98= 49 г/моль-экв; Мэ(H2SO4) – молярная масса эквивалента серной кислоты. Молярная концентрация эквивалента вычисляется по формуле
CH = |
mЧ1000 |
|
MЭ ЧV |
71
Взаимосвязь между молярной концентрацией и молярной концентрацией эквивалента отражена в следующей формуле
CM = f ЧCH .
Массовая концентрация – это отношение массы растворенного вещества к объему раствора.
Численное значение этой концентрации выражается в г/л, мг/мл, г/мл. В титриметрическом анализе применяют единицу измерения массовой концентрации в г/мл. Это титр раствора, Т.
Например, Т(HNO3)=0,01232 г/мл:
Т = m/V
Титр рабочего раствора по определяемому веществу, Т(В/А), г/мл – это отношение массы m(А) определяемого вещества к эквивалентномуобъему V(В) рабочего раствора:
T(B/A)=m(А)/V(В)
Другими словами, Т(В/А) показывает, какая масса анализируемого вещества (А) реагирует с 1 мл рабочего раствора вещества (В).
Зная Т(В/А) и объем (мл) рабочего раствора (В), затраченного на титрование, можно рассчитать массу (г) определяемого вещества:
m(А) = Т(В/А) V(В)
Например, m(Na2CO3)=T(HCI/ Na2CO3)×V(HCI). Кроме того,
Т(В/А) = сн(В)×Мэ(А)/1000
Массовая доля w(А) вещества А – это отношение массы m(А) вещества А к общей массе mобщ раствора или смеси веществ:
w(А)= m(А) / mобщ
В количественном анализе массовую долю измеряют в процентах. Она характеризует содержание компонента в твердом веществе или
растворе:
w(А) = [m (А)/ mобщ]×100(%)
При этом возможны, например, следующие варианты употребления терминов: реактив чистотой 98 % (по массе); соль, содержащая по массе 3,1 % примесей, минерал с массовой долей SiO2 8,4 %, w(SiO2)=8,4%; раствор плотностью 1,28 г/см3 с массовой долейH2SO437 % или w(H2SO4)=37 %.Это означает, что 37 г серной кислоты содержится в 100
граствора, плотность которого равна 1,28 г/см3.
Всправочных таблицах приведены для растворов кислот, оснований и некоторых солей соответствующие значения плотностей этих
растворов (r в г/см3) и массовые доли (w %) веществ. Используя эти величины, можно рассчитать молярную концентрацию эквивалента или массовую концентрацию вещества в растворе.
72
Пример 1. В 45,0 мл воды растворили 5,0 г КOH. Вычислить массовую долю растворенного компонента.
Решение: воспользуемся приведенной выше формулой: w = 5×100/(5 + 45) =10 %
Масса полученного раствора равна 50,0 г, т. к. плотность воды при комнатной температуре равна 1,0 г/см3.
Взаимосвязь между молярной концентрацией, молярной концентрацией эквивалента и массовой долей растворенного компонента и титром приводится в формулах, приведенных в таблице.
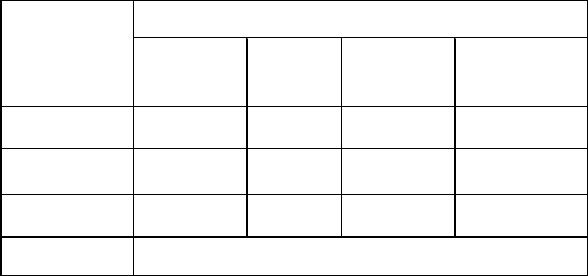
Таблица
Формулы пересчета концентраций растворов
Определяемая |
|
|
|
|
|
|
|
|
|
Исходная концентрация |
|
|
|||||
концентрация |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ω |
СМ |
СН |
|
|
Т |
|
|||||
Процентная |
|
m |
|
|
|
|
|
C |
|
M |
CHэквM |
Ч |
f |
T 100 |
|
||
ω, % |
|
|
вещ. |
Ч100% |
M |
Ч |
|
Ч |
|
|
Ч |
||||||
|
|
|
10Чρ |
10Чρ |
|
|
ρ |
||||||||||
|
mр-ра |
|
|
|
|
|
|
||||||||||
Молярная |
|
ω |
Ч10Чρ |
моль/л |
СHэквf |
|
|
T Ч1000 |
|||||||||
См, моль/л |
|
|
|
|
|
|
|
|
|
|
|
Ч |
|
|
|
M |
|
|
|
|
|
M |
|
|
|
|
|
|
|
|
|||||
Нормальная |
|
ω |
Ч10Чρ |
CM |
моль экв/л |
T Ч1000 |
|
||||||||||
Сн, моль экв/л |
|
|
|
|
fэкв |
|
|
|
|
M Ч fэкв |
|||||||
|
|
M Ч fэкв |
|
|
|
|
|||||||||||
Титр Т, г/мл |
|
|
|
ω |
|
|
ρ |
C |
|
M |
CHэквM |
|
f |
г/мл |
|||
|
|
|
|
|
|
Ч |
|
|
M |
Ч |
|
Ч |
Ч |
|
|
|
|
|
|
|
|
100 |
|
1000 |
1000 |
|
|
|
|
||||||
Примечание ρ – плотность раствора, г/см3; fэкв – фактор эквивалентности; М – молярная масса вещества, г/моль; m – масса, г
При переходе от массовой доли растворенного компонента к молярной или молярной концентрации эквивалента необходимо учитывать плотность раствора. Между массой вещества (m), его плотностью (ρ) и
объемом (V) существует следующее соотношение: ρ = m/V.
В справочных таблицах для растворов кислот, оснований и некоторых солей приведены массовые доли веществ (ω, %) и соответствующие
значения плотностей этих растворов (ρ, г/см3). Используя эти величины, можно рассчитать молярную, молярную концентрацию эквивалента или массовую концентрацию раствора.
73
ПРИЛОЖЕНИЕ 3
Расчеты при приготовлении растворов
Стандартные растворы. В титриметрическом анализе растворы с точно известной концентрацией называют рабочими, или стандартными. Их можно приготовить несколькими способами: а) по точной навеске исходного вещества; б) по приблизительной навеске вещества с последующим определением точной концентрации (стандартизацией) приготовленного раствора по соответствующему стандартному раствору; в) по фиксаналу.
В первом способе в качестве исходных веществ для приготовления раствора можно применять только химически чистые, устойчивые соединения, состав которых строго соответствует химической формуле. Такие вещества называют установочными, или первичными стандартами. Стандартные растворы из таких веществ приготавливают растворением точной навески в воде и разбавлением полученного раствора до
требуемого объема. Зная массу (m) растворенного в воде химически чистого соединения и объем (V) раствора, легко вычислить титр (Т) и молярную концентрацию эквивалента ( Сн) приготовленного раствора:
T = |
m |
г/мл (1) |
СH = |
m ×1000 |
(2) |
|
V |
|
|
MЭ × V |
|
Второй способ основан на приготовлении растворов из веществ, не удовлетворяющих перечисленным выше требованиям. В этом случае сначала готовят раствор приблизительной концентрации по навеске вещества, взятой на технических весах. Параллельно с этим готовят стандартный раствор какого-либо подходящего установочного вещества (первичный стандарт). Далее первичный стандарт титруют раствором , приготовленным по приблизительной навеске, и, зная концентрацию стандартного раствора Сн(А) вычисляют концентрацию приготовленного раствора Сн(В) ( формулы 3, 4). Титрованные растворы, концентрацию которых находят в результате титрования, называются стандартизованными (или титрованными) растворами (или вторичными стандартами), а установление точной концентрации раствора титрованием называют стандартизацией раствора.
(CH ЧV )A = (CH ЧV )B |
|
(3) |
CH (A) = m(A)Ч1000 |
, |
(4) |
MЭ (A)ЧV |
|
|
Приготовление стандартного раствора из фиксанала |
сводится к |
|
74
тому, чтобы количественно перенести содержание ампулы, в которую запаяно точно дозированное количество или различных твердых веществ, или растворов известной концентрации в мерную колбу определенной емкости (чаще всего 1 л), после чего растворить вещество в дистиллированной воде и полученный раствор разбавить водой до метки.
Приготовление растворов из концентрированных растворов разбавлением. При приготовлении растворов (например, кислот и оснований) используется разбавление. В этом случае исходят из того, что при разбавлении раствора его объем и концентрация будут изменяться, а общее количество моль или моль эквивалентов растворенного вещества останется постоянным. Поэтому при разбавлении раствора справедливо равенство:
(СН ЧV )конц = (СН ЧV )разб или (СМ ЧV )конц = (СМ ЧV )разб |
(5) |
Следовательно, зная молярную или нормальную концентрацию концентрированного раствора, можно вычислить его объем, необходимый для приготовления разбавленного раствора заданного объема и заданной концентрации.
Пример 1.
Сколько миллилитров конц. H2SO4 (ρ=1,49 г/см3), содержащей 60% H2SO4, нужно взять для приготовления 500 мл0,1 н. раствора?
Решение:
1. Вычислим молярную концентрацию эквивалента концентрированной H2SO4:
CH = |
ω × ρ × 10 |
= |
60 × 1,49 × 10 |
= 18 |
н |
|
M × f |
|
49 |
|
|
2. Если раствор разбавлять, то его объем и концентрация будут изменяться, но общее количество эквивалентов растворенного вещества останется постоянным. Поэтому при разбавлении, как и при титровании, справедливо равенство: (CH × V )1 = (CH × V )2 . Применяя его к рассмат-
риваемому случаю, получим: 18 × V = 0,1× 500 , откуда Vконц(H2SO4)=3 мл.
Пример 2.
Рассчитать, какой объем 3 н H2SO4 следует прибавить к 1 л 0,6 нH2SO4, чтобы получить 1,5 н раствор?
Решение:
(CH × V )1 + (CH × V )2 = (CH × V )3
3V + 0,6 × 1 = (V1 + 1) × 1,5
Решив полученное уравнение, получим V=600 мл.
75