Материал: Гиндуллина Хром-метода анлза
(насадкой), а внутреннюю стенку капиллярной колонки покрывают пленкой жидкости или пылью адсорбента.
В зависимости от цели проведения хроматографического процесса различают аналитическую хроматографию (качественный и количественный анализ); препаративную хроматографию (для получения веществ в чистом виде, для концентрирования и выделения микропримесей); промышленную (производственную) хроматографию для автоматического управления процессом (при этом целевой продукт из колонки поступает в датчик). Хроматографию часто используют для исследовательских целей при изучении растворов, каталитических процессов, кинетики химических процессов и т.п.
Классификация по способам проведения анализа подразделяет хроматографию на три вида: 1) фронтальный, 2) проявительный, 3) вытеснительный .
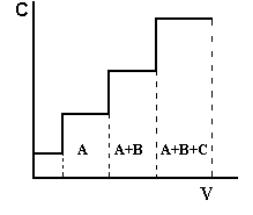
Фронтальный метод наиболее прост по выполнению. Через хроматографическую колонку с сорбентом непрерывным потоком пропускают раствор или газовую смесь исследуемых веществ, сорбируемость которых увеличивается в ряду А < В < С. Соответственно этому компоненты располагаются в колонке. Однако они разделяются не полностью. В чистом виде может быть выделен лишь первый, наиболее слабо сорбирующийся компонент, который движется вдоль слоя сорбента впереди остальных. За зоной первого компонента следует в непосредственном контакте зона, содержащая первый и второй компоненты. Третья зона содержит смесь первого, второго и третьего компонентов. В некоторый момент времени сорбент насыщается, и наступает «проскок», т.е. из колонки начинают выходить компоненты в соответствии с их сорбируемостью. Если пропускать жидкость или газ, выходящие из колонки, через детектор концентраций и наносить показания его в течение всего опыта на график, то полученная выходная кривая будет иметь форму ступенчатой кривой (рис.1.1).
Фронтальный метод не нашел широкого применения в анализе, т.к. не дает полного разделения компонентов анализируемой смеси. Однако этот метод весьма эффективен для препаративного выделения чистого вещества из технического образца при условии, что это вещество удерживается в колонке слабее всех других компонентов объекта анализа.
Типичные примеры применения фронтального анализа: очистка и умягчение воды ионообменными материалами; очистка воздуха активированными углями от отравляющих веществ в противогазах и вентиляционных фильтрах химических предприятий; концентрирование ценных веществ из сточных промышленных вод металлургических предприя-
6
тий; очистка лекарственных препаратов и пищевых продуктов с помощью ионообменников и т.д.
Рис.1.1. Выходная кривая фронтального анализа
А, В, С – разделяемые вещества
Проявительный (элюентный) метод выгодно отличается от фронтального тем, что он позволяет полностью разделить много-компо- нентную смесь. Хроматографическую колонку промывают растворителем или газом-носителем (элюентом), обладающим меньшей сорбируемостью, чем любое из разделяемых веществ. Затем в колонку вводят исследуемую смесь в виде порции раствора или газа, а не непрерывно, и продолжают пропускать элюент. При этом разделяемые вещества перемещаются вдоль колонки с разными скоростями в соответствии с их сорбируемостью. На выходе из колонки детектор фиксирует непрерывно концентрацию компонентов, а связанный с ним регистрирующий прибор записывает выходную кривую в виде ряда пиков, число которых соответствует числу разделенных компонентов (рис.1.2).
Проявительный метод анализа получил широкое применение как в жидкостной, так и в газовой хроматографии. Это объясняется тем, что при правильном выборе условий разделения компоненты смеси выходят из колонки в чистом виде, и их можно выделить для исследования другими методами анализа. Кроме того, качественный и количественный состав анализируемой смеси можно определить простым измерением объемов удерживания и площадей пиков соответствующих компонентов на полученной хроматограмме.
Вытеснительный метод отличается от фронтального и проявительного тем, что после введения пробы исследуемой смеси колонку
7
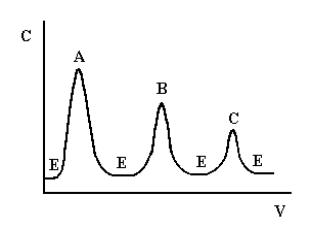
Рис. 1.2. Выходная кривая проявительного анализа
А, В, С – разделяемые вещества, Е – растворитель (элюент)
промывают растворителем или газом-носителем, к которым добавляют раствор вещества (вытеснитель), обладающего большей сорбируемостью, чем любое из разделяемых веществ. По мере продвижения по колонке элюент вытесняет вещество С, которое в свою очередь вытесняет вещество В и т.д. В результате вытесняемая смесь перемещается впереди фронта вытеснителя и скорость движения вещества равна скорости движения вытеснителя. Разделяемые вещества и на колонке, и в элюате располагаются последовательно друг за другом. Каждый из компонентов выделяется в чистом виде, но не количественно, так как зоны компонентов не разделены промежутками чистого сорбента.
Невозможность получения на выходе из колонки достаточно чистых компонентов разделяемой смеси, а также длительность процесса разделения затрудняют использование этого метода в аналитических целях. Однако для препаративных целей метод не потерял значения, так как возможность применения таких высокоактивных и доступных адсорбентов, как активированные угли, позволяет достигнуть высокой производительности. Достоинством метода является также то, что зоны не размываются в отличие от проявительного анализа.
Вопросы для самоконтроля
1.В чем сущность хроматографического процесса?
2.Каково назначение подвижной и неподвижной фаз?
3.Какие процессы происходят в колонке?
4.Как классифицируют методы хроматографии по агрегатному состоянию фаз и по способу хроматографирования??
5.В чем состоит проявительный (элюентный ) анализ?
8
6.В чем преимущество элюентной хроматографии перед фронтальной и вытеснительной?
7.Как классифицируют методы хроматографии по технике проведения эксперимента и цели ?
8.В чем сущность хроматографического разделения по методу: а) газожидкостной хроматографии; б) распределительной жидкостной хроматографии; в) осадочной хроматографии; г) тонкослойной хроматографии; д) ионообменной хроматографии; е) эксклюзионной хроматографии?
9.Как влияет температура на хроматографический процесс?
3.Ионообменная хроматография
Воснове ионообменной хроматографии лежит обратимый стехиометрический обмен ионов, содержащихся в хроматографируемом растворе, на ионы веществ, называемых ионитами или ионобменниками. Иониты могут быть органические и неорганические, природные и синтетические. По знаку обменивающихся ионов различают катиониты (для обмена катионов) и аниониты (для обмена анионов).
К природным ионитам относятся алюмосиликаты, некоторые сорта каменных углей, мягкие и твердые угли даже без предварительной обработки.
Ваналитической практике широко используют синтетические иониты. Ионообменники получают реакциями поликонденсации либо полимеризации, линейные цепи полимеров разветвлены и связаны друг
сдругом «мостиками», например, молекулами дивинилбензола; в состав ионитов входят различные функциональные (ионогенные) группы, которые и определяют наиболее характерные свойства ионитов. Иониты нерастворимы в воде, кислотах, щелочах и во многих органических растворителях, но способны набухать в воде за счет гидрофильных ионогенных групп.
Органические катиониты содержат кислотные функциональные
группы: – SO3–, – PO3–, – COO–, – OH –. Органические аниониты содержат группы основного характера: – NH2+, = NH+, ≡ N+, – N(CH3)3+. Катиониты представляют собой полиэлектролиты, диссоциирующие с об-
разованием высокомолекулярного аниона (например, RSO3–) и подвижного катиона (например, Н+- иона),легко обменивающегося на другие катионы. Аниониты диссоциируют на высокомолекулярный катион (например, RNH+) и подвижный анион (например, ОН–), способный обмениваться на другие анионы (R – высокомолекулярный углеводородный радикал ионообменной смолы).
9
Реакции ионного обмена можно представить схематично сле-дую- щим образом:
RSO3H + CaCl2 Ђ (RSO3)2 Ca + 2HCl
(катионный обмен)
RN(CH3 )3OH + NaCl Ђ RN (CH3 )3Cl + NaOH
(анионный обмен)
Реакции ионного обмена обратимы и в первом приближении подчиняются закону действующих масс.
Важной характеристикой ионита является его обменная емкость.
3.1. Обменная емкость ионитов
Обменная емкость (ОЕ) – количественная мера способности ионита поглощать противоионы. Численно обменную емкость выражают количеством поглощенных миллимоль эквивалентов ионов на 1г сухой смолы в Н+-форме для катионита и Сl −-форме для анионита.
Определение емкости можно отнести и к единице объема набухшего слоя ионита. Обменная емкость, полученная в статических условиях, когда навеску ионита помещают в раствор насыщающего иона определенной концентрации и выдерживают при встряхивании до полного насыщения ионита, называется статической (СОЕ). Величина ее отличается от величины обменной емкости, полученной в динамических условиях при пропускании насыщающего раствора через колонку с ионитом.
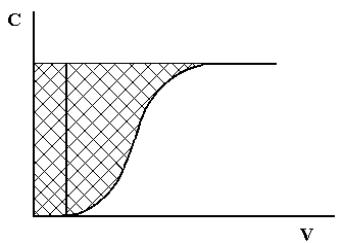
Рис.1.3. Выходная хроматографическая кривая
Динамическая обменная емкость характеризуется двумя показателями: динамической обменной емкостью до проскока (ДОЕ) и полной динамической емкостью (ПДОЕ). ДОЕ представляет собой емкость
10