Материал: Гиндуллина Хром-метода анлза
предыдущей. Элюат, содержащий ионы цинка, собирают в другую коническую колбу емкостью 250мл.
Следует помнить, что над слоем анионита всегда должна находиться жидкость.
2. Определение никеля
Содержание ионов никеля в солянокислом растворе определяют комплексонометрическим методом. Для этого в коническую колбу с ионами никеля добавляют 50 мл дистиллированной воды, 10 мл 6М раствора NaOH и по каплям 12 % NH4OH до изменения окраски красной лакмусовой бумаги в серо-голубой цвет (красную лакмусовую бумагу помещают в раствор и, не вынимая ее, следят за изменением цвета). После этого добавляют щепотку индикатора мурексида и титруют трилоном Б до перехода желтой окраски раствора в фиолетовую.
Содержание никеля определяют по формуле:
m(Ni2+ ) = |
C ЧV ЧMЭ |
(2.21), |
|
1000 |
|||
|
|
где С – молярная концентрация эквивалента трилона Б, моль-экв/л ;
V – объем трилона Б, израсходованный на титрование, мл; MЭ (Ni2+) –
молярная масса эквивалента никеля в данной реакции, г/моль-экв; m (Ni2+) – масса никеля в исследуемом растворе, г
3. Определение цинка
В коническую колбу, содержащую ионы цинка, добавляют по каплям из бюретки 12 % раствор аммиака до щелочной среды по красному лакмусу, 5 мл аммиачной буферной смеси, щепотку индикатора эриохрома черного или хрома темно-синего и титруют трилоном Б до изменения фиолетово-красной окраски в синюю.
Содержание цинка определяют по формуле:
m(Zn2+ ) = |
C ЧV ЧMЭ |
(2.22), |
|
1000 |
|||
|
|
где С – молярная концентрация эквивалента трилона Б, моль-экв/л;
V – объем трилона Б, израсходованный на титрование, мл; MЭ (Zn2+) –
молярная масса эквивалента цинка в данной реакции, г/моль-экв; m (Zn2+) – масса цинка в исследуемом растворе, г
ТОНКОСЛОЙНАЯ ХРОМАТОГРАФИЯ
Работа 1. Разделение и обнаружение галогенидов
Цель работы: разделить и идентифицировать галогенид-ионы методом одномерной восходящей тонкослойной хроматографии.
56
Сущность работы: В тонкослойной хроматографии (ТСХ) процесс разделения происходит в слое тонкодисперсного сорбента, нанесенного на стеклянную или металлическую пластинку. В органическом анализе наибольшее распространение получила адсорбционная ТСХ (подвижная фаза – жидкость, неподвижная фаза – адсорбент).
Анализ смеси веществ проводят по следующей схеме: на пластинку сорбента на небольшом расстоянии от края наносят на линию старта каплю разделяемой смеси, пластинку подсушивают и помещают в хроматографическую камеру с ПФ. ПФ под действием капиллярных сил поднимается по сорбенту, вместе с ней перемещаются с различной скоростью определяемые вещества.
Анализируемый раствор наносят на стартовую линию с помощью стеклянного капилляра в объеме не более 5–10 мкл. Чем меньше площадь стартового пятна, тем менее размытой будет зона вещества после хроматографирования. Поэтому пробу наносят в одну и ту же точку в несколько приемов, каждый раз подсушивая пятно.
Зоны разделяемых веществ имеют вид пятен, которые могут быть видимыми и невидимыми; в последнем случае хроматограмму проявляют – опрыскивают раствором специфического реагента, либо подвергают воздействию УФ-излучения.
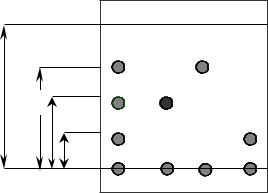
Скорость перемещения компонентов определяется соответствующими коэффициентами распределения: чем меньше коэффициент распределения, тем быстрее вещество передвигается по сорбенту. В качестве характеристики удерживания используется величина Rf – подвижность, определяемая как отношение расстояния фронтов компонента и ПФ (рис. 1)
L |
li |
линия фронта
линия старта
Смесь А В С
Рис.2.1. Плоскостная хроматограмма. Определение Rf
57
Rf = |
l |
(2.23), |
|
L |
|||
|
|
где l – расстояние от линии старта до центра пятна компонента, см; L – расстояние, пройденное ПФ от линии старта до линии фронта, см.
Под фронтом растворителя понимают видимую границу распространения растворителя по пластинке.
Величина Rf не зависит от концентрации определяемого вещества и от присутствия других веществ, но зависит от природы вещества, природы ПФ и НФ и температуры.
Качественный анализ проводят, сравнивая Rf компонентов смеси и стандартных веществ.
Растворы, реактивы, аппаратура.
1.Стандартный раствор NaCl, 1 М.
2.Стандартный раствор KBr, 1 М.
3.Стандартный раствор KJ, 1 М.
4.Бромкрезоловый пурпурный, 0,1%-ный раствор в этаноле с добавлением 1 капли аммиака.
5.Подвижная фаза – смесь ацетона (65 мл), н-бутанола (20 мл), конц. аммиака (10 мл), дистиллированной воды (5 мл).
6.Хроматографическая пластинка марки «Silufol» или др.
7.Капилляры стеклянные
8.Хроматографическая камера
Выполнение работы
1.На дно хроматографической камеры помещают подвижную фазу (высота слоя около 0,5 см), закрепляют на задней стенке камеры кусочек фильтровальной бумаги, смоченный в растворителе, затем закрывают крышкой и оставляют на 15–20 мин для насыщения камеры парами ПФ.
2.На хроматографической пластинке на расстоянии около 1 см от краев отмечают линию старта и линию фронта и с помощью капилляра наносят на стартовую линию каплю раствора разделяемой смеси, рядом наносят по капле растворов индивидуальных галогенидов, используемых в качестве стандартов.
3.Пластинку высушивают, помещают в хроматографическую камеру и плотно закрывают крышкой. Во время разделения не рекомендуется открывать крышку камеры, перемещать камеру. Анионы продвигаются по пластинке в виде аммонийных солей, катионы щелочных металлов остаются на старте.
4.Когда фронт ПФ пройдет заданное расстояние и произойдет разделение компонентов, пластинку вынимают, высушивают в токе теплого воздуха и приступают к идентификации пятен.
58
5.Для обнаружения пятен хроматограмму опрыскивают раствором бромкрезолового пурпурного и подсушивают. Аммонийные соли дают желтые пятна, а ионы щелочных металлов – ярко-синие (на старте). После хроматографирования сопоставляют положение пятен исследуемой смеси и индивидуальных веществ, затем делают вывод о присутствии или отсутствии их в анализируемом растворе.
6.Для идентификации компонентов сравнивают рассчитанные величины Rf для компонентов смеси и индивидуальных веществ. Рассчи-
тывают коээфициент разделения α для пар ионов как отношение подвижностей Rf и оценивают степень разделения. Делают вывод о закономерности изменения величины Rf в ряду галогенид-ионов.
БУМАЖНАЯ ХРОМАТОГРАФИЯ
Работа 1. Разделение железа (III) и меди (II)
Цель работы: разделить и идентифицировать ионы железа и меди методом круговой бумажной хроматографии.
Сущность работы. Хроматография на бумаге – разновидность метода распределительной хроматографии. Носителем для неподвижного растворителя служит при этом фильтровальная бумага.
Анализ смеси веществ проводят по следующей схеме: на круглый обеззоленный фильтр в центр наносят каплю разделяемой смеси, фильтр подсушивают и помещают в хроматографическую камеру с ПФ. ПФ под действием капиллярных сил поднимается по «фитилю», достигает стартового пятна с разделяемой смесью, вместе с ней перемещаются с различной скоростью определяемые вещества.
Анализируемый раствор наносят на стартовую линию с помощью стеклянного капилляра в объеме не более 5–10 мкл. Чем меньше площадь стартового пятна, тем менее размытой будет зона вещества после хроматографирования. Поэтому пробу наносят в одну и ту же точку в несколько приемов, каждый раз подсушивая пятно.
Зоны разделяемых веществ имеют вид концентрических колец, которые могут быть видимыми и невидимыми; в последнем случае хроматограмму проявляют – опрыскивают раствором специфического реагента, либо подвергают воздействию УФ-излучения (см. рис.2.2).
Скорость перемещения компонентов определяется соответствующими коэффициентами распределения: чем меньше коэффициент распределения, тем быстрее вещество передвигается по сорбенту. В качестве характеристики удерживания используется величина Rf – подвижность, определяемая как отношение расстояния фронтов компонента и ПФ:
59

Rf = Ll ,
где l – расстояние, пройденное зоной компонента от старта пятна, см;
L – расстояние, пройденное подвижной фазой, см. Под фронтом растворителя понимают видимую границу распространения растворителя по бумаге.
Рис.2.2. Круговая хроматограмма
1 – круглый фильтр; 2 – «фитиль», погружаемый в растворитель;.А – место нанесения анализируемого раствора
Величина Rf каждого катиона не зависит от концентрации определяемого катиона, температуры, присутствия других катионов и природы аниона, с которым связан изучаемый катион, но зависит от состава и свойств используемой ПФ, а также сорта хроматографической бумаги. У катионов железа (III) и меди (II) значения Rf значительно отличаются по величине. Поэтому удается их четкое разделение на бумаге.
Растворы, реактивы, аппаратура.
1.Стандартный раствор соли Fe 3+, 1 мг/мл
2.Стандартный раствор соли Cu 2+, 1 мг/мл
3.Раствор K4[Fe(CN)6], 10% -ный
4.Подвижная фаза – смесь этанола с 5М HCl (9:1) по объему
5.Обеззоленная фильтровальная бумага «синяя лента»
6.Капилляры стеклянные
7.Хроматографическая камера
Выполнение работы
60