Материал: Функции белков в организме. Стероидные гормоны. Липиды
Суточная потребность составляет 2-3 мг.
Микроорганизмы кишечника жвачных животных активно синтезируют его; эти животные не нуждаются во введении витамина В6 с пищей. Микрофлора кишечника человека также синтезирует витамин В6, но в недостаточных количествах, поэтому для человека и большинства животных основным источником витамина являются продукты питания.
Механизм ферментативного катализа
В процессе катализа реакции в контакт с субстратом вступает не вся молекула фермента, а определенный ее участок, который называется активным центром. Эта зона молекулы не состоит из последовательности аминокислот, а формируется при скручивании белковой молекулы в третичную структуру. Отдельные участки аминокислот сближаются между собой, образуя определенную конфигурацию активного центра. Важная особенность строения активного центра - его поверхность комплементарна поверхности субстрата, т.е. остатки АК этой зоны фермента способны вступать в химическое взаимодействие с определенными группами субстрата. Можно представить, что активный центр фермента совпадает со структурой субстрата как ключ и замок.
В процессе ферментативной реакции различают несколько стадий: присоединение молекулы субстрата к ферменту, преобразование первичного промежуточного соединения в один или несколько последовательных (переходных) комплексов и протекающее в одну или несколько стадий отделение конечных продуктов реакции от фермента.
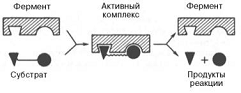
Образование нестойкого фермент-субстратного комплекса согласно теории Э. Фишера «ключ-замок».
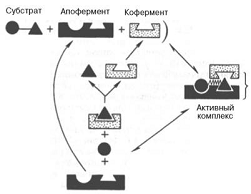
Участок фермента, содержащий такие функциональные группы, называется активным центром. В активном центре условно различают так называемый каталитический участок, непосредственно отвечающий за превращения субстратной молекулы, и контактную площадку, которая обеспечивает специфическое сродство к субстрату и формирование его комплекса с ферментом - сорбционный участок. Ферменты, связываясь с субстратом, образуют промежуточный фермент-субстратный комплекс, который затем распадается на свободный фермент и продукт реакции.
Под изоферментами понимают ферменты, катализирующие одну и ту же реакцию, но различающиеся по физическим, химическим и иммунохимическим свойствам (ранее описаны изоферменты ЛДГ).
Мультиферментные комплексы
Скорость реакций можно повысить, не увеличивая концентрации субстратов, если собрать различные участвующие в последовательных реакциях ферменты в большой мультиферментный комплекс. При таком способе организации продукт фермента А переходит непосредственно к ферменту Б и т. д. до конечного продукта, причем лимитирующая стадия диффузии отсутствует даже при очень низких внутриклеточных концентрациях промежуточных соединений.
Мультиферментный комплекс оксидаз митохондрийсостоит из 3-х компонентов.
Флавиновые дегидрогеназы. Содержат ФАД. Наиболее обычный субстрат для них - НАДФН2.
Железо-серный белок. Содержит негеминовое железо с переменной валентностью.
Цитохром Р450. Его строение отличается от строения цитохромов цепи митоходриального окисления.
Мультиферментный комплекс формирует цепь переноса электронов и протонов, в конце ее происходит активация кислорода. Активированный кислород присоединяется к активному центру цитохрома Р450, и на него переносятся электроны, а затем этот кислород включается в молекулу субстрата
Ферменты являются высокоспецифичными катализаторами; это их уникальное свойство. Ферменты проявляют специфичность в отношении типа катализируемой химической реакции. Каждый фермент катализирует определенную реакцию. Ферменты проявляют отчетливо выраженную субстратную специфичность; некоторые ферменты действуют только на один субстрат, другие - на группу родственных субстратов.
Механизмы обеспечения высокой специфичности ферментов: комплементарность, баланс между прочностью и лабильностью структуры активного центра, индуцированное связывание, многоточечность связывания субстрата в активном центре, повышение специфичности по принципу «двойного сита» в двух-субстратных реакциях.
При действии на субстраты, содержащие асимметричные центры, ферменты, как правило, проявляют стереоспецифичность. Она оказывается абсолютной в тех случаях, когда в ферментативную реакцию вовлекается асимметрический центр. Так, например, L-лактатдегидрогеназа действует только на L-лактат, в то время как D-лактатдегидрогеназа - только на D-лактат. В тех случаях, когда субстрат не содержит, а продукт содержит асимметрический атом углерода, происходит асимметрический синтез и при восстановлении пирувата L-лактатдегидрогеназой образуется только L-лактат.
Акт катализа складывается из трех последовательных этапов.
. Образование фермент-субстратного комплекса при взаимодействии через активный центр.
. Связывание субстрата происходит в нескольких точках активного центра, что приводит к изменению структуры субстрата, его деформации за счет изменения энергии связей в молекуле. Это вторая стадия и называется она активацией субстрата. При этом происходит определенная химическая модификация субстрата и превращение его в новый продукт или продукты.
. В результате такого превращения новое вещество (продукт) утрачивает способность удерживаться в активном центре фермента и фермент-субстратный, вернее уже фермент-продуктный комплекс диссоциирует (распадается).
Ферментативные эффекторы - вещества, изменяющие скорость ферментативного катализа и регулирующие за счет этого метаболизм. Среди них различают ингибиторы - замедляющие скорость реакции и активаторы - ускоряющие ферментативную реакцию.
В зависимости от механизма торможения реакции различают конкурентные и неконкурентные ингибиторы. Строение молекулы конкурентного ингибитора сходно со структурой субстрата и совпадает с поверхностью активного центра как ключ с замком (или почти совпадает). Степень этого сходства может даже быть выше чем с субстратом.Концентрация способного к катализу фермента при этом снижается и скорость образование продуктов реакции резко падает .В качестве конкурентных ингибиторов выступает большое число химических веществ эндогенного и экзогенного происхождения (т.е. образующихся в организме и поступающих извне - ксенобиотики, соответственно). Эндогенные вещества являются регуляторами метаболизма и называются антиметаболитами. Второй вид ингибиторов - неконкурентные. Они взаимодействую с ферментом вне активного центра и избыток субстрата не влияет на их ингибирующую способность, как в случае с конкурентными ингибиторами. Эти ингибиторы взаимодействуют или с определенными группами фермента (тяжелые металлы связываются с тиоловыми группами Цис) или чаще всего регуляторным центром, что снижает связывающую способность активного центра. Необратимые ингибиторы инактивируют фермент, образуя с его АК или другими компонентами структуры химическую связь. Обычно это ковалентная связь с одним из участков активного центра. Такой комплекс практически недиссоциирует в физиологических условиях. В другом случае ингибитор нарушает конформационную структуру молекулы фермента - вызывает его денатурацию. Действие обратимых ингибиторов может быть снято при переизбытке субстрата или под действием веществ, изменяющих химическую структуру ингибитора. Конкурентные и неконкурентные ингибиторы относятся в большинстве случаев к обратимым.
Помимо ингибиторов известны еще активаторы ферментативного катализа. Они:
защищают молекулу фермента от инактивирующих воздействий,
образуют с субстратом комплекс, который более активно связывается с активным центром Ф,
взаимодействуя с ферментом, имеющим
четвертичную структуру, разъединяют его субъединицы и тем самым открывают
доступ субстрату к активному центру.
Стероидные гормоны. Мужские половые
гормоны. Строение и биологическая роль гормонов
Стероиды - производные восстановленных конденсированных циклических систем - циклопентанпергидрофенантренов. В организме человека основной стероид - холестерол, остальные стероиды - его производные. Мужские половые гормоны вырабатываются в основном в мужских половых железах - в интерстициальных клетках Лейдига семенников (95%). Небольшое количество андрогенов образуется в коре надпочечников.
Путь биосинтеза андрогенов в яичках
и коре надпочечников одинаков. Предшественником андрогенов, как и других
стероидных гормонов, служит холестерол, который либо поступает из плазмы в
составе ЛПНП, либо синтезируется в самих железах из ацетил-КоА. Отщепление боковой
цепи холестерола и образование прегненолона - скорость-лимитирующая реакция.
Однако, в отличие от аналогичной реакции, протекающей в надпочечниках, эта
стадия стимулируется ЛГ (а не АКТГ). ЛГ, связываясь с рецептором плазматической
мембраны клеток Лейдига, активирует аденилатциклазу, увеличивая тем самым
внутриклеточную концентрацию цАМФ, что в конечном итоге вызывает активацию
фермента, который расщепляет боковую цепь холестерола между С-20 и С-22.
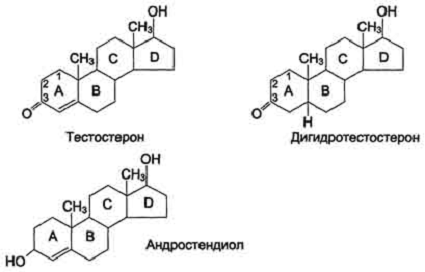
Мужские половые гормоны.
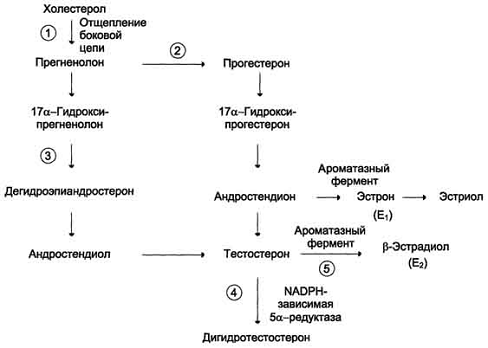
Схема синтеза половых гормонов
Суточная секреция тестостерона у мужчин составляет в норме примерно 5 мг и сохраняется на протяжении всей жизни организма. Гормон циркулирует в крови в связанном с белками плазмы состоянии: альбумином (40%) и специфически связывающим половые гормоны глобулином (называемым секс-гормонсвязывающим глобулином, СГСГ). Лишь 2% от общего количества гормона в крови транспортируется в свободном виде, и именно такие молекулы проявляют биологическую активность.
Дигидротестостерон. В семенных канальцах, предстательной железе, коже, наружных половых органах тестостерон служит предшественником более активного адцрогена - дигидротестостерона. Это превращение, в котором участвует примерно 4% тестостерона, происходит в результате восстановления двойной связи кольца А и 3-кетогруппы при участии цитоплазматического фермента - NADPH-зависимой 5α-редуктазы. Семенники человека секретируют в сутки до 50-100 мкг дигидротестостерона. Однако большее количество гормона - следствие периферических превращений, и суммарная суточная секреция дигидротестостерона составляет 400 мкг, что почти в 10 раз меньше уровня секреции тестостерона.
В некоторых периферических тканях небольшое количество тестостерона превращается в эстрадиол. В качестве побочных продуктов клетки Лейдига также постоянно секретируют эстрадиол и прогестерон, хотя роль этих гормонов в развитии и поддержании функций размножения и формирования полового поведения у мужчин до настоящего времени не выяснена.
В препубертатный период секреция андрогенов подавляет по механизму отрицательной обратной связи секрецию гонадотропина до начала пубертатного периода, когда гипофизарные клетки становятся менее чувствительными к ингибирующему действию циркулирующих в крови андрогенов. Эта потеря чувствительности приводит к циклически импульсному освобождению ЛГ и ФСГ. ЛГ, связываясь с рецепторами клеток Лейдига, стимулирует образование тестостерона интерстициальными клетками Лейдига, а ФСГ, связываясь с рецепторами клеток Сертоли в семенниках, стимулирует сперматогенез. Тестостерон замыкает отрицательную обратную связь на уровне гипофиза и гипоталамуса, уменьшая частоту секреторных импульсов ЛГ. Торможение секреции ФСГ аденогипофизом происходит под действием белка ингибина, вырабатываемого клетками Сертоли. ФСГ стимулирует синтез этого белка, который по механизму отрицательной обратной связи тормозит дальнейшую секрецию ФСГ.
К мишеням тестостерона относят эмбриональные вольфовы структуры, сперматогонии, мышцы, кости, почки, мозг. Подобно другим стероидным гормонам, андрогены образуют внутри клетки комплекс с рецептором, который связывается с определённым участком хроматина, активируя специфические гены, белковые продукты которых опосредуют биологические эффекты андрогенов.
Физиологическое действие андрогенов
различно в разные периоды жизни организма. У эмбриона под действием андрогенов
из вольфова протока образуются придаток яичка (эпидидимис), семявыносящий
проток и семенной пузырёк. У плода мужского пола происходит маскулинизация
мозга. Поскольку андрогены в организме обладают мощным анаболическим действием
и стимулируют клеточное деление, повышенный уровень андрогенов в препубертатный
период приводит к скачкообразному увеличению линейных размеров тела, увеличению
скелетных мышц, росту костей, но одновременно способствуют и остановке роста,
так как стимулируют сращение эпифизов длинных костей с их стволами. Андрогены
вызывают изменение структуры кожи и волос, снижение тембра голоса вследствие
утолщения голосовых связок и увеличения объёма гортани, стимулируют секрецию
сальных желёз.
Вода в живом организме. Состояние
воды в живых тканях, ее функции. Эндогенная вода
Вода. За небольшим исключением (кость и эмаль зубов), вода является преобладающим компонентом клеток - в среднем 75-85%. В клетке вода находится в свободном и связанном состоянии. Биологическое значение воды: растворитель (для полярных веществ, неполярные вещества в воде не растворяются); среда для реакций, участник реакций (расщепление белков), участвует в поддержании теплового равновесия клетки; источник кислорода и водорода при фотосинтезе; основное средство передвижения веществ в организме.
Вся вода, что есть в организме, разделяется на внутриклеточную и внеклеточную, каждая из которых существует в виде двух фракций:
а) фракция воды, способная к обмену;
б) фракция воды, связанная в коллоидных системах с молекулами органических веществ (белков, жиров, углеводов).
Около 66 % всей воды организма входит в состав внутриклеточной жидкости и 33 % находится вне клеток. Внеклеточная вода является основой внутрисосудистых жидкостей (лимфы, плазмы кровь) и межклеточной жидкости.
Функции воды.
Вода принимает участие в:
формировании внутриклеточных структур;
формировании пространственных конформаций молекул белков (вторичной, третичной);
многих биохимических реакциях гидролиза, гидратации, окисления, возобновление и др.;
осуществляет транспортную функцию за счет высокой растворимой способности и текучести;
принимает участие в выведении из организма продуктов разпада;
является средой для осуществления почти всех химических реакций в организме;
принимает участие в теплорегуляции путем испарения из легких и из поверхности кожи;
осуществляет механическую функцию - является компонентом смазывания трущихся поверхностей в суставах, добавляет упругости хрящам и межпозвонковым дискам;
является компонентом секретов организма: пота, мочи, слюны, молока и тому подобное.
Ткани и клетки используют два вида воды: экзо и эндогенную.
Потребность организма в воде зависит от возраста, интенсивности обменных процессов, мускульной деятельности, функционального состояния почек, температуры окружающей среды, состава еды. У взрослых она составляет в среднем 40 г на 1 кг массы тела, для детей эта величина приблизительно втрое больше - от 70 до 150 г на 1 кг массы тела. За сутки к организму в нормальных условиях поступает около 2,5 л воды, включая экзо- и эндогенную. Последняя усваивается в организме при распаде белков, углеводов и особенно жиров. При том, что при окислении 100 г жира образуется 107 мл воды, 100 г белка - 41 мл воды, 100 г углеводов - 55 мл воды.
Всасывание воды, что поступает с едой, происходит по всему желудочно-кишечному тракту: небольшое количество воды всасывается в ротовой полости и пищеводе, часть - в желудке, часть - в толстом кишечнике, основная масса - в тонком кишечнике.
Вода с питательными веществами путем
диффузии и осмоса, а частично пиноцитоза и активного транспорта, проникает
внутрь эпителия слизистых оболочек кишечника. Эндоплазматичной сетью она
перемещается в клетки и поступает в межклеточное пространство, потом в
межклеточную жидкость, капилляры, венулы, подэпителиальную и пидслизистую
венозной сетки кишечной ворсинки, воротную вену, печень и большой круг
кровообращения. Часть воды поступает через лимфатическую систему. Выведение
воды из организма осуществляется с мочой, калом, потом и выдыханием.
|
Водный баланс |
|||
|
Употребление воды |
мл |
Выделение воды |
мл |
|
Жидкости |
1500 |
Моча |
1600 |
|
Вода с пищи |
800 |
900 |
|
|
Вода с обмена веществ |
300 |
Кал |
100 |
|
Итого |
2600 |
Итого |
2600 |