Материал: Функции белков в организме. Стероидные гормоны. Липиды
Функции белков в организме. Стероидные гормоны. Липиды
КОНТРОЛЬНАЯ РАБОТА
по
дисциплине «Биохимия»
г.
План
Строение, состав и физиологическая роль отдельных органелл клетки
Напишите структурные формулы дипептидов карнозин (бета-аланилгистидин) и ансерин (бета- аланил-1- метилгистидин), опишите их функции в организме
Функции белков в организме
Классификация белков по степени сложности. Липопротеиды. Состав, строение, биологическая роль
Напишите последовательность оснований в м-РНК, образованной на цепи ДНК с последовательностью ГТГ-ГЦТ-ГЦА-ТАЦ-ЦЦГ-АГЦ-ГТГ-ГАТ-ААГ-ГТА-ГЦГ-ГЦЦ-ТЦГ-ТАГ-ТГТ-ЦТГ-ЦЦГ-АЦТ-ГЦА-ТЦА. Установите последовательность аминокислот в пептиде
Привести структурную формулу витамина С, указать его физико-химические характеристики (агрегатное состояние, растворимость в воде и органических растворителях, влияние температуры, кислотности среды и солнечного облучения на стабильность витамина), пояснить, в какой кофермент оно включается в организме или не включается, подчеркнуть биологическую роль витамина, а также его минимальную норму потребления в сутки в составе продуктов питания, указать источник витамина, признаки гипер - и авитаминоза
Привести структурную формулу витамина В6 (пиридоксин), указать его физико-химические характеристики (агрегатное состояние, растворимость в воде и органических растворителях, влияние температуры, кислотности среды и солнечного облучения на стабильность витамина), пояснить , в какой кофермент оно включается в организме или не включается, подчеркнуть биологическую роль витамина, а также его минимальную норму потребления в сутки в составе продуктов питания, указать источник витамина, признаки гипер- и авитаминоза
Механизм ферментативного катализа
Стероидные гормоны. Мужские половые гормоны. Строение и биологическая роль гормонов
Вода в живом организме. Состояние воды в живых тканях, ее функции. Эндогенная вода
Полисахариды морских водорослей. Состав, строение. Функции в организме
Классификация липидов. Сложные липиды. Фосфолипиды. Строение. Распространение. Биологическая роль
Литература
гормон липид белок органелла
Строение, состав и физиологическая роль
отдельных органелл клетки
Основными компонентами клетки являются: наружная клеточная мембрана, цитоплазма и ядро. Клеточная мембрана - это оболочка клетки, выполняющая следующие функции:
разделение содержимого клетки и внешней среды;
регуляция обмена веществ между клеткой и средой;
место протекания некоторых биохимических реакций (в том числе фотосинтеза <#"870672.files/image001.gif">
Они увеличивают амплитуду мышечного сокращения, предварительно сниженную утомлением. Имидазолсодержащие дипептиды не влияют непосредственно на сократительный аппарат, но увеличивают эффективность работы ионных насосов мышечной клетки.
Карнозин участвует в процессах фосфорилирования, происходящего в мышцах при образовании фосфатных соединений. Карнозин является естественным дипептидом, который находится в мышечных волокнах обоих типов - 1 и 2 (медленные и быстрые) . Но в значительно более высоких концентрациях он содержится в волокнах 2 типа. Именно этот тип является наиболее чувствительным к мышечному росту.
Ансерин также связан с физиологической
функцией мышц: появление его в мышечной ткани совпадает по времени с
формированием их сократительной функции; мышцы, несущие большую функциональную
нагрузку, содержат больше ансерина.
Функции белков в организме
Белки занимают центральное место в метаболизме организма человека, выполняя ряд важных функций:
) структурную или пластическую (структурная основа клеток, органеллы, фибриллярные белки);
) транспортную (липопротеиды, гемоглобин, альбумин);
) сократительную (мышечные белки - актин, миозин);
) каталитическую (ферменты);
) регуляторную (гормоны);
) защитную (иммуноглобулины, антитела, интерферон; белки системы свертывания крови и фибринолиза);
) энергетическую (распад аминокислот обеспечивает до 18% потребляемой энергии).
Пример:
В плазме крови содержится 7% всех
белков организма при концентрации 60 - 80 г/л. Белки плазмы крови выполняют
множество функций. Альбумин, транстиретин, транскортин, трансферрин и некоторые
другие белки вьшолняют транспортную функцию.
|
руппа |
Белки |
Концентрация в сыворотке крови, г/л |
Функция |
|
Альбумины |
Транстиретин |
0,25 |
Транспорт тироксина и трийодтиронина |
|
|
Альбумин |
40 |
Поддержание осмотического давления, транспорт жирных кислот, билирубина, жёлчных кислот, стероидных гормонов, лекарств, неорганических ионов, резерв аминокислот |
|
|
ЛПВП |
0,35 |
Транспорт холестерола |
|
|
Транскортин |
0,03 |
Транспорт кортизола, кортикостерона, прогестерона |
|
|
Кислый α1-гликопротеин |
1 |
Транспорт прогестерона |
|
|
Тироксинсвязывающий глобулин |
0,02 |
Транспорт тироксина и трийодтиронина |
|
α2-Глобулины |
Церулоплазмин |
0,35 |
Транспорт ионов меди, оксидоредуктаза |
|
|
1 |
Связывание гемоглобина |
|
|
|
α2-Макроглобулин |
2,6 |
Ингибитор плазменных протеиназ, транспорт цинка |
|
|
Ретинолсвязывающий белок |
0,04 |
Транспорт ретинола |
|
|
Витамин D связывающий белок |
0,4 |
Транспорт кальциферола |
|
β-Глобулины |
ЛПНП |
3,5 |
Транспорт холестерола |
|
|
Трансферрин |
3 |
Транспорт ионов железа |
|
|
Транскобаламин |
25×10-9 |
Транспорт витамина B12 |
|
|
Глобулин связывающий белок |
20×10-6 |
Транспорт тестостерона и эстрадиола |
Классификация белков по степени сложности.
Липопротеиды. Состав, строение, биологическая роль
Простые белки состоят только из аминокислот, а сложные белки содержат, кроме аминокислот, другие небелковые вещества,, например, углеводы, липиды, нуклеиновые кислоты и др.
Липопротеиды.
Этот класс сложных беков состоит из белка и простетической группы, представленной каким-либо липидом. Белковая группа гидрофильна, а простетическая гидрофобна, что и играет роль в организации мембран и их избирательной проницаемости. В частности, в составе липопротеинов открыты нейтральные жиры (триглицериды), свободные жирные кислоты, фосфолипиды, холестериды. Липопротеины широко распространены в природе и выполняют разнообразные биологические функции. Они входят в состав клеточной мембраны и внутриклеточных биомембран ядра, митохондрий, микросом (структурированные липопротеины), а также присутствуют в свободном состоянии (главным образом в плазме крови). К липопротеинам относятся, кроме того, тромбопластический белок ткани легких, липовителлин желтка куриного яйца, некоторые фосфолипиды молока и т.д. Установлено, что липопротенины участвуют в структурной, комплексной организации миелиновых оболочек, нервной ткани, фоторецепторной и электронно-транспортной систем, палочек и колбочек сетчатки и др.
Большинство ЛП синтезируется в печени или в слизистой оболочке кишечника. Они содержат гидрофобное липидное ядро, окруженное полярными липидами и оболочкой из белков, получивших название апобелки. Обычно ЛП содержат до 5% углеводов (глюкоза, галактоза, гексозамины, сиаловая кислота), поэтому некоторые из них являются и гликопротеинами.
Триглицериды, холестерин, эфиры холестерина и фосфолипиды транспортируются в форме водорастворимых липопротеидов. Липопротеиды - это сферические частицы, состоящие из гидрофобной сердцевины и гидрофильной оболочки. Сердцевина содержит неполярные липиды - триглицериды и эфиры холестерина. Оболочка построена из полярных липидов - холестерина и фосфолипидов, причем заряженные концы этих молекул обращены наружу. Кроме того, в состав оболочки входят белки, нековалентно связанные с фосфолипидами и холестерином, - апопротеины. Апопротеины поддерживают структуру липопротеидных частиц и обеспечивают их взаимодействие с рецепторами липопротеидов. Липопротеиды подразделяют на несколько классов в зависимости от их плотности и подвижности при электрофорезе. Плотность липопротеидной частицы определяется отношением апопротеины/липиды: чем больше это отношение, тем выше плотность. В крови, взятой натощак, присутствуют только ЛПОНП, ЛПНП и ЛПВП, тогда как другие липопротеиды (хиломикроны, остаточные компоненты хиломикронов, а также ЛППП) выявляются только после еды или при нарушениях обмена липидов. ЛПОНП образуются главным образом в печени. Это основная транспортная форма эндогенных триглицеридов, синтезирующихся в печени. ЛПОНП - главный поставщик триглицеридов для скелетных мышц и миокарда. В состав ЛПОНП входят апопротеины C, E и B100. По сравнению с хиломикронами, ЛПОНП содержат меньше триглицеридов, но больше холестерина и эфиров холестерина. Известно, что развитие атеросклероза ускоряется на фоне повышенной концентрации ЛПОНП при сахарном диабете и болезнях почек.
ЛППП. В капиллярах скелетных мышц, миокарда и жировой ткани ЛПОНП расщепляются липопротеидлипазой с образованием ЛППП. ЛППП содержат апопротеины E и B100. В печени половина ЛППП превращается в ЛПНП под действием триацилглицероллипазы, а оставшиеся ЛППП связываются с рецепторами гепатоцитов, подвергаются эндоцитозу и разрушаются.
ЛПНП являются конечными продуктами расщепления ЛПОНП и ЛППП. ЛПНП - это самые атерогенные липопротеиды. В составе ЛПНП содержится примерно две трети всего холестерина плазмы, преимущественно в виде эфиров холестерина. В отличие от других липопротеидов, ЛПНП содержат только один апопротеин - B100. Избыток ЛПНП - один из главных факторов риска атеросклероза.
ЛПВП синтезируются в печени и кишечнике и
содержат эфиры холестерина и фосфолипиды. Важнейшая функция ЛПВП - удаление
холестерина из тканей. Связывание ЛПВП с рецепторами вызывает выброс
холестерина из клеток. Первоначально холестерин встраивается в оболочку ЛПВП,
но затем под действием лецитинхолестерин-ацилтрансферазы он этерифицируется и
перемещается в сердцевину ЛПВП. В печени ЛПВП связываются с рецепторами и
разрушаются. Таким образом, ЛПВП - это антиатерогенные липопротеиды.
Напишите последовательность оснований в м-РНК,
образованной на цепи ДНК с последовательностью
ГТГ-ГЦТ-ГЦА-ТАЦ-ЦЦГ-АГЦ-ГТГ-ГАТ-ААГ-ГТА-ГЦГ-ГЦЦ-ТЦГ-ТАГ-ТГТ-ЦТГ-ЦЦГ-АЦТ-ГЦА-ТЦА.
Установите последовательность аминокислот в пептиде
Генетический код - система записи генетической информации в ДНК в виде определенной последовательности нуклеотидов. Последовательность нуклеотидов определяет последовательность включения АК в синтезируемый белок. 3 нуклеотида - триплет - кодон - кодируют 1 АК. Совокупность триплетов и составляет генетический код.
в ДНК содержится тимин, а в РНК - урацил.
В качестве азотистых оснований в РНК присутствуют урацил, цитозин, аденин и тимин
Заменяем цитозин на гуанин, гуанин на цитозин, тимин на аденин, аденин на урацил
ГТГ-ГЦТ-ГЦА-ТАЦ-ЦЦГ-АГЦ-ГТГ-ГАТ-ААГ-ГТА-ГЦГ-ГЦЦ-ТЦГ-ТАГ-ТГТ-ЦТГ-ЦЦГ-АЦТ-ГЦА-ТЦА.
М-РНК
ЦАЦ-ЦГА-ЦГУ-АУГ-ГГЦ-УЦГ-ЦАЦ-ЦУА-УУЦ-ЦАУ-ЦГЦ-ЦГГ-АГЦ-АУЦ-АЦА-ГАЦ-ГГЦ-УГА-ЦГУ-АГУ.
Пептид:
ГИС-ТРЕГ-
АРГ-МЕТ-ГЛИ-СЕР-ГИС-ЛЕЙ-ФЕН-ГИС-АРГ-АРГ-СЕР-ИЛЕЙ-ТРЕ-АСП-ГЛИ-СТОП-АРГ-СЕР
Привести структурную формулу витамина С, указать
его физико-химические характеристики (агрегатное состояние, растворимость в
воде и органических растворителях, влияние температуры, кислотности среды и
солнечного облучения на стабильность витамина), пояснить, в какой кофермент оно
включается в организме или не включается, подчеркнуть биологическую роль
витамина, а также его минимальную норму потребления в сутки в составе продуктов
питания, указать источник витамина, признаки гипер - и авитаминоза
По физическим свойствам аскорбиновая кислота
представляет собой белый кристаллический порошок кислого вкуса. Легко растворим
в воде, растворим в спирте. Легко тразлагается при нагревании, в кислой среде
более устойчива. Аскорбиновая кислота или витамин С получила название
антискорбутного, антицинготного фактора, предохраняющего от развития цинги -
болезни, принимавшей в средние века характер эпидемии. По химической структуре
аскорбиновая кислота представляет собой лактон кислоты со структурой, близкой структуре
L-глюкозы. Аскорбиновая кислота относится к сильным кислотам; кислый характер
ее обусловлен наличием двух обратимо диссоциирующих енольных гидроксилов у 2-го
и 3-го углеродных атомов.
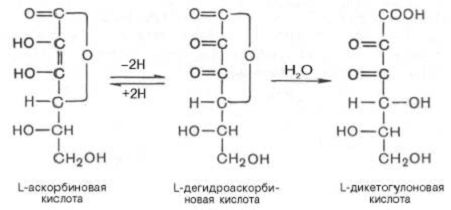
Из представленных структурных формул видно, что наиболее важным химическим свойством аскорбиновой кислоты <#"870672.files/image003.gif">
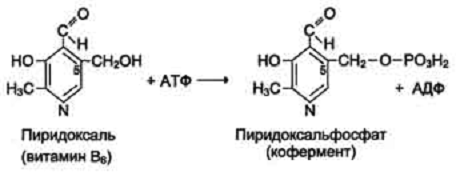
Все формы витамина В6 используются в организме
для синтеза коферментов: пиридоксальфосфата и пиридоксаминфосфата. Коферменты
образуются путём фосфорилирования по гидроксиметильной группе в пятом положении
пиримидинового кольца при участии фермента пиридоксалькиназы и АТФ как
источника фосфата.
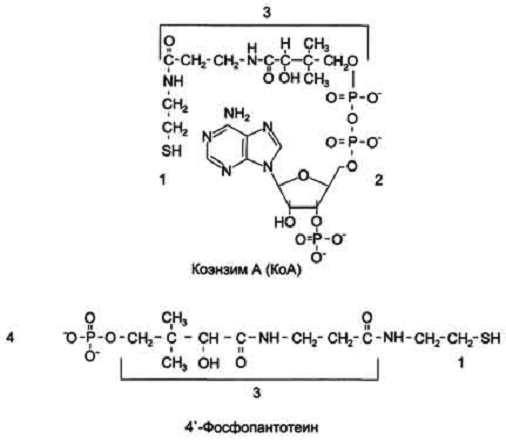
Строение КоА и 4'-фосфопантотеина. 1 - тиоэтаноламин; 2 - аденозил-3'-фосфо-5'-дифосфат; 3 - пантотеновая кислота; 4 - 4'-фосфопантотеин (фосфорилированная пантотеновая кислота, соединённая с тиоэтаноламином).
Все 3 формы витамина - бесцветные кристаллы, хорошо растворимые в воде. Пиридоксин довольно устойчив даже при нагревании в присутствии кислот и щелочей, он хорошо растворим в этиловом спирте и воде. Однако при воздействии солнечных лучей витамин В6 быстро разрушается. Все формы витамина В6 (пиридоксин, пиридоксаль и пиридоксамин) реагируют как основания с кислотами, образуя соли. Он обладает горьковато-кислым вкусом.
Пиридоксалевые ферменты играют ключевую роль в
обмене аминокислот: катализируют реакции трансаминирования и
декарбоксилирования аминокислот, участвуют в специфических реакциях метаболизма
отдельных аминокислот: серина, треонина, триптофана, серосодержащих
аминокислот, а также в синтезе гема. Пиридоксальфермент катализирует реакцию
переаминирования. В результате серии реакций, включающих в себя образование
фермент-субстратных комплексов с гистидинаминотрансферазой, гистидин переходит
в оксогистидин, а глиоксилевая килотая - в глицин. Над стрелкой внизу -
схематически группа лизина от ферментного белка
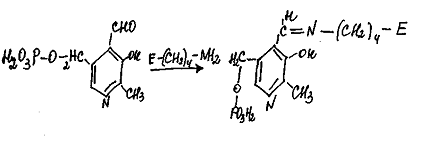
Взаимодействие между субстратом
<#"870672.files/image007.gif">
Пиридоксаминфосфат на второй стадии
реакции реагирует с α-кетокислотой
- глиоксилевой, что через те же стадии образования промежуточных соединений
(идущих в обратном направлении) приводит к синтезу новой аминокислоты
<#"870672.files/image008.gif">
Авитаминоз В6 у детей проявляется повышенной возбудимостью ЦНС, периодическими судорогами, что связано, возможно, с недостаточным образованием тормозного медиатора ГАМК, специфическими дерматитами. У взрослых признаки гиповитаминоза В6 наблюдают при длительном лечении туберкулёза изониазидом (антагонист витамина В6). При этом возникают поражения нервной системы (полиневриты), дерматиты.
Источники витамина В6 для человека - такие продукты питания, как яйца, печень, молоко, зеленый перец, морковь, пшеница, дрожжи. Некоторое количество витамина синтезируется кишечной флорой.
Содержание пиридоксина в 100 граммах продукта составляет: в печени - 0,9 мг, в постном мясе (говядина, телятина) - примерно 0,3 мг, в мясе птицы - 0,17 мг, в рыбе - не менее 0,39 мг, в соевых бобах - около 0,86 мг, в грецких орехах - не менее 0,68 мг, в пророщенных зёрнах пшеницы - 0,72 мг, в бананах - не менее 0,34 мг, в авокадо - 0,22 мг, в шпинате - 0,25 мг, в отрубях - 0,17 мг.