Материал: fizika (1)
Charm с. Квантовое число с может принимать значения -3, -2, -1, 0, +1, +2, +3. В настоящее время обнаружены частицы, имеющие с = 0, +1 и -1. Например, барион Λ+ имеет с = +1.
Bottomness b. Квантовое число b может принимать значения -3, -2, -1, 0, +1, +2, +3. В настоящее время обнаружены частицы, имеющие b = 0, +1, -1. Например, В+-мезон имеет b = +1.
Topness t. Квантовое число t может принимать значения -3, -2, -1, 0, +1, +2, +3. В настоящее время обнаружено всего одно состояние с t = +1.
Изоспин I. Сильновзаимодействующие частицы можно разбить на группы частиц, обладающих схожими свойствами (одинаковое значение спина, чётности, барионного числа, странности и др. квантовых чисел, сохраняющихся в сильных взаимодействиях) - изотопические мультиплеты. Величина изоспина I определяет число частиц, входящих в один изотопический мультиплет, n и р составляет изотопический дуплет I = 1/2; Σ+, Σ-, Σ0, входят в состав изотопического триплета I = 1, Λ - изотопический синглет I = 0, число частиц, входящих в один изотопический мультиплет, 2I + 1.
G - четность - это квантовое число, соответствующее симметрии относительно одновременной операции зарядового сопряжения с и изменения знака третьего компонента I изоспина. G-четность сохраняется только в сильных взаимодействиях.
Античасти́ца — частица-двойник некоторой другой элементарной частицы, обладающая той же массой и тем же спином, отличающаяся от неё знаками всех других характеристик взаимодействия[1] (зарядов, таких как электрический[2] и цветовой заряды, барионное и лептонное квантовые числа).
3. 1. Строение атомного ядра, его размеры, Нуклоны, их масса в единицах энергии. Известные в природе типы сил (или взаимодействий), и их количественное соотношение, характерные времена.
Атом состоит из ядра и окружающего его электронного "облака". Находящиеся в электронном облаке электроны несут отрицательныйэлектрический заряд. Протоны, входящие в состав ядра, несут положительный заряд.
В любом атоме число протонов в ядре в точности равно числу электронов в электронном облаке, поэтому атом в целом – нейтральная частица, не несущая заряда.
Атом может потерять один или несколько электронов или наоборот – захватить чужие электроны. В этом случае атом приобретает положительный или отрицательный заряд и называется ионом.
Практически вся масса атома сосредоточена в его ядре, так как масса электрона составляет всего лишь 1/1836 часть массы протона. Плотность вещества в ядре фантастически велика – порядка 1013 - 1014 г/см3. Спичечный коробок, наполненный веществом такой плотности, весил бы 2,5 миллиарда тонн!
Внешние размеры атома – это размеры гораздо менее плотного электронного облака, которое примерно в 100000 раз больше диаметра ядра.
Кроме протонов, в состав ядра большинства атомов входят нейтроны, не несущие никакого заряда. Масса нейтрона практически не отличается от массы протона. Вместе протоны и нейтроны называются нуклонами (от латинского nucleus – ядро).
Электроны, протоны и нейтроны являются главными "строительными деталями" атомов и называются субатомными частицами. Их заряды и массы в кг и в специальных “атомных” единицах массы (а.е.м.) показаны в таблице 2-1.
Таблица :Субатомные частицы.
Частица |
Заряд |
Масса: |
|
|
|
кг |
а.е.м. |
Протон |
+1 |
1,67·10-27 |
1,00728 |
Нейтрон |
0 |
1,67·10-27 |
1,00867 |
Электрон |
-1 |
9,11·10-31 |
0,000549 |
2. Квантовые числа (главное, орбитальное, спиновое). Распределение электронной плотности в атоме, орбитали, заполнение электронов в элементах периодической таблицы.
Электроны могут находиться в атоме водорода, только имея определенные значения энергии. Состояния с другими значениями трактуются как неустойчивые (нестационарные), поэтому при E≠En, электрон должен излучать или поглощать энергию, с тем, чтобы перейти в одно из состояний, дозволенных для него при данных условиях.
Решение уравнения Шредингера для атома водорода приводит к появлению дискретных энергетических уровней (как и в случае с потенциальной ямой).
Собственные
функции уравнения содержат три
целочисленных параметра n,
l
и m.
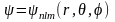 .
Таким образом существует столько
квантовых чисел, сколько степеней
свободы имеет электрон — три квантовых
числа определяют поведение волновой
функции Ψ в пространстве.
.
Таким образом существует столько
квантовых чисел, сколько степеней
свободы имеет электрон — три квантовых
числа определяют поведение волновой
функции Ψ в пространстве.
Главное квантовое число n.
Уровни энергии, соответствующие различным квантовым состояниям, зависят только от n:
Параметр n называют главным квантовым числом, которое отражает удаленность электронного слоя от ядра и запас энергии электронов в этом слое. Чем больше значение n, тем «размазаннее» электронное облако и больше энергия электронов.
Орбитальное квантовое число l.
Совместно с n определяет форму орбиты.
Поскольку каждому возможному значению энергии соответствует в возбужденном состоянии несколько орбит, состояния получили названия вырожденных. Все состояния за исключением низшего вырождены.
Параметр l называют орбитальным или азимутальным квантовым числом, характеризующим форму электронного облака и определяющим момент количества движения по орбите L:
Число l принимает значения 0, 1, 2…(n-1), т.е. для данного значения главного квантового числа n существует n значений орбитального числа l=0,1,2…(n-1).
М
 агнитное
квантовое число m.
агнитное
квантовое число m.
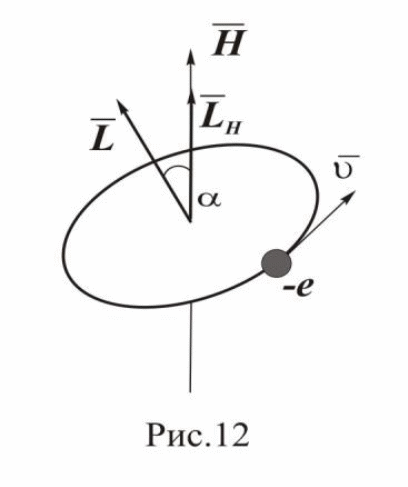
Магнитное квантовое число определяет ориентацию электронной орбиты относительно направления магнитного поля. В квантовой механике строго доказано, что существует пространственное квантование: вектор момента импульса L электрона имеет лишь такие ориентации в пространстве, при которых проекция LH вектора L на направление внешнего магнитного поля H принимает квантованные, целочисленные значения, кратные ħ=h/2π: LH=mh/2π, где m — магнитное квантовое число, которое может принимать значения 0,±1,±2…±l (l — орбитальное квантовое число).
Квантовые числа n, l и m создают различные квантовые состояния атома водорода, для которых получается различное распределение электронной плотности. Боровские орбиты электрона представляют собой геометрические места точек, в которых с наибольшей вероятностью может быть обнаружен электрон.
Спиновое квантовое число s.
Четвертое спиновое квантовое число определяется ориентацией собственного момента количества движения электрона относительно орбитального момента L.
Спин
является квантуемой величиной
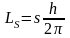 ,
где s=±1/2
квантовое число собственного механического
момента электрона.
,
где s=±1/2
квантовое число собственного механического
момента электрона.
4. 1. Принцип неопределенности Гейзенберга. Волновая функция, вероятность нахождения частицы, определение среднего значения величины.
Своеобразие свойств микрочастиц проявляется в том, что не для всех переменных получаются при измерениях определенные значения. Так, например, электрон (и любая другая микрочастица) не может иметь одновременно точные значения координаты х и импульса р.
Массы субатомных частиц чрезвычайно малы. Показатель степени (например, десять в минус двадцать седьмой степени) показывает, сколько нулей после запятой нужно записать, чтобы получилась десятичная дробь, выражающая массу субатомной частицы в килограммах. Это ничтожнейшая часть килограмма, поэтому массу субатомных частиц удобнее выражать в атомных единицах массы (сокращенно – а.е.м.). За атомную единицу массы принята ровно 1/12 часть массы атома углерода, в ядре которого содержится 6 протонов и 6 нейтронов. Схематическое изображение такого "эталонного" атома углерода приведено на рис. 2-5 (б). Атомную единицу массы можно выразить и в граммах: 1 а.е.м. = 1,660540·10-24 г.
А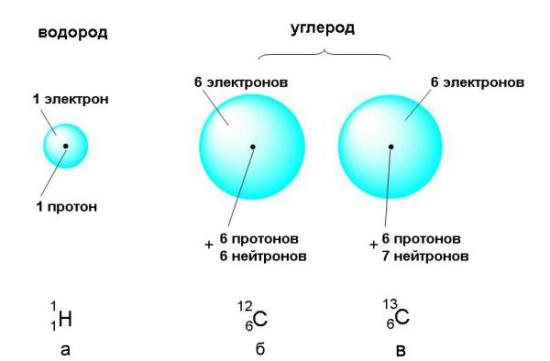 томы
состоят из положительно заряженного
ядра и электронного облака. а)
В состав ядра атома водорода входит
только 1 протон, а электронное облако
заполняется одним электроном. б)
В ядре атома углерода 6 протонов и 6
нейтронов, а в электронном облаке – 6
электронов. в)
Существует также изотопный
углерод, ядре которого на 1 нейтрон
больше.
Содержание этого изотопа в природном
углероде составляет чуть более 1% (об
изотопах см. ниже). Линейные размеры
атомов очень малы: их радиусы составляют
от 0,3 до 2,6 ангстрема (1 ангстрем = 10–8
см). Радиус ядра около 10–5
ангстрема, то есть 10–13
см. Это в 100000 раз меньше размеров
электронной оболочки. Поэтому правильно
показать относительные пропорции ядер
и электронных оболочек на рисунке
невозможно. Если бы атом увеличился до
размеров Земли, то ядро имело бы всего
около 60 м в диаметре и могло бы поместиться
на футбольном поле.
томы
состоят из положительно заряженного
ядра и электронного облака. а)
В состав ядра атома водорода входит
только 1 протон, а электронное облако
заполняется одним электроном. б)
В ядре атома углерода 6 протонов и 6
нейтронов, а в электронном облаке – 6
электронов. в)
Существует также изотопный
углерод, ядре которого на 1 нейтрон
больше.
Содержание этого изотопа в природном
углероде составляет чуть более 1% (об
изотопах см. ниже). Линейные размеры
атомов очень малы: их радиусы составляют
от 0,3 до 2,6 ангстрема (1 ангстрем = 10–8
см). Радиус ядра около 10–5
ангстрема, то есть 10–13
см. Это в 100000 раз меньше размеров
электронной оболочки. Поэтому правильно
показать относительные пропорции ядер
и электронных оболочек на рисунке
невозможно. Если бы атом увеличился до
размеров Земли, то ядро имело бы всего
около 60 м в диаметре и могло бы поместиться
на футбольном поле.
mпротона-938,28 МэВ^2
mэлектрона-0,511 МэВ^2
mнейтрона-939,57 МэВ^2
Виды взаимодейстия – все полностью про это на моей бумажке про элементарные части хорошо класс.
Неопределенности координат и импульса удовлетворяют соотношению В. Гейзенберга:
![]()
где х и р — неопределенности значений х и р, являющиеся среднеквадратичными отклонениями.
Это выражение называется соотношением неопределенностей или принципом неопределенности.
Этот принцип утверждает, что если частица локализована в пространстве со среднеквадратичным отклонением х, то ее импульс может принимать значения, находящиеся в пределах «ширины» р.
Физический смысл принципа неопределенности состоит в том, что невозможно одновременно определить
значения координаты и импульса частицы.
Электроны, фотоны, нейтроны и другие микрочастицы в одних случаях ведут себя как частицы, в других проявляют свои волновые свойства. Это значит, что объекты микромира не являются ни классическими частицами, ни классическими волнами, и для изучения их свойств не применимы классические методы описания частиц и волн.
Соотношение неопределенности Гейзенберга показывает, что в микромире для квантовых объектов, чем точнее определено значение координаты частицы, тем менее точно определено значение импульса частицы и наоборот.
Δx·Δpx≥h
Микрочастицы не имеют одновременно точного значения координаты и соответствующей проекции импульса. Соотношение неопределенностей позволяет оценить, в какой мере можно применять к микрочастицам понятия классической механики. Оно показывает, что к микрообъектам неприменимо классическое понятие траектории (т.к. движение по траектории характеризуется в любой момент времени определенными значениями координат и скорости).
2. Понятие оператора физической величины, собственных значений. Оператор импульса, кинетической энергии. Уравнение Шрёдингера.
5. 1. Рентгеновское излучение (тормозное и характеристическое), вид спектров, механизм возникновения, закон Мозли. Получение рентгеновского излучения, его применение. Взаимодействие рентгеновского излучения с веществом.
Р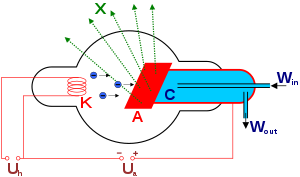 ентгеновское
излучение — эм волны, энергия фотонов
которых лежит на шкале эм волн между уф
и гамма-излучением. Оно возникает при
воздействии на вещество быстрых
электронов.
ентгеновское
излучение — эм волны, энергия фотонов
которых лежит на шкале эм волн между уф
и гамма-излучением. Оно возникает при
воздействии на вещество быстрых
электронов.
Источник: рентгеновская трубка. При взаимодействии электронов с материалом антикатода образуется рентгеновское излучение.
Различают два типа рентгеновского излучения: тормозное и характеристическое. Тормозное излучение образует сплошной спектр, возникающий при торможении быстрых электронов в веществе антикатода.
Характеристическое излучение появляется при повышении напряжения на трубке. Образуется линейчатый спектр, который состоит из отдельных линий и зависит от веществ, из которых состоит антикатод. Каждый элемент обладает характерным линейчатым спектром.
Особенности характеристических спектров:
При увеличении атомного номера Z элемента спектр монотонно смещается в коротковолновую часть.
Спектры разных элементов имеют сходный характер.
Состоят из нескольких серий: K, L, M, N, O. Каждая серия насчитывает небольшое количество линий Kα, Kβ, … .
Закон Мозли — соотношение между длиной волны (или частотой) рентгеновского излучения и атомным номером элемента. Чем больше атомный номер элемента, тем меньше длина волны характеристической линии.
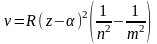 ,
где α
— const,
своя для каждой серии, R
— постоянная Ридберга, m=1,2,3…
(определяет рентгеновскую серию),
n=m+1,m+2…(определяет
линию соответствующей серии), a
— постоянная, имеющая определенное
значение для каждой линии.
,
где α
— const,
своя для каждой серии, R
— постоянная Ридберга, m=1,2,3…
(определяет рентгеновскую серию),
n=m+1,m+2…(определяет
линию соответствующей серии), a
— постоянная, имеющая определенное
значение для каждой линии.
α — постоянная экранирования. Ее смысл: электроны атома находятся под действием ядра, притяжение которого ослабевает под действием остальных электронов, окружающих его. На электрон, совершающий переход, действует не весь заряд ядра Ze, а заряд (Z-α)e, ослабленный экранирующим действием других электронов.
Закон Мозли устанавливает линейную связь между квадратным корнем из обратной длины волны спектральных линий и атомным номером элемента. Эта связь позволяет по измененной длине волны точно установить атомный номер данного элемента, и значит заряд его ядра.
Этот закон сыграл важную роль при уточнении расположения элементов в периодической системе.
В соответствии с Законом Мозли, рентгеновские характеристические спектры не обнаруживают периодических закономерностей, присущих оптическим спектрам. Это указывает на то, что проявляющиеся в характеристических рентгеновских спектрах внутренние электронные оболочки атомов всех элементов имеют аналогичное строение.
В зависимости от ряда факторов — от числа нуклонов в ядре атома (изотопический сдвиг), состояния внешних электронных оболочек (химический сдвиг) и пр. — положение спектральных линий на диаграмме Мозли может несколько изменяться. Изучение этих сдвигов позволяет получать детальные сведения об атоме.
Взаимодействие рентгеновского излучения с веществом.
В зависимости от энергии фотона hv и энергии ионизации Au атомов вещества различают три процесса:
Когерентное (классическое) рассеяние. Рассеяние длинноволнового рентгеновского излучения происходит без изменения длины волны. Оно возникает, если энергия фотона меньше энергии ионизации hv< Au. Т.к. в этом случае энергия фотона рентгеновского излучения и энергия атома не изменяются, то когерентное рассеяние не вызывает биологического действия. Тем не менее при создании защиты от рентгеновского излучения нужно учитывать возможность направления первичного пучка. Этот вид взаимодействия имеет значение для структурного аналазиа.
Некогерентное рассеяние (эффект Комптона). Рассеяние рентгеновского излучения с изменением длины волны — некогерентное, а само явление — эффект Комптона. Он возникает, если энергия фотона рентгеновского излучения больше энергии ионизации hv> Au. При взаимодействии с атомом энергия фотона расходуется на образование нового рассеянного фотона рентгеновского излучения с энергией hv’, на отрыв электрона от атома (энергия ионизации Au) и сообщение электрону кинетической энергии Ek: hv=hv’+ Au+Ek. В этом явлении наряду с вторичным рентгеновским излучением появляются электроны отдачи с кинетической энергией. Атомы или молекулы вещества становятся ионами.
Фотоэффект. При фотоэффекте рентгеновское излучение поглощается атомом, в результате чего вылетает электрон, а атом ионизируется. Если энергия фотона недостаточна для ионизации, то фотоэффект проявляется в возбуждении атома без вылета электрона.