Материал: fizika (1)
ml – характеризует ориентацию электронного облака (орбиты) в пространстве:
Главное квaнтовое число n определяет общую энергию электрона и степень его удаления от ядра (номер энергетического уровня); оно принимает любые целочисленные значения, начиная с 1 (n = 1, 2, 3, . . .)
Орбитальное (побочное или азимутальное) квантовое число l определяет форму атомной орбитали. Определяет момент импульса в электроне. Оно может принимать целочисленные значения от 0 до n-1 (l = 0, 1, 2, 3,..., n-1). Каждому значению l соответствует орбиталь особой формы.
Орбитали с l = 0 называются s-орбиталями, l =1 - р-орбиталями (3 типа, отличающихся магнитным квантовым числом m), l = 2 - d-орбиталями (5 типов), l = 3 - f-орбиталями (7 типов).
Магнитное квантовое число m определяет направление орбитали в пространстве. Его значения изменяются от +l до - l, включая 0. Например, при l = 1 число mпринимает 3 значения: +1, 0, -1, поэтому существуют 3 типа р-АО: px, py, pz.
Спиновое квантовое число s может принимать лишь два возможных значения +1/2 и -1/2. Они соответствуют двум возможным и противоположным друг другу направлениям собственного магнитного момента электрона.
В нормальном (невозбужденном) состоянии атома электроны должны располагаться на самых низких доступных для них энергетических уровнях. Поэтому, казалось бы, в любом атоме в нормально состоянии все электроны должны быть в состоянии 1s (n=1,l=0). Но это не так.
Почему? Принцип Паули. Формулировка принципа Паули, которая и была введена им в квантовую теорию (1925 г.) еще до построения квантовой механики: в одном и том же атоме (или в какой-либо квантовой системе) не может быть двух электронов, обладающих одинаковой совокупностью четырех квантовых чисел: n, l, m, ms - одновременно два электрона не могут находиться в одном и том же состоянии.
Принцип Паули утверждает, что два электрона, связанные в одном и том же атоме различаются значениями, по крайней мере, одного квантового числа.
М аксимальное
число электронов, находящихся в
состояниях, описываемых набором трех
квантовых чисел n,
l
и m,
и отличающихся только ориентацией
спинов электронов равно 2.
аксимальное
число электронов, находящихся в
состояниях, описываемых набором трех
квантовых чисел n,
l
и m,
и отличающихся только ориентацией
спинов электронов равно 2.
Спиновое число может принимать только 2 значения, поэтому в состояниях с данным значением n могут находиться в атоме не более 2n2 электронов:
С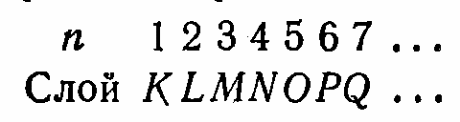 овокупность
электронов в многоэлектронном атоме,
имеющих одно и то же главное квантовое
число n,
называется электронной
оболочкой
или слоем.
Оболочки подразделяются на подоболочки,
отличающиеся значением квантового
числа l.
овокупность
электронов в многоэлектронном атоме,
имеющих одно и то же главное квантовое
число n,
называется электронной
оболочкой
или слоем.
Оболочки подразделяются на подоболочки,
отличающиеся значением квантового
числа l.
Область пространства, в которой высока вероятность обнаружить электрон, называют подоболочкой или орбиталью. Вид основных типов орбиталей показан на рисунке:
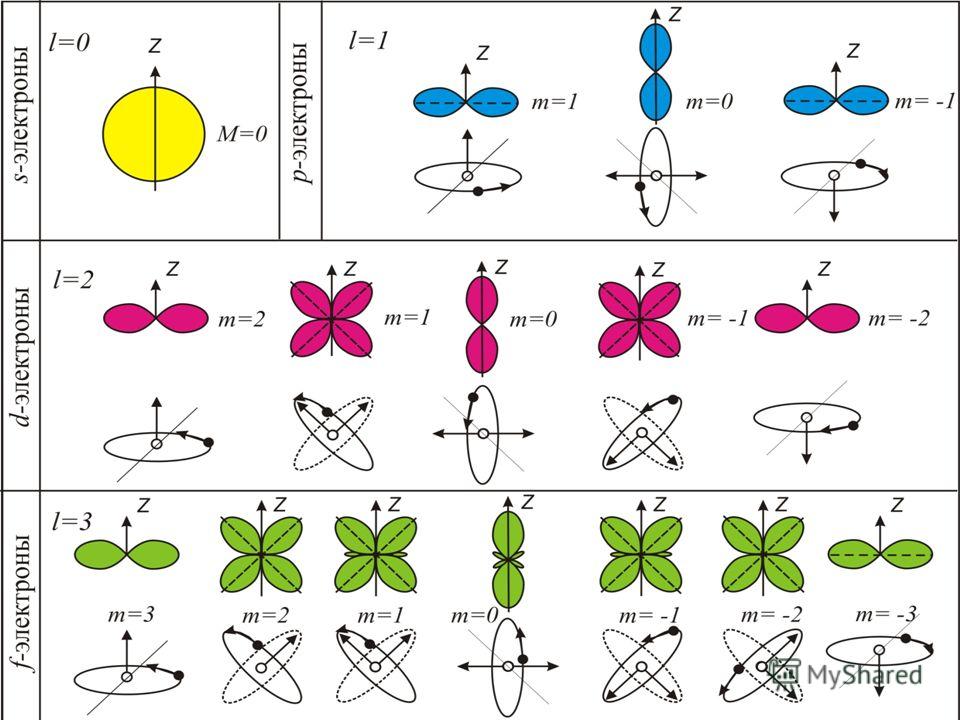
Поскольку орбитальное квантовое число принимает значения от 0 до -1, число подоболочек равно порядковому номеру n оболочки. Количество электронов в подоболочке определяется магнитным и спиновым квантовыми числами: максимальное число электронов в подоболочке с данным l равно 2(2l + 1). Обозначения оболочек, а также распределение электронов по оболочкам и подоболочкам приведено в таблице
Главное квантовое число n |
1 |
2 |
3 |
4 |
5 |
||||||||||||
Символ оболочки |
K |
L |
M |
N |
O |
||||||||||||
Максимальное число электроновв оболочке |
2 |
8 |
18 |
32 |
50 |
||||||||||||
Орбитальное квантовое число l |
0 |
0 |
1 |
0 |
1 |
2 |
0 |
1 |
2 |
3 |
0 |
1 |
2 |
3 |
4 |
||
Символ подоболочки |
1s |
2s |
2p |
3s |
3p |
3d |
4s |
4p |
4d |
4f |
5s |
5p |
5d |
5f |
5g |
||
Максимальное число электронов в подоболочке |
2 |
2 |
6 |
2 |
6 |
10 |
2 |
6 |
10 |
14 |
2 |
6 |
10 |
14 |
18 |
||
т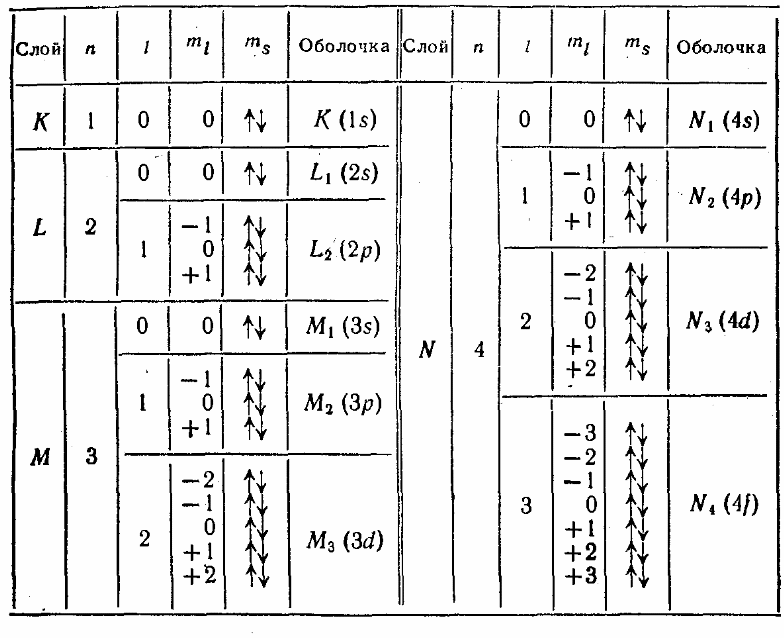 а
же таблица, но понятнее
а
же таблица, но понятнее
Таблица Менделеева
В современном варианте системы предполагается сведение элементов в двумерную таблицу, в которой каждый столбец (группа) определяет основные физико-химические свойства, а строки представляют собой периоды, в определённой мере подобные друг другу.
Объяснение периодическому закону дала квантовая теория атома.
В основе систематики химических элементов лежит заряд ядра атома, а не его атомная масса (Бор, 1922).
Заряд ядра любого атома выражается целым числом Z в единицах элементарного заряда е, равного заряду одного электрона, взятому со знаком плюс.
Число Z определяет номер химического элемента в периодической системе и называется его порядковым номером. Если атом электрически нейтрален, то число электронов в атомной оболочке равно Z.
Свойства элементов зависят от числа электронов в атомной оболочке и ее строения.
Химические свойства элементов определяются периферийными электронами.
Современное объяснение периодической системы элементов основано на трех принципах.
Принцип первый: состояние атомной оболочки характеризуется состояниями ее отдельных электронов, которые полностью определяются четырьмя квантовыми числами:
Принцип второй - Паули: В атоме может существовать только один электрон в состоянии, характеризуемом данными значениями четырех квантовых чисел. Это означает, что два электрона, связанные в одном и том же атоме, должны различаться значениями, по крайней мере, одного квантового числа.
Принцип третий: атом устойчив тогда, когда находится в состоянии с наименьшей возможной энергией (правило Хунда). Это означает, что при присоединении к системе нового электрона его энергия связи должна быть максимально возможной.
ОСТААЛЬНОЕ ГОВНО ПРО ЗАПОЛЕНИЕ НА БУМАЖКЕ ЕБУЧЕЙ
2. 1. Волны де Бройля, длина волны электрона, ускоренного в электрическом потенциале. Волновые свойства частиц, опыты Дэвиссона и Джермера.
Волны де Бройля – волны, связанные с любой движущейся материальной частицей. Любая движущаяся частица (например, электрон) ведёт себя не только как локализованный в пространстве перемещающийся объект - корпускула, но и как волна, причём длина этой волны даётся формулой λ = h/р, где h = 6.6·10-34 Дж.сек – постоянная Планка, а р – импульс частицы. Эта волна и получила название волны де Бройля (в честь французского физика-теоретика Луи де Бройля, впервые высказавшего гипотезу о таких волнах в 1923 г.). Если частица имеет массу m и скорость v << с (с – скорость света), то импульс частицы р = mv и дебройлевская длина волны связаны соотношением λ = h/mv.
Длина волны де Бройля тем меньше, чем больше масса частицы и её скорость. Например, частице с массой в 1 кг, движущейся со скоростью 1 м/с, соответствует волна де Бройля с длиной волны примерно равной 6,626*10^-34 м, что лежит далеко за пределом, доступным наблюдению. Поэтому волновые свойства несущественны в механике макроскопических тел. Для электронов же с энергиями от 1 эВ до 10 000 эВ длина волны де Бройля лежит в пределах от ~ 1 нм до 10−2 нм, то есть в интервале длин волн рентгеновского излучения. Поэтому волновые свойства электронов должны проявляться, например, при их рассеянии на тех же кристаллах, на которых наблюдается дифракция рентгеновских лучей
Свет обладает как волновыми, так и корпускулярными свойствами. Волновые свойства проявляются при распространении света (интерференция, дифракция). Корпускулярные свойства проявляются при взаимодействии света с веществом (фотоэффект, излучение и поглощение света атомами).
Свойства фотона как частицы (энергия E и импульс p) связаны с его волновыми свойствами (частотой ν и длиной волны λ) соотношениями
E = hν; p = hν / c = h / λ, |
|
|
Опыт Дэвиссона-Джермера
Проводилось
исследование отражения электронов от
монокристалла никеля. Установка включала
в себя монокристалл никеля, сошлифованный
под углом и установленный на держателе.
На плоскость шлифа направлялся
перпендикулярно пучок монохроматических
электронов. Скорость электронов
определялась напряжением U{\displaystyle
\ U} на
электронной пушке:
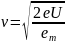
{\displaystyle \upsilon ={\sqrt {\frac {2eU}{m_{e}}}}.}Под углом {\displaystyle \ \theta } к падающему пучку электронов устанавливался цилиндр Фарадея, соединённый с чувствительным гальванометром. По показаниям гальванометра определялась интенсивность отражённого от кристалла электронного пучка. Вся установка находилась в вакууме.
В опытах измерялась интенсивность рассеянного кристаллом электронного пучка в зависимости от угла рассеяния {\displaystyle \ 0<\theta <90^{o},} от азимутального угла {\displaystyle \ 0<\varphi <360^{o}}, от скорости {\displaystyle \ \upsilon } электронов в пучке.
Опыты показали, что имеется ярко выраженная выборочность рассеяния электронов. При различных значениях углов и скоростей, в отражённых лучах наблюдаются максимумы и минимумы интенсивности. Условие максимума:
{\displaystyle
\ \Delta =2d\sin \theta =\lambda n,n=1,2,...}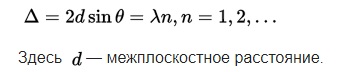
Таким образом наблюдалась дифракция электронов на кристаллической решетке монокристалла. Опыт явился блестящим подтверждением существования у микрочастиц волновых свойств.
Так как дифракционная картина исследовалась для потока электронов, то необходимо было доказать, что волновые свойства присущи не только потоку большой совокупности электронов, но и каждому электрону в отдельности. Это удалось экспериментально подтвердить в 1948 году советском физику В. А. Фабриканту. Он показал, что даже в случае столь слабого электронного пучка, когда каждый электрон проходит через прибор независимо от других (промежуток времени между двумя электронами в 104 раз больше времени прохождения электроном прибора), возникающая при длительной экспозиции дифракционная картина не отличается от дифракционных картин, получаемых при короткой экспозиции для потоков электронов, в десятки миллионов раз более интенсивных. Следовательно, волновые свойства частиц не являются свойством их коллектива, а присущи каждой частице в отдельности.
Впоследствии дифракционные явления обнаружили также для нейтронов, протонов, атомных и молекулярных пучков. Это окончательно послужило доказательством наличия волновых свойств микрочастиц и позволило описывать движение микрочастиц в виде волнового процесса, характеризующегося определенной длиной волны, рассчитываемой по формуле де Бройля. Открытие волновых свойств микрочастиц привело к появлению и развитию новых методов исследования структуры веществ, таких, как электронография и нейтронография, а также к возникновению новой отрасли науки — электронной оптики.
2. Классификация элементарных частиц, лептоны, адроны. Свойства элементарных частиц (заряд, спин и т.Д.). Античастицы. Кварковая модель адронов.
Элементарные частицы обычно подразделяют на 4 класса. К одному из них относится тоько одна частица – фотон. Второй класс образуют лептоны, третий – мезоны, четвертый – барионы. Мезоны и барионы часто объединяют одним классном сильно взаимодействующих частиц, называемых адронами.
Краткая характеристика: страницы 267-268 Савельева моего.
Каждая частица описывается набором физических величин – квантовых чисел, определяющих её свойства. Наиболее часто употребляемые характеристики частиц следующие.
Масса частицы, m. Массы частиц меняются в широких пределах от 0 (фотон) до 90 ГэВ (Z-бозон). Z-бозон - наиболее тяжелая из известных частиц. Однако могут существовать и более тяжелые частицы. Массы адронов зависят от типов входящих в их состав кварков, а также от их спиновых состояний.
Время жизни, τ. В зависимости от времени жизни частицы делятся на стабильные частицы, имеющие относительно большое время жизни, и нестабильные.
К стабильным частицам относят частицы, распадающиеся по слабому или электромагнитному взаимодействию. Деление частиц на стабильные и нестабильные условно. Поэтому к стабильным частицам принадлежат такие частицы, как электрон, протон, для которых в настоящее время распады не обнаружены, так и π0-мезон, имеющий время жизни τ = 0.8×10-16 с.
К нестабильным частицам относят частицы, распадающиеся в результате сильного взаимодействия. Их обычно называют резонансами. Характерное время жизни резонансов - 10-23-10-24 с.
Спин J. Величина спина измеряется в единицах ħ и может принимать 0, полуцелые и целые значения. Например, спин π-, К-мезонов равен 0. Спин электрона, мюона равен 1/2. Спин фотона равен 1. Существуют частицы и с большим значением спина. Частицы с полуцелым спином подчиняются статистике Ферми-Дирака, с целым спином - Бозе–Эйнштейна.
Электрический заряд q. Электрический заряд является целой кратной величиной от е = 1,6×10-19 Кл, называемой элементарным электрическим зарядом. Частицы могут иметь заряды 0, ±1, ±2.
Внутренняя четность Р. Квантовое число Р характеризует свойство симметрии волновой функции относительно пространственных отражений. Квантовое число Р имеет значение +1, -1.
Наряду с общими для всех частиц характеристиками, используют также квантовые числа, которые приписывают только отдельным группам частиц.
Квантовые числа: барионное число В, странность s, очарование (charm) с, красота (bottomness или beauty) b, верхний (topness) t, изотопический спин I приписывают только сильновзаимодействующим частицам - адронам.
Лептонные числа Le, Lμ, Lτ. Лептонные числа приписывают частицам, образующим группу лептонов. Лептоны e, μ и τ участвуют только в электромагнитных и слабых взаимодействиях. Лептоны νe, nμ и nτ участвуют только в слабых взаимодействиях. Лептонные числа имеют значения Le, Lμ, Lτ = 0, +1, -1. Например, e-, электронное нейтрино ne имеют Le= +l; , имеют Le = - l. Все адроны имеют .
Барионное число В. Барионное число имеет значение В = 0, +1, -1. Барионы, например, n, р, Λ, Σ, нуклонные резонансы имеют барионное число В = +1. Мезоны, мезонные резонансы имеют В = 0, антибарионы имеют В = -1.
Странность s. Квантовое число s может принимать значения -3, -2, -1, 0, +1, +2, +3 и определяется кварковым составом адронов. Например, гипероны Λ, Σ имеют s = -l; K+- , K–- мезоны имеют s = + l.