Материал: Физические и химические свойства серной кислоты
Повышение степени превращения SО2 может быть достигнуто разными путями. Наиболее распространенный из них - создание схем двойного контактирования.
В производстве серной кислоты контактным методом окисление SО2 по реакции SO2+1/2O2↔SO3+Q происходит в присутствии катализатора. Способностью ускорять окисление SO2 обладают различные металлы, их сплавы и оксиды, некоторые соли, силикаты и многие другие вещества. Каждый катализатор обеспечивает определенную, характерную для него степень превращения. В заводских условиях выгоднее пользоваться катализаторами, при помощи которых достигается наибольшая степень превращения, так как остаточное количество неокисленного SO2 не улавливается в абсорбционном отделении, а удаляется в атмосферу вместе с отходящими газами.
Длительное время лучшим катализатором данного процесса считали платину, которую в мелкораздробленном состоянии наносили на волокнистый асбест, силикагель или сульфат магния. Однако платина, хотя и обладает наивысшей каталитической активностью, очень дорога. Кроме того, ее активность сильно понижается при наличии в газе самых незначительных количеств мышьяка, селена, хлора и других примесей. Поэтому применение платинового катализатора приводило к усложнению аппаратурного оформления из-за необходимости тщательной очистки газа и повышало стоимость готовой продукции.
Среди неплатиновых катализаторов наибольшей каталитической активностью обладает ванадиевый катализатор (на основе пентоксида ванадия V2O5), он более дешевый и менее чувствительный к примесям, чем платиновый катализатор.[1,4]
В производстве серной кислоты в качестве катализатора применяют контактные массы на основе оксида ванадия (V) марок БАВ и СВД, названные так по начальным буквам элементов, входящих в их состав[5].
БАВ (барий, алюминий, ванадий) состав:
Существуют другие изобретения катализаторов. Изобретение относится к катализаторам для окисления диоксида серы и может быть использовано в производстве серной кислоты при переработке газовых смесей с обычным и повышенным содержанием диоксида серы.
Известен катализатор для окисления диоксида серы, состоящий из пятиокиси ванадия с добавками щелочных промоторов соединений натрия, калия, рубидия и (или) цезия на носителе диатомите, содержащем SiO2, CaO. Смесь щелочных промоторов в пересчете на окислы содержит, мас. Na2O 5-30; Rb2O и (или) Cs2O 15-35; K2O 8-35.
Активность катализатора при 485oC 90,2-91% при 420oC 57,8-59,7% при испытании в следующих условиях: V 4000 ч-1, содержание диоксида серы в исходной газовой смеси 7 об. остальное воздух. Механическая прочность на раздавливание 1-2 МПа [6]
Реакция окисления S02 экзотермична; тепловой эффект ее, как и любой химической реакции, зависит от температуры.
В интервале 400-700°С тепловой эффект реакции окисления (в кДж/моль) с
достаточной для технических расчетов точностью может быть вычислен по формуле
Q= 10
142 - 9.26T или 24205 - 2,21T (в ккал/моль) (18)
где Т - температура, К.
Реакция окисления S02 в S03 обратима. Константа равновесия
этой реакции (в Па-0,5) описывается уравнением
![]()
![]() (19)
(19)
где Pso2 , Pso3 , Pо2-равновесные
парциальные Давления SO2, SO3 и О2 , Па. Величина Кр зависит от
температуры:
Таблица 1. Зависимость константы равновесия от температуры
|
t,ºС |
Кр |
t,ºС |
Кр |
|
390 400 425 450 475 500 |
1,801 1,410 0,768 0,437 0,258 0,159 |
525 575 600 625 650 |
0,100 0,044 0,030 0,021 0,015 |
Значения Кр в интервале 390-650 °С могут быть вычислены по формуле
![]()
![]() (20)
(20)
или более точно
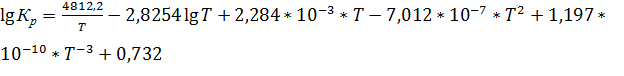
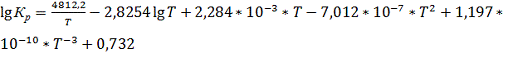 (21)
(21)
2.1 Равновесная степень превращения
Степень превращения S02,
достигаемая на катализаторе, зависит от его активности, состава газа,
продолжительности контакта газа с катализатором, давления и др. Для газа
данного состава теоретически возможная, т. е. равновесная степень превращения
зависит от температуры и выражается уравнением :
![]()
![]() (22)
(22)
где
Pso2 , Pso3 - равновесные парциальные давления SO2 и
SO3.
Подставив
в уравнение (6-5) отношение Pso3/ Pso2 из уравнения (23), получим:
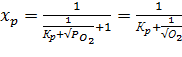
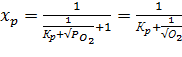 (24)
(24)
Если
обозначить Р - общее давление газа (в Па), а - начальное содержание S02 в
газовой смеси (объема. %), b - начальное содержание кислорода в газовой смеси
(объемн. %), то уравнение (6-6) примет вид:
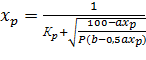
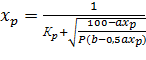 (25)
(25)
Определение равновесной степени превращения по этому уравнению производится методом последовательных приближений. В правую часть уравнения подставляют ожидаемое значение хр и проводят вычисления. Если найденное значение отличается от предварительно принятого, расчет повторяют.
С
понижением температуры и повышением давления газа значение хр возрастает. Это
обусловлено тем, что реакция окисления протекает с выделением тепла и
уменьшением общего числа молекул. Ниже приведены значения хр при различных
температурах н давлении 0,1 МПа для газа, содержащего 7% S02,
11% 02 и 82% N2:
Таблица 2. Зависимость степени превращения от температуры
|
t,ºС |
xp·100 |
t,ºС |
xp·100 |
t,ºС |
xp·100 |
|
390 400 410 420 430 440 450 460 |
99,4 99,2 99,0 98,7 98,4 98,0 97,5 96,9 |
470 480 490 500 510 520 530 540 |
96,2 95,4 64,5 93,4 92,1 90,7 89,2 87,4 |
550 560 570 580 590 650 700 1000 |
85,5 82,5 80,1 77,6 75,0 58,5 43,6 5,0 |
Равновесная степень превращения зависит от соотношения SO2 и О2 в газе, которое
в свою очередь зависит от вида обжигаемого сырья и количества подаваемого
воздуха. Чем больше введено воздуха, тем
меньше S02 и больше 02 содержится в газовой
смеси и, следовательно, тем выше равновесная степень превращения.
Таблица 3. Зависимость равновесной степени превращения от давления
|
t, *С |
Хр* 100 при давлении (в МПа) |
|||||
|
|
0,1 |
0,5 |
1 |
2,5 |
5,0 |
10,0 |
|
400 450 500 550 600 |
99,2 97,5 93,4 85,5 73,4 |
99,6 98,9 96,9 92,9 85.8 |
99,7 99,2 97,8 94,9 89,5 |
99,9 99,5 98,6 96,7 93,3 |
99,9 99,6 99,0 97,7 95,0 |
99,9 99,7 99,3 93,3 96,4 |
Таблица 4. Зависимость равновесной степени превращения хр от состава газовой смеси (при 475 °С и давлении 0,1 МПа)
|
Содержание в газе, объем. % |
хр.100 |
Содержание в газе, объем. % |
хр.100 |
|||
|
SO2 |
|
О2 |
|
SO2 |
О2 |
|
|
2 3 4 5 6 |
|
18,4 16,72 15,28 13,86 12,43 |
97,1 97,0 96,8 96,5 96,2 |
7 8 9 10 |
11,0 9,58 8,15 6,72 |
95,8 95,2 94,3 92,3 |
2.2 Скорость реакции S02 в S03
В производственных условиях существенное значение имеет скорость окисления S02.
Скорость процесса окисления S02 в S03 на ванадиевом катализаторе (в
неподвижном слое) выражается уравнением
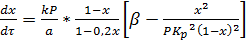
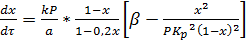 (26)
(26)
![]()
![]() (27)
(27)
где
x-степень превращения, доли единицы; τ - время контакта, с; а-начальная концентрация SOa,
доли единицы; хр - равновесная степень превращения, доли; b -
начальная концентрация кислорода, доли; Т-температура, К; Р - общее давление,
Па; Кр - константа равновесия [уравнение (6-4)], Па-0,5; k -
константа скорости реакции, с-1-Па-1:
![]()
![]() (28)
(28)
k0 - коэффициент; E-энергия активации, Дж/моль;
Энергия активации реакции окисления оксида серы (IV) кислородом в оксид
серы (VI) весьма велика. Поэтому, в отсутствие катализатора реакция окисления
даже при высокой температуре практически не идет. Применение катализатора
позволяет снизить энергию активации и увеличить скорость окисления.[5]
.3 Окисление S02 на
катализаторе в кипящем слое
В кипящем слое происходит весьма интенсивное перемешивание газа с частицами катализатора, в результате чего температура и состав газа практически одинаковы во всем объеме катализатора. При этом значительно увеличивается скорость внешней диффузии S02 и О2 к поверхности катализатора.
Гидравлическое сопротивление кипящего слоя не зависят от размера зерен, поэтому для каталитического окисления S02 в кипящем слое применяются очень мелкие сферические гранулы (радиус 0,5-2 мм), что обеспечивает практически полное использование внутренней поверхности катализатора.
Кинетика процесса окисления диоксида серы во взвешенном слое катализатора
в значительной степени определяется гидродинамическими факторами, так как кроме
интенсивного радиального и осевого перемешивания возможен проскок газа в виде
пузырей. Учесть все факторы очень трудно. Однако опытно-промышленные и
промышленные испытания показывают, что в реакторах большого диаметра
достигаются условия полного перемешивания. Поэтому скорость окисления S02 в этом случае можно принять
одинаковой во всех точках кипящего слоя и, следовательно, расчетное уравнение
(6-19) можно представить в таком виде:
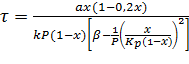
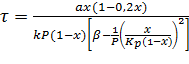 (29)
(29)
Где x - степень превращения на выходе газа из кипящего слоя (она такая же во всем слое катализатора)
Зависимость Хр от температуры, давления и содержания оксида серы (IV) в
обжиговом газе представлена на рис. 1.

Рис. 1. Зависимость равновесной степени превращения оксида серы (IV) в оксид серы (VI) от температуры (А), давления (Б) и содержания оксида серы (IV) в газе (В).
Для газа, получаемого обжигом колчедана и сжиганием серы в воздухе, достижение степени превращения более 98% нецелесообразно, так как это связано с резким увеличением количества катализатора. Между тем при высокой производительности сернокислотных установок (строящихся в настоящее время) и степени превращения 98% санитарная норма содержания S02 в атмосфере может быть достигнута только в случае сооружения очень высокой (и поэтому дорогой) трубы для отходящих газов или при проведении дополнительной санитарной очистки отходящих газов от S02- Например, при производительности установки 5000 т/сут количество SO2, выбрасываемого в атмосферу (в одной точке), составляет 100 т/сут (в пересчете на H2S04).
Для увеличения конечной степени превращения S02 применяют двойное контактирование (ДК). Сущность его состоит в том, что окисление S02 (контактирование) ведут в две стадии, на первой стадии обеспечивается степень превращения 90%. Затем из реакционной смеси выделяют S03, после чего проводят вторую стадию контактирования, в которой достигается ж=95% от оставшегося S02; общая степень превращения составляет 99,5%.
Реакция
окисления S02 обратима, поэтому общая скорость процесса W
выражается как:
![]()
![]() (30)
(30)
где
![]()
![]() ,
, ![]()
![]() -
скорости прямой и обратной реакций;
-
скорости прямой и обратной реакций; ![]()
![]() ,
,![]()
![]() -константы скорости прямой и обратной реакций; CSO2, CO2 ,
CSO3 - концентрации в газе SО2, О2, SО3; l,m,n
-порядок соответствующей реакции.
-константы скорости прямой и обратной реакций; CSO2, CO2 ,
CSO3 - концентрации в газе SО2, О2, SО3; l,m,n
-порядок соответствующей реакции.
Из уравнения (30) следует, что если SО3 выводится из реакционной смеси после первой стадии контактирования, то перед второй стадией CSO3=0 и r2 =0. Следовательно, скорость процесса увеличивается. В этом случае конечная степень превращения выражается уравнением
![]()
![]() (31)
(31)
где x1, x2, хп- степени превращения на первой, второй (от оставшегося после первой ступени) и на конечной стадиях, доли.
Таким образом, хп = 0,9+ (1-0,9)0,95 = 0,995.
Противоречие между кинетикой и термодинамикой процесса окисления оксида
серы (IV) достаточно успешно снимается конструкцией и температурным режимом
работы контактного аппарата. Это достигается разбивкой процесса на стадии,
каждая из которых отвечает оптимальным условиям процесса контактирования[1].
Таблица 5. Степень превращения на каждой ступени контактного аппарата
|
Слои |
слой первой ступени |
слой второй ступени |
|||
|
|
1 |
2 |
3 |
4 |
5 |
|
Температура газа, оС на входе в слой на выходе из слоя |
420 603 |
465 575 |
450 465 |
430 446 |
410 414 |
|
Хр, % |
71,1 |
83,8 |
94,0 |
90,9 |
93,0 |
3 ТЕХНОЛОГИЯ СЕРНОЙ КИСЛОТЫ
3.1 Сырье для технологии
Исходными реагентами для получение серной кислоты могут быть элементная сера и серосодержащие соединения, из которых можно получить либо серу, либо диоксид серы. Такими соединениями являются сульфиды железа, сульфиды цветных металлов (меди, цинка и пр.), сероводород и ряд других сернистых соединений.
Традиционно основные источники сырья - сера и железный (серный) колчедан. Постепенно доля колчедана как сырьевого источника уменьшается, что связано и с большими транспортными расходами на его транспортировку (кроме серы в нем весьма велика доля других компонентов), и с невозможностью избавиться от отхода - огарка. Значительное место в сырьевом балансе производства серной кислоты занимают отходящие газы цветной металлургии, содержащие диоксид серы.