Материал: Элементы современной физики атомов и молекул_1


Частицы с полуцелым спином (электроны, протоны, нейтроны) описываются антисимметричными волновыми функциями называются фермионами.
Частицы с нулевым или целочисленным спином (π - мезоны, фотоны) описываются симметричными волновыми функциями называются бозонами.
Многоэлектронный атом. Правила распределения электронов по орбиталям. Принцип Паули
Распределение электронов по состояниям
для любого невозбужденного атома происходит на основании следующих
законов:
пpинципа минимума энеpгии, пpинципа запpета Паули, правила Хунда.
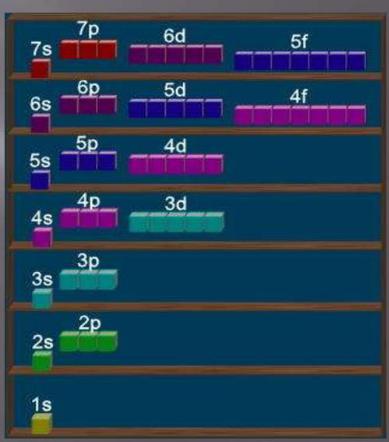
Принцип наименьшей энергии
Наиболее устойчивым состоянием атома считается
то, при котором суммарная энергия его электронов
минимальна.
Это значит, что при заполнении электронами обиталей в многоэлектронном атоме в первую очередь заполняются все максимально возможные свободные орбитали с наименьшей энергией (т.е. уровни с наименьшими квантовыми числами).
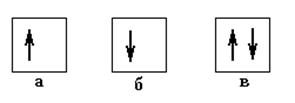
Принцип Паули
два электрона в атоме не могут одновременно находиться в одном и том же состоянии;
в атоме (в любой квантовой системе) не может быть двух фермионов (электронов) с одинаковой набором квантовых чисел n, l, m и mS.
Число электронов, находящихся в данном квантовом состоянии и описываемых набором квантовых чисел:
Z (n, l, m, ms ) 0 |
Z (n, l, m, ms ) 1 |
Общее |
число |
|
электронов, |
n 1 |
находящихся |
в |
квантовом |
Z (n) 2(2l 1) 2n2 |
|
состоянии с данным n: |
l 0 |
|||