Материал: Элементы современной физики атомов и молекул_1
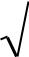
l – орбитальное (азимутальное) квантовое число
определяет форму электронного облака (орбитали) и характеризует величину орбитального момента импульса электрона в атоме.
Момент импульса электрона относительно ядра:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Le |
l(l 1) |
||
l = 0, 1, 2, …, n – 1. |
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
l |
0 |
1 |
2 |
3 |
4 |
|
5 |
|
|
|
|
|
|
|
|
|
|
|
|
символ |
s |
p |
d |
f |
g |
|
h |
|
|
|
|
|
|
|
|
|
|
|
|
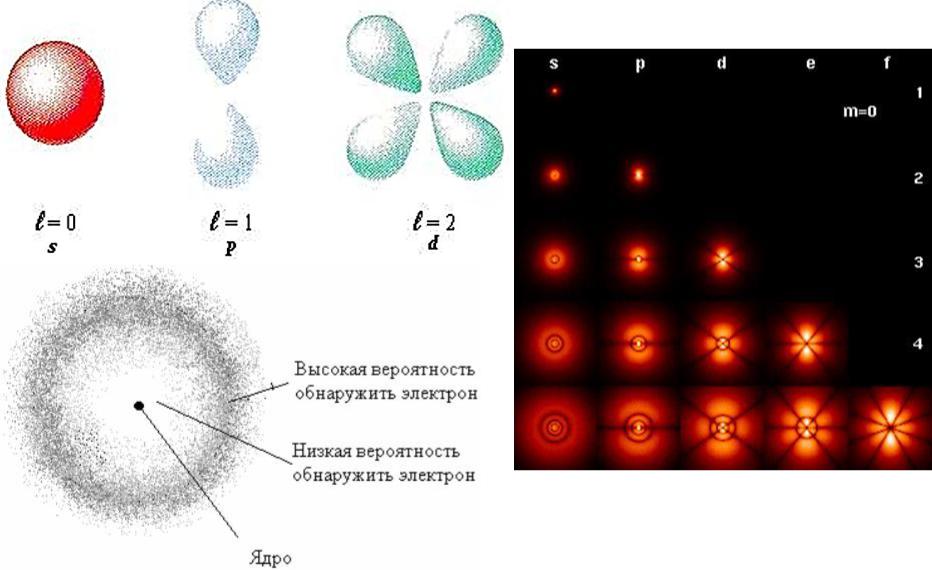
Область пространства, в которой высока вероятность обнаружить электрон (не менее 0,95%), называется
орбиталью.
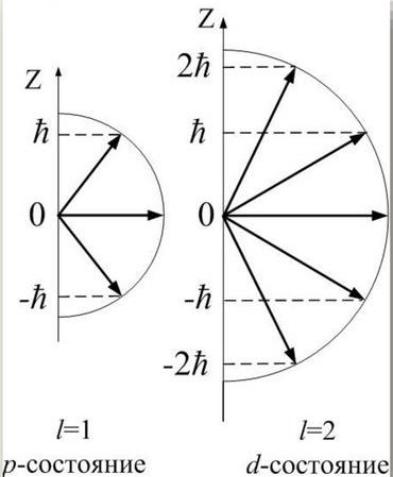
m - магнитное квантовое число
определяет проекцию вектора орбитального момента импульса электрона атома на направление внешнего магнитного поля (ориентацию орбитали в пространстве).
(Ll )z m
m = 0, ±1, ±2, …, ±l.
Всего таких ориентаций в пространстве, т.е. состояний электрона, будет 2l + 1
Эффект Зеемана – в магнитном поле уровень с главным квантовым числом n расщепляется на 2l + 1 подуровней.
Общее число состояний:
n 1
N (2l 1) n2
l 0
Общее число состояний при заданном n с учетом спина:
N 2n2

Опыты Штерна и Герлаха
(экспериментальное доказательство квантования проекции магнитного момента атома на направление магнитного поля)
Если бы момент импульса атома |
(его |
|
магнитный момент |
) мог принимать |
|
произвольные |
ориентации |
в |
пространстве (т.е. в магнитном поле), то
наблюдалось |
бы |
непрерывное |
|
распределение |
попаданий |
атомов |
|
серебра на фотопластинку с |
большой |
||
плотностью попаданий в середине.
Но на фотопластинке получились две резкие полосы – все атомы отклонялись в магнитном поле двояким образом, соответствующим лишь двум возможным ориентациям магнитного момента.
Этим доказывался квантовый характер магнитных моментов электронов.